Навигация по справочнику TehTab.ru: главная страница / / Техническая информация / / Свойства рабочих сред / / Вода, лед и снег / / Свойства воды (h3O) при температурах от 0 до 100°С при атмосферном давлении = 1,013 бар. Плотность. Давление насыщенных паров (=saturation vapor pressure). Удельная энтальпия (=specific enthalpy). Теплоемкость (=specific heat). Объемная теплоемкость…..
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Нашли ошибку? Есть дополнения? Напишите нам об этом, указав ссылку на страницу. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
TehTab.ru Реклама, сотрудничество: [email protected] | Обращаем ваше внимание на то, что данный интернет-сайт носит исключительно информационный характер. Информация, представленная на сайте, не является официальной и предоставлена только в целях ознакомления. Все риски за использование информаци с сайта посетители берут на себя. Проект TehTab.ru является некоммерческим, не поддерживается никакими политическими партиями и иностранными организациями. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Адрес этой страницы (вложенность) в справочнике dpva.ru: главная страница / / Техническая информация / / Рабочие среды / / Вода, лед и снег (хладагент R718) / / Свойства воды при температурах 0 — 100°С при атмосферном давлении. Плотность воды. Давление насыщенных паров воды (=saturation vapor pressure). Удельная энтальпия воды (=specific enthalpy). Теплоемкость воды (=specific heat). Объемная теплоемкость воды Поделиться:
Поиск в инженерном справочнике DPVA. Введите свой запрос: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Если Вы не обнаружили себя в списке поставщиков, заметили ошибку, или у Вас есть дополнительные численные данные для коллег по теме, сообщите , пожалуйста. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Коды баннеров проекта DPVA.ru Консультации и техническая | Проект является некоммерческим. Информация, представленная на сайте, не является официальной и предоставлена только в целях ознакомления. Владельцы сайта www.dpva.ru не несут никакой ответственности за риски, связанные с использованием информации, полученной с этого интернет-ресурса. Free xml sitemap generator | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Изохорная теплоемкость водно-углеводородной смесин-гексан вода Текст научной статьи по специальности «Химические науки»
ИЗОХОРНАЯ ТЕПЛОЕМКОСТЬ ВОДНО-УГЛЕВОДОРОДНОЙ СМЕСИ Н-ГЕКСАН — ВОДА*
Г.В. Степанов, Е.И. Безгомонова, С.М. Оракова (Институт физики им. Х.И. Амирханова Дагестанского НЦ РАН)
Изохорная теплоемкость является очень важным параметром для определения термодинамических свойств жидкостей и газов, фазовых переходов, критических и сверхкритических явлений теплоемкости. Поэтому исследование изохорной теплоемкости водноуглеводородных систем, несомненно, будет представлять интерес в связи с интенсивным развитием энергетической, газовой, нефтяной и нефтехимической отраслей промышленности.
Изохорная теплоемкость воды и н-алканов достаточно подробно исследована [1, 2], в отличие от бинарных водно-углеводородных систем, которые требуют экспериментального изучения.
Исследования изохорной теплоемкости (Су) системы н-гексан -вода в широком диапазоне температур, плотностей и концентраций были проведены на адиабатическом калориметре Х.И. Амирханова [1, 3-6]. Для исследований использовался калориметр объемом 432,61±0,02 см при комнатной температуре. 4,5 —
3,5 —
3,0 ———1————1————1————1————1
480 485 490 495 500
Т, К
Рис. 1. Зависимость изохорной теплоемкости от температуры для концентрации х = 0,2 м.д. Н2О по изохоре V = 3,96 см /г
В интервале концентраций от 0,256 до 0,935 м.д. Н2О первый скачок на температурной зависимости С обусловлен фазовым переходом жидкость — газ слабого раствора воды в н-гексане в присутствии жидкой фазы воды, второй скачок — фазовым переходом жидкость -жидкость или жидкость (Н2О) — паровая фаза (н-гексана) (растворение компонентов).
Фазовый переход жидкость — жидкость характеризуется плавным изменением теплоемкости, растянутым в некотором интервале температур (1-2 К). Теплоемкость при фазовом переходе жидкость -газ для некритических изохор изменяется более резко в интервале 0,1-0,3 К (рис. 2).
г, к
Рис. 2. Зависимость изохорной теплоемкости от температуры для концентрации х = 0,615 м.д. Н2О по изохоре V = 3,496 см /г
Из рис. 1, 2 видно, что изохорная теплоемкость очень точно по скачку на температурной зависимости фиксирует момент фазового перехода, что позволяет легко построить фазовую диаграмму смеси вода -углеводород.
На рис. 3 приведена построенная по данным изохорной теплоемкости фазовая диаграмма в Т-х координатах.
675
650
625 600 « 575 550 525 500 475
450
газовая
фаза
0
V»
/ ж1+ж2
кт
& вккт
— ж+г / /4
ж1+ж2+г л.
V
дкт
\
\
I
I I I I 1 *
I
Ь.
КТ2
-со
0,0
0,2 0,4 0.8 0,0
х, мольные доли воды
1.0
Рис. 3. Фазовая диаграмма системы вода — н-гексан в Т-х координатах
Поскольку н-гексан является более летучим компонентом, он располагается над поверхностью воды и при увеличении температуры по изохоре происходит фазовый переход жидкость — газ н-гексана (вернее, слабый раствор воды в н-гексане) над поверхностью воды. Вода в этом случае выполняет роль балластного объема. В зависимости от содержания смеси изохора может быть жидкостной (т.е. р > рк), паровой (р < рк) или критической.
Эксперимент по измерению изохорной теплоемкости системы н-гексан — вода для составов 0,256; 0,615; 0,854; 0,935 м.д. Н2О показал, что форма кривых фазового равновесия системы жидкость — пар н-гексана в присутствии жидкой фазы воды очень похожа на кривую фазового равновесия чистого н-гексана (рис. 4) с максимумом в критической точке. Разница лишь в том, что максимум кривых с увеличением концентрации воды смещается в сторону больших плотностей, т.е. критическая плотность постоянно изменяется (см. рис. 4), но критические температуры для всех составов одинаковы и совпадают с Тс = 494,69 К верхней конечной критической точки (ВККТ) состава
0,256 м. более летучего компонента в присутствии жидкой фазы воды на кривых фазового равновесия жидкость — пар (рис. 5).
р, кг/м3
Рис. 5. Кривая фазового равновесия для всех концентраций:
▲ — 0,256 м.д. Н2О; А — 0,615 м.д. Н2О; * — 0,854 м.д. Н2О; о — 0,935 м.д. Н2О
Все кривые фазового равновесия совпадают между собой в пределах погрешности эксперимента. Совпадают и критические параметры: Тс = 494,69 К; рс = 225,49 кг/м3 (для чистого н-гексана Тс = 507,85 К; рс = 234 кг/м3). Это позволяет предположить, что для интервала концентраций от 0,256 до 0,935 м.д. Н2О более летучий компонент будет представлять собой раствор воды в н-гексане состава 0,256 м.д. Н2О.
Зависимость изохорной теплоемкости от температуры по критическим изохорам для составов 0,615; 0,854 и 0,935 м.д. Н2О представлена на рис. 6.
Су,
8.0 -I
7.5 —
7.0 —
6.5 —
6.0 —
5.5 —
5.0 —
4.5 —
4. 0—
492
а б в Т,К
Рис. 6. Зависимость изохорной теплоемкости от температуры системы вода — н-гексан по критическим изохорам для составов: а — х = 0,615 м.д. Н2О, v = 3,496 см3/г; б — х = 0,854 м. д. Н2О, v = 2,504 см3/г; в — х = 0,935 м. д. Н2О, v = 2,0 см3/г
Кривые изохорной теплоемкости на рис. 6 аналогичны соответствующим кривым теплоемкости для однокомпонентных жидкостей и описываются скейлинговой зависимостью.
Уменьшение изохорной теплоемкости смеси при увеличении концентрации воды объясняется уменьшением флуктуационной составляющей теплоемкости слабого раствора воды в н-гексане при постоянной теплоемкости воды.
Список литературы
1. Амирханов Х.И. Изохорная теплоемкость воды и водяного пара / Х.И. Амирханов, Г.В. Степанов, Б.Г. Алибеков. — Махачкала: Даг-книгоиздат, 1969. — 216 с.
2. Амирханов Х.И. Изохорная теплоемкость и другие калорические свойства углеводородов метанового ряда / Х.И. Амирханов, Б.Г. Алибеков, Д.И. Вихров, В. А. Мирская. — Махачкала: Дагкнигоиз-дат, 1981. — 135 с.
3. Kamilov I.K. The experimental investigation of Cv, P,V,T — properties and the equation of state of the n-hexane — water system / I.K. Kamilov,
кДж/(кг • К)
—I———————1-1 —i————1———1— i-1-1-1-1
494 496 498 494 496 498 493 494 495 496 497
G.V. Stepanov, L.V. Malisheva at al. // Fluid Phase equilibrium 1996. -V. 125. — P. 177-184.
4. Степанов Г.В. Термодинамические свойства смеси вода -н-гексан при критических и сверхкритических параметрах / Г.В. Степанов, К.А. Шахбанов, Л.В. Малышева // ТВТ. — 1997. — Т. 35. — № 2. -С. 228-233.
5. Kamilov I.K. Liquid-Liquid Vapor, Liquid-Liquid, and Liquid-Vapor Phase Transitions in Aqueous n-Hexane Mixtures from Isochoric Heat Capacity Measurements / I.K. Kamilov, G.V. Stepanov,
I.M. Abdulagatov at al. // J. Chem. Eng. Data. — 2001. — V. 46. — № 6. -P. 1556-1567.
6. Безгомонова Е.И. Определение линии азеотропа из калорических данных / Е.И. Безгомонова, С.М. Оракова, Г.В. Степанов, К.А. Шахбанов // ЖФХ. — 2007. — Т. 81. — № 12. — С. 2150-2153.
7. Степанов Г. В. // Химия и компьютерное моделирование. Бут-леровские сообщения: материалы Х конф. по теплоф. св-вам веществ (Приложение к журналу: спецвыпуск) / Г. В. Степанов, А. Р. Расулов, Е.И. Милихина, Г.М. Атаев. — Казань. — 2002. — № 10. — С. 58-60.
Термодинамика воды и пара IAPWS-IF97
Термодинамика воды и пара IAPWS-IF97
Программа КИП и А (PRO)
Расчеты термодинамических свойств воды и пара применяются довольно широко в метрологической практике, например при расчете сужающих устройств. Основных базисных методик в настоящее время две — два стандарта организации IAPWS (Международной Организации Свойств Воды и Пара) — IAPWS-95 и IAPWS-97.
IAPWS-95 возникла раньше, рекомендуема для научных расчетов. В России аналог — ГСССД 187-99. Недостатком являлся медленный алгоритм компьютерных расчетов. Поэтому вскоре появился более быстрый индустриальный стандарт IAPWS-97, применяемый в системах АСУТП. Разница в расчетах небольшая, но все таки есть.
В программе КИП и А расчеты выполнены в стандарте IAPWS-IF97. Входные и рассчитываемые параметры приведены в таблице ниже:
| Рассчитываемые параметры | Пары входных параметров: p — абсолютное давление T — температура h — удельная энтальпия s — удельная энтропия | ||||
| v | Удельный объем | p,T | p,h | p,s | h,s |
| ρ | Плотность | + | + | + | + |
| s | Энтропия | + | + | + | + |
| h | Энтальпия | + | + | + | + |
| u | Внутренняя энергия | + | + | + | + |
| g | Свободная энергия Гиббса | + | — | — | — |
| Cp | Изобарная теплоемкость | + | + | + | + |
| Cv | Изохорная теплоемкость | + | + | + | + |
| Kt | Изотермическая сжимаемость | + | + | + | + |
| λ | Коэффициент теплопроводности | + | + | + | + |
| k | Термический коэффициент диффузии | + | + | + | + |
| η | Динамическая вязкость | + | + | + | + |
| ν | Кинематическая вязкость | + | + | + | + |
| w | Скорость звука | + | + | + | + |
| αv | Изобарный коэффициент расширения | + | + | + | + |
| Pr | Число Прандтля | + | + | + | + |
| ε | Диэлектрическая постоянная | + | + | + | + |
При запуске модуля расчетов термодинамических свойств воды и пара, появляется окно (рисунок слева, для Android устройств), с изначально валидными входными параметрами давления и температуры рассчитываемой среды. Сразу же происходит расчет выходных величин, указанных в таблице выше.
Допустимыми являются значения температуры от 0 до 1000°C и давления от 10 Па до 100 МПа.
При изменении входных параметров, меняются рассчитываемые величины. Если входные параметры выходят за допустимые пределы, значения выходных величин устанавливаются равными 0.
В программе была использована библиотека функций IAPWS-IF97, компании Hummeling Engineering.
Теплофизические свойства воды | Блог Александра Воробьева
Опубликовано 22 Апр 2018
Рубрика: Теплотехника | 7 комментариев
Зачем искать и листать бумажные таблицы справочников? Они больше вам не нужны! Предлагаемые вниманию пользовательские функции (далее – ПФ) Полковова Вячеслава Леонидовича помогут мгновенно, с высокой точностью рассчитать теплофизические свойства воды.
В базовом пакете 6 функций. По заданным пользователем давлению и температуре воды вычисляются: объемная плотность, энтальпия, динамическая вязкость, изобарная теплоемкость, теплопроводность и число Прандтля.
При запуске файла Excel на предупреждение системы безопасности следует выбрать «Не отключать макросы». Если выбрать «Отключить макросы», то ПФ работать не будут.
В таблице, представленной ниже, приведены сводные данные по точности расчёта базовым пакетом ПФ физических параметров воды в диапазоне абсолютных давлений 0,1÷25 МПа и температур 0÷150 °С. Оценки погрешностей выполнены в сравнении с табличными данными из [1].
Пользовательские функции написаны на встроенном в Excel языке VBA. Можно посмотреть текст программ в папке Module, открыв редактор: Сервис – Макрос – Редактор Visual Basic.
Функции можно использовать при расчетах в любой ячейке листа Excel. (Конечно, модули с программами должны быть предварительно записаны в вашем файле.)
Процедура вызова требуемой пользовательской функции:
1. В выбранной ячейке листа Excel ставится знак “=”.
2. В строке формул нажимается “fx” – вызов формулы.
3. Из представленных категорий функций выбирается категория “Определённые пользователем”.
4. Из представленного перечня пользовательских функций выбирается требуемая пользовательская функция.
5. Заполняются аргументы функции согласно представленной таблице.
6. После ввода последнего аргумента в ячейке выводится результат расчёта (вычисленное значение пользовательской функции).
7. Нажатием кнопки “ОК” в представленной таблице вычисленное значение пользовательской функции переносится в выбранную ячейку листа Excel
Примечание: Аргументы функции могут вводиться в виде числовых значений, либо путем обращения к ячейкам, в которых представлены значения аргументов.
Литература:
1. А.А. Александров, Б.А. Григорьев. «Таблицы теплофизических свойств воды и водяного пара». Справочник. Москва, «МЭИ», 1999.
2. МИ 2412-97 «Рекомендация. ГСИИ. Уравнения измерений тепловой энергии и количества теплоносителя».
P. S.:
Публикации пользовательских функций Полковова В.Л. будут продолжены. Вячеслав Леонидович написал более восьмидесяти бесценных ПФ, имеющих огромное прикладное значение. Представленный базовый пакет ПФ используется во многих расчетах при решении конкретных практических задач, которые будут рассмотрены в следующих статьях.
Инженеры-теплотехники и все интересующиеся темой, подписывайтесь на анонсы в окне, расположенном вверху страницы или сразу после статьи, и получайте уведомления о публикациях новых материалов.
Ссылка на скачивание файла: teplofizicheskie-svojstva-vody (xls 72,0KB).
Другие статьи автора блога
На главную
Статьи с близкой тематикой
Отзывы
Теплоносители
Теплоносители
Многие технологические процессы в химической промышленности и в энергетике требуют подвода или отвода тепловой энергии. Для этого используют теплоносители, которые поглощают или отдают тепловую энергию в теплообменных аппаратах.
Теплагенты
Теплагенты разделяют на три класса:
- Высокотемпературные газообразные.
- Пары жидкостей.
- Жидкие.
Диапазоны температур, в которых образуются и используются теплагенты различных химических составов и фазовых состояний, представлены на рисунке ТН-1.
Рисунок ТН-1. Интервалы рабочих температур теплагентов.
Высокотемпературные газообразные
Это отходящие дымовые газы, образующиеся при сжигании углеводородного топлива в печах, топках, камерах сгорания, турбинах. Обладают низкой теплоёмкостью, поэтому могут в процессе теплообмена отдать относительно немного тепловой энергии, менее 300 кДж / кг. Имеют низкий коэффициент теплоотдачи.
Высокая температура отходящих газов побуждает всё же утилизировать их тепловую энергию. Для этого широко используются регенеративные теплообменники, см. раздел сайта Регенеративные теплообменники.
Достоинства и недостатки отработанных и топочных газов
Преимущества | Недостатки |
|
|
Водяной пар
Наиболее широко используются установки для получения насыщенного пара, котлы получения перегретого пара для энергетических установок, котлы – утилизаторы, выпарные установки.
Паровые котлы, обеспечивающие получение насыщенного пара, используются на химических предприятиях.
Паровые котлы на тепловых электростанциях снабжают перегретым паром паровые турбины, вращающие роторы электрогенераторов.
Котлы-утилизаторы используют на химических производствах для переработки тепловой энергии, высвобождающейся при экзотермических химических процессах. Так, при сжигании серы при производстве серной кислоты диоксид серы имеет температуру около 1 000 оС. Для дальнейшей переработки температуру необходимо понизить до 320 — 400 оС. Для этого за печью обжига устанавливается котёл – утилизатор.
Выпарные установки, обеспечивающие концентрирование водных растворов солей, в качестве побочного продукта выдают пар невысокого давления. Его можно компримировать, т.е. превратить в пар более высокого давления. Даже с учётом затрат на энергию для компрессора, осуществляющего компримирование, это выгодно. Компримированный пар используется для подогрева самой выпарной установки.
Достоинства и недостатки водяного пара как теплагента
Преимущества | Недостатки |
|
Высокотемпературные органические носители
Для нагревания выше 190 оС вместо водяного пара используют высокотемпературные органические жидкости (ВОТ). Такими жидкостями могут быть этиленгликоль, глицерин, нафталин, продукты хлорирования дифенила и полифенолов, их смеси.
Подобрав соответствующий теплагент, можно, например, производить нагрев парами дифенила при атмосферном давлении и температуре теплоносителя 260 оС. Для получения пара такой температуры он должен иметь давление 4,6 МПа.
Достоинства и недостатки ВОТ как теплагента
Преимущества | Недостатки |
|
|
Вода
Горячая вода получается как побочный продукт в котлах, предназначенных для получения водяного пара.
Она может быть получена как конденсат, образующийся при работе выпарных установок.
Она может быть получена специально в водогрейных котлах.
Достоинства и недостатки воды как теплагента
Преимущества | Недостатки |
|
Минеральные масла
Минеральные масла – это жидкие смеси высококипящих углеводородов с температурой кипения 300 – 600 оС. Получаются при переработке нефти. Эти среды используются для транспортировки тепла от топочных газов к потребителю достаточно давно, если нельзя организовать транспортировку перегретой водой или паром высокого давления.
Достоинства и недостатки минеральных масел как теплагента
Преимущества | Недостатки |
|
|
Ионные высокотемпературные теплоносители
Ионными высокотемпературными теплагентами являются расплавы солей. Широко используется смесь, состоящая из 40% Na NO2, 7% Na NO3, 53% K NO3. Также применяется смесь 45% Na NO2 и 55% KNO3.
Температура плавления смесей – около 140 оС.
ИВТ используются для транспортировки тепла, получаемого от дымовых газов.
Достоинства и недостатки ИВТ как теплагента
Преимущества | Недостатки |
|
|
Кремнийорганические высокотемпературные теплоносители
Кремнийорганические высокотемпературные теплоносители (КВТ) относятся к группе ионных высокотемпературных органических теплоносителей.
К КВТ относят силиконы, например, тетракрезилоксисилан, тетракселилоксисилан, арил- и алкилполисилоксаны.
Тетракрезилоксисилан является эфиром кремниевой кислоты и крезола. Это жидкость светло – коричневого цвета с температурой плавления – 36 оС, кипит при атмосферном давлении при 440 оС.
КВТ используются как транспорт тепла от дымовых газов.
Достоинства и недостатки КВТ как теплагента
Преимущества | Недостатки |
|
|
Жидкометаллические теплоносители
Для транспортировки тепла дымовых газов могут использоваться расплавы металлов с низкой температурой плавления, таких, как свинец, висмут, кадмий, сурьма, олово.
Нижняя рабочая температура таких теплоносителей определяется температурой плавления металла.
Также жидкометаллические теплоносители нашли широкое применение в атомной энергетике.
Достоинства и недостатки жидкометаллических теплоносителей
Преимущества | Недостатки |
|
|
Хладагенты
Хладагенты делятся на жидкие и газообразные, в зависимости от фазового состояния. Фазовое состояние хладагента в ходе теплообмена может изменяться.
Преимущественно в химической промышленности в качестве хладагента используется воздух. Дешевизна и доступность воздуха перевешивает его недостатки как хладагента – низкие плотность и теплоёмкость, низкий коэффициент теплопередачи.
В процессах, связанных с малыми количествами продукции, малотоннажных процессах, используются другие газы, например, элегаз SF6, шестифтористая сера. Плотность элегаза в пять раз больше воздуха, а молярная изобарная теплоёмкость — в три раза.
Высокая стоимость элегаза ограничивает его широкое использование.
Из жидких хладагентов в химической промышленности чаще всего используется вода. Этот хладагент занимает второе место по доступности после воздуха.
Воздух и вода обеспечивают потребности химических производств в хладагентах, если требуется охлаждение до 30 оС.
Отобранное воздухом и водой тепло непосредственно рассеивается в окружающей среде, что существенно снижает стоимость процессов охлаждения.
Охлаждение до более низких температур осуществляется с помощью «посредников» — холодильных машин. Но и они, в конечном итоге, отдают отобранное у объекта охлаждения тепло в окружающую среду.
В качестве хладагента, обеспечивающего доставку холода к объекту охлаждения, может использоваться вода, если рабочие температуры выше температуры ее замерзания. Температуру замерзания можно понизить, добавляя в воду, например, соли, такие, как хлорид кальция. Водные растворы солей называют холодильными рассолами. Они играют роль промежуточного теплоносителя, охлаждаясь при тепловом взаимодействии с рабочим телом холодильной машины (источник холода) и нагреваясь в ходе теплового взаимодействия с охлаждаемой средой, которая является целевым потребителем холода.
Рабочим телом в холодильной машине служат вещества, которые легко конденсируются при повышении давления в компрессоре холодильной машины. Жидкое рабочее тело затем охлаждается, отдавая накопленное тепло окружающей среде в рекуперативном теплообменнике, затем, испаряясь (или адиабатически расширяясь) забирает тепло у промежуточного теплоносителя. В качестве рабочего тела в холодильных машинах используется аммиак, фреоны (хладоны), двуокись углерода (углекислый газ).
В ряде случаев удаётся обойтись без промежуточного теплоносителя, холодильного рассола, и организовать охлаждение целевой среды за счёт её непосредственного теплового взаимодействия с рабочим телом холодильной машины.
Аммиак, фреоны, диоксид углерода и холодильные рассолы составляют класс низкотемпературных жидких хладагентов, обеспечивающих охлаждение в диапазоне температур от – 120 оС до 30 оС,
Для охлаждения в диапазоне от – 120 оС и почти абсолютного нуля по Кельвину используются сжиженные газы, криоагенты – этан, метан, кислород, азот, аргон, гелий.
Интервалы рабочих температур для различных хладагентов представлены на рисунке ТН-2.
Рисунок ТН-2. Интервалы рабочих температур хладагентов.
Воздух
Воздух – прямой источник холода. В большинстве случаев воздух можно сразу использовать как хладагент без предварительной подготовки. Даже если подготовка требуется (снижение влажности и удаление механических взвесей), воздух всё равно остаётся наиболее дешёвым хладагентом.
Теплообменная аппаратура, в которой воздух выступает хладагентом, имеет достаточно высокую стоимость в силу того, что её размеры велики. Низкие плотность воздуха и теплоёмкость приводят к необходимости прокачивать через теплообменник его большие объёмы. Это приводит к большим рабочим сечениям аппаратов. Низкий коэффициент теплоотдачи от стенки к воздуху приводит к необходимости увеличивать площадь поверхности теплообмена со стороны воздуха. Для этого применяют оребрение, см. раздел сайта Поверхностные теплообменники.
Недостатки воздуха, как хладагента (низкая плотность, теплоёмкость, коэффициент теплоотдачи) компенсируются, если осуществлять теплообмен не через стенку теплообменника, а при непосредственном взаимодействии агентов в смесительных теплообменниках, см. раздел сайта Смесительные теплообменники.
Охлаждение со смешением применяется в основном для пары вода – воздух. Частичное испарение воды и капельный унос в процессе её охлаждения и связанные с этим безвозвратные потери воды не существенно увеличивают стоимость технологического процесса. Воздействие на окружающую среду увлажнённого воздуха не слишком велико, хотя всё равно должно приниматься в расчёт.
Наиболее распространёнными аппаратами для охлаждения воды воздухом при их смешении являются градирни, см. раздел сайта Смесительные теплообменники. Охлаждение воды в градирнях происходит как за счёт теплообмена воды и воздуха, но, в основном – за счёт частичного испарения воды при противоточном движении воздуха и воды.
Достоинства и недостатки воздуха как хладагента
Преимущества | Недостатки |
|
|
Вода как хладагент
Вода может служить прямым источником холода, как и воздух. В зависимости от времени года в России температура воды – от 4 до 25 и более градусов. Артезианская вода – от 4 до 12 оС. При проектировании водоохлаждающих установок температуру воды принимают, исходя из самых неблагоприятных, с точки зрения охлаждения, условий.
Для воды, как хладагента, не следует рассчитывать на охлаждение ниже 30 оС за счёт теплопередачи в окружающую среду.
Существует проблема при отборе тепла водой при высоких температурах охлаждаемого вещества. Если температура воды после отвода тепла составляет около 80 оС, то в системе её циркуляции могут выпадать нерастворимые осадки, состоящие из нерастворимых карбонатов, образующихся из гидрокарбонатов кальция и магния. Поэтому следует выбирать режим охлаждения, при котором вода не нагревается свыше 50 оС.
Для уменьшения выпадения нерастворимых осадков в трубах циркуляции воды применяют различные виды водоподготовки для её очистки. На больших химических предприятиях и мощных электростанциях для этого функционируют цеха водоподготовки и соответствующие химические лаборатории.
Особенно высокие требования к воде предъявляются, если она используется в химических реакциях или для приготовления пара.
Использование водоподготовки и требования по охране окружающей среды всё больше заставляют производителей переходить на замкнутые системы водоснабжения, внедряя циклы водооборота.
Достоинства и недостатки воды как хладагента
Преимущества | Недостатки |
|
|
Холодильные рассолы
Холодильные рассолы приготовляются из воды и растворимых солей – хлорид кальция, натрия и пр.
Рассолы применяются как транспорт для доставки холода от холодильной машины к потребителю. Например, мощная холодильная машина ледового дворца на хладонах производит холод. Холодильный рассол растекается по трубам, положенным под ледовой ареной и вызывает образование льда из воды, которой была залита арена.
Вода, которая замерзает при 0 оС, для транспортировки холода в этих условиях не пригодна.
Раствор, который по массе содержит 30% хлорида кальция, замерзает при температуре ниже – 50 оС.
Таким образом, холодильные рассолы могут использоваться в температурном диапазоне от – 50 до + 30 оС.
Совместно с холодильными рассолами в этом температурном диапазоне в качестве хладагентов используются аммиак, фреоны (хладоны) и углекислая кислота.
Достоинства и недостатки холодильных рассолов
Преимущества | Недостатки |
|
|
Аммиак в роли хладагента
Аммиак, NH3 – в н.у. бесцветный газ с резким запахом. При повышенном давлении легко сжижается. Температура плавления аммиака – 77,7 оС, кипит в н.у. при – 33 оС.
Эти свойства и невысокая стоимость производства позволяют использовать аммиак в абсорбционных и компрессионных холодильных машинах.
До настоящего времени аммиак остаётся самым распространённым холодильным агентом.
По физиологическому действию на организм аммиак относится к группе веществ удушающего и нейротропного действия, способных при вдыхании вызвать токсический отёк лёгких и тяжёлое поражение нервной системы.
Поэтому при использовании аммиака должны предусматриваться меры безопасности для обслуживающего персонал и лиц, проживающих или работающих возле мощных холодильных машин, использующих аммиак.
Достоинства и недостатки аммиака как хладагента
Преимущества | Недостатки |
|
|
Фреоны – хладоны
Фреоны (хладоны) – техническое название группы насыщенных алифатических фторсодержащих углеводородов. Используются в качестве хладагентов Фреоны могу содержать хлор и бром. Содержащие атомы хлора фреоны при попадании в атмосферу имеют тенденцию накапливаться в её верхних слоях. Образующийся при их разрушении под действием солнечной радиации свободный хлор губительно действует на озоновый слой атмосферы Земли. Поэтому в настоящее время действует всемирная конвенция, запрещающая использование хлорсодержащих фреонов.
Достоинства и недостатки фреонов
Преимущества | Недостатки |
|
|
Перейти к полной версии
Перейти к мобильной версии
Конвертер удельной теплоёмкости • Термодинамика — теплота • Компактный калькулятор • Онлайн-конвертеры единиц измерения
Конвертер длины и расстоянияКонвертер массыКонвертер мер объема сыпучих продуктов и продуктов питанияКонвертер площадиКонвертер объема и единиц измерения в кулинарных рецептахКонвертер температурыКонвертер давления, механического напряжения, модуля ЮнгаКонвертер энергии и работыКонвертер мощностиКонвертер силыКонвертер времениКонвертер линейной скоростиПлоский уголКонвертер тепловой эффективности и топливной экономичностиКонвертер чисел в различных системах счисления.Конвертер единиц измерения количества информацииКурсы валютРазмеры женской одежды и обувиРазмеры мужской одежды и обувиКонвертер угловой скорости и частоты вращенияКонвертер ускоренияКонвертер углового ускоренияКонвертер плотностиКонвертер удельного объемаКонвертер момента инерцииКонвертер момента силыКонвертер вращающего моментаКонвертер удельной теплоты сгорания (по массе)Конвертер плотности энергии и удельной теплоты сгорания топлива (по объему)Конвертер разности температурКонвертер коэффициента теплового расширенияКонвертер термического сопротивленияКонвертер удельной теплопроводностиКонвертер удельной теплоёмкостиКонвертер энергетической экспозиции и мощности теплового излученияКонвертер плотности теплового потокаКонвертер коэффициента теплоотдачиКонвертер объёмного расходаКонвертер массового расходаКонвертер молярного расходаКонвертер плотности потока массыКонвертер молярной концентрацииКонвертер массовой концентрации в раствореКонвертер динамической (абсолютной) вязкостиКонвертер кинематической вязкостиКонвертер поверхностного натяженияКонвертер паропроницаемостиКонвертер плотности потока водяного параКонвертер уровня звукаКонвертер чувствительности микрофоновКонвертер уровня звукового давления (SPL)Конвертер уровня звукового давления с возможностью выбора опорного давленияКонвертер яркостиКонвертер силы светаКонвертер освещённостиКонвертер разрешения в компьютерной графикеКонвертер частоты и длины волныОптическая сила в диоптриях и фокусное расстояниеОптическая сила в диоптриях и увеличение линзы (×)Конвертер электрического зарядаКонвертер линейной плотности зарядаКонвертер поверхностной плотности зарядаКонвертер объемной плотности зарядаКонвертер электрического токаКонвертер линейной плотности токаКонвертер поверхностной плотности токаКонвертер напряжённости электрического поляКонвертер электростатического потенциала и напряженияКонвертер электрического сопротивленияКонвертер удельного электрического сопротивленияКонвертер электрической проводимостиКонвертер удельной электрической проводимостиЭлектрическая емкостьКонвертер индуктивностиКонвертер реактивной мощностиКонвертер Американского калибра проводовУровни в dBm (дБм или дБмВт), dBV (дБВ), ваттах и др. единицахКонвертер магнитодвижущей силыКонвертер напряженности магнитного поляКонвертер магнитного потокаКонвертер магнитной индукцииРадиация. Конвертер мощности поглощенной дозы ионизирующего излученияРадиоактивность. Конвертер радиоактивного распадаРадиация. Конвертер экспозиционной дозыРадиация. Конвертер поглощённой дозыКонвертер десятичных приставокПередача данныхКонвертер единиц типографики и обработки изображенийКонвертер единиц измерения объема лесоматериаловВычисление молярной массыПериодическая система химических элементов Д. И. Менделеева
Удельная теплоемкость фарфора равна примерно 0,8 Дж/г•°С. Фарфоровая чашка для кофе эспрессо весит приблизительно 60 грамм, значит ее теплоемкость — около 50 Дж/°С. Удельная теплоемкость воды — 4,2 Дж/г•°С. То есть, теплоемкость 50 г кофе эспрессо равна приблизительно 210 Дж/°С.
Общие сведения
Молекулы движутся под воздействием тепла — это движение называется молекулярной диффузией. Чем выше температура вещества, тем быстрее молекулы движутся и тем более интенсивно происходит диффузия. На движение молекул влияет не только температура, но и давление, вязкость вещества и его концентрация, сопротивление диффузии, расстояние, которое проходят молекулы при их перемещениях, и их масса. Например, если сравнить как происходит процесс диффузии в воде и в мёде, когда все другие переменные, кроме вязкости, равны, то очевидно, что молекулы в воде движутся и диффундируют быстрее, чем в мёде, так как у мёда более высокая вязкость.
Для движения молекулам необходима энергия, и чем быстрее они движутся, тем больше энергии им требуется. Тепло — один из видов энергии, используемой в этом случае. То есть, если поддерживать в веществе определенную температуру, то молекулы будут двигаться, а если температуру увеличить, то и движение ускорится. Энергию в форме тепла получают, сжигая топливо, например природный газ, уголь, или древесину. Если нагреть несколько веществ, используя одинаковое количество энергии, то некоторые вещества, скорее всего, будут нагреваться быстрее, чем остальные, из-за более интенсивной диффузии. Теплоемкость и удельная теплоемкость описывают как раз эти свойства веществ.
Удельная теплоемкость определяет какое количество энергии (то есть, тепла) требуется, чтобы изменить температуру тела или вещества определенной массы на определенную величину. Это свойство отличается от теплоемкости, которая определяет количество энергии, необходимое чтобы изменить температуру всего тела или вещества на определенную температуру. В вычислениях теплоемкости, в отличие от удельной теплоемкости, не учитывают массу. Теплоемкость и удельную теплоемкость вычисляют только для веществ и тел в устойчивом агрегатном состоянии, например для твердых тел. В этой статье рассматриваются оба эти понятия, так как они взаимосвязаны.
Теплоемкость и удельная теплоемкость материалов и веществ
Металлы
Так выглядит нагретый до 800°C резистивный нагревательный элемент.
У металлов очень прочная молекулярная структура, так как расстояние между молекулами в металлах и других твердых телах намного меньше, чем в жидкостях и газах. Благодаря этому, молекулы могут двигаться только на очень маленькие расстояния, и, соответственно, для того чтобы заставить их двигаться с большей скоростью необходимо намного меньше энергии, чем для молекул жидкостей и газов. Благодаря этому свойству, их удельная теплоемкость мала. Это значит, что температуру металла поднять очень легко.
Удельная теплоемкость морской воды равна 3993 Дж/кг•K.
Вода
С другой стороны, у воды очень высокая удельная теплоемкость, даже по сравнению с другими жидкостями, поэтому нужно намного больше энергии, чтобы нагреть одну единицу массы воды на один градус, по сравнению с веществами, удельная теплоемкость которых ниже. Вода имеет высокую теплоемкость благодаря прочным связям между атомами водорода в молекуле воды.
Вода — один из главных составляющих всех живых организмов и растений на Земле, поэтому ее удельная теплоемкость играет большую роль для жизни на нашей планете. Благодаря высокой удельной теплоемкости воды, температура жидкости в растениях и температура полостной жидкости в организме животных мало изменяется даже в очень холодные или очень жаркие дни.
Антифриз
Вода обеспечивает систему поддержания теплового режима как у животных и растений, так и на поверхности Земле в целом. Огромная часть нашей планеты покрыта водой, поэтому именно вода играет большую роль в регулировании погоды и климата. Даже при большом количестве тепла, поступающем в результате воздействия солнечного излучения на поверхность Земли, температура воды в океанах, морях и других водоемах увеличивается постепенно, и окружающая температура тоже меняется медленно. С другой стороны, влияние на температуру интенсивности тепла от солнечного излучения велико на планетах, где нет больших поверхностей, покрытых водой, таких как Земля, или в районах Земли, где мало воды. Это особенно заметно, если посмотреть на разность дневных и ночных температур. Так, например, вблизи океана разница между дневной и ночной температурами невелика, но в пустыне она огромна.
Высокая теплоемкость воды также означает, что вода не только медленно нагревается, но и медленно остывает. Благодаря этому свойству воду часто используют как хладагент, то есть, как охлаждающую жидкость. К тому же, использовать воду выгодно благодаря ее низкой цене. В странах с холодным климатом горячая вода циркулирует в трубах для обогрева. В смеси с этиленгликолем ее используют в радиаторах автомобилей для охлаждения двигателя. Такие жидкости называют антифризом. Теплоемкость этиленгликоля ниже, чем теплоемкость воды, поэтому теплоемкость такой смеси тоже ниже, а значит эффективность системы охлаждения с антифризом также ниже, чем системы с водой. Но с этим приходится мириться, так как этиленгликоль не дает воде замерзнуть зимой и повредить каналы системы охлаждения автомобиля. В охлаждающие жидкости, предназначенные для более холодного климата, добавляют больше этиленгликоля.
Теплоемкость в повседневной жизни
При прочих равных условиях, теплоемкость материалов определяет, как быстро они нагреваются. Чем выше теплоемкость, тем больше энергии необходимо, чтобы нагреть этот материал. То есть, если два материала с разной теплоемкостью нагревать одинаковым количеством тепла и в одинаковых условиях, то вещество с меньшей теплоемкостью будет быстрее нагреваться. Материалы с высокой теплоемкостью, наоборот, нагреваются и отдают тепло назад в окружающую среду медленнее.
Суп долго остается горячим в керамической суповой чашке
Кухонные принадлежности и посуда
Чаще всего мы выбираем материалы для посуды и кухонных принадлежностей, основываясь на их теплоемкости. Это в основном касается предметов, которые напрямую контактируют с теплом, например кастрюль, тарелок, форм для выпекания, и другой аналогичной посуды. Например, для кастрюль и сковородок лучше использовать материалы с низкой теплоемкостью, например металлы. Это помогает теплу легче и быстрее передаваться от нагревателя через кастрюлю к продуктам питания и ускоряет процесс приготовления пищи.
С другой стороны, так как материалы с высокой теплоемкостью долго держат тепло, их хорошо использовать для изоляции, то есть когда необходимо сохранить тепло продуктов, и не дать ему уйти в окружающую среду или, наоборот, не дать теплу помещения нагреть охлажденные продукты. Чаще всего такие материалы используют для тарелок и чашек, в которых подают горячую или, наоборот, очень холодную еду и напитки. Они помогают не только сохранить температуру продукта, но и не дают людям обжечься. Посуда из керамики и вспененного полистирола — хорошие примеры использования таких материалов.
Сыр хорошо изолирует продукты под ним и помогает им долго оставаться теплыми
Теплоизолирующие продукты питания
В зависимости от ряда факторов, например содержания воды и жира в продуктах, их теплоемкость и удельная теплоемкость бывает разной. В кулинарии знания о теплоемкости продуктов дают возможность использовать некоторые продукты для изоляции. Если теплоизолирующими продуктами накрыть другую еду, то они помогут этой еде под ними дольше сохранить тепло. Если у блюд под этими теплоизолирующими продуктами высокая теплоемкость, то они и так медленно отдают тепло в окружающую среду. После того, как они хорошо прогреются, они теряют тепло и воду еще медленнее благодаря изолирующим продуктам сверху. Поэтому они дольше остаются горячими.
Пример теплоизолирующего продукта — сыр, особенно на пицце и других похожих блюдах. Пока он не расплавился, он пропускает водяные пары, что позволяет продуктам под ним быстро остыть, так как содержащаяся в них вода испаряется и при этом охлаждает содержащие ее продукты. Растаявший же сыр покрывает поверхность блюда и изолирует продукты под ним. Часто под сыром оказываются продукты с высоким содержанием воды, например соусы и овощи. Благодаря этому у них высокая теплоемкость, и они долго держат тепло, особенно потому, что находятся под расплавленным сыром, который не выпускает наружу водяные пары. Именно поэтому пицца из духовки настолько горяча, что можно легко обжечься соусом или овощами, даже когда тесто по краям уже остыло. Поверхность пиццы под сыром долго не остывает, что делает возможным доставку пиццы на дом в хорошо изолированной термо-сумке.
Белый молочный соус на горячем бутерброде крок-месье изолирует продукты под ним, и помогает им долго оставаться теплыми
В некоторых рецептах соусы используют так же, как и сыр, для теплоизоляции продуктов под ним. Чем больше содержание жира в соусе, тем лучше он изолирует продукты — особенно хороши в этом случае соусы, основанные на масле или сливках. Это опять связано с тем, что жир препятствует испарению воды и, следовательно, отбору тепла, требуемого для испарения.
В кулинарии для термоизоляции иногда используют также материалы, не пригодные в пищу. Повара в странах Центральной Америке, на Филиппинах, в Индии, Таиланде, Вьетнаме и во многих других странах часто используют в этих целях листья банана. Их можно не только собрать в саду, но и купить в магазине или на рынке — их даже импортируют для этих целей в страны, где не выращивают бананы. Иногда в целях изоляции используют алюминиевую фольгу. Она не только предотвращает испарение воды, но и помогает сохранить тепло внутри за счет предотвращения теплопередачи в форме излучения. Если обернуть в фольгу крылышки и другие выступающие части птицы при ее запекании, то фольга не даст им перегреться и сгореть.
Приготовление пищи
У продуктов с высоким содержанием жира, например у сыра, низкая теплоёмкость. Они сильнее нагреваются при меньшем количестве энергии, по сравнению с продуктами с высокой теплоёмкостью, и достигают температур, достаточно высоких для того, чтобы произошла реакция Майяра. Реакция Майяра — это химическая реакция, которая происходит между сахарами и аминокислотами, и изменяет вкус и внешний вид продуктов. Эта реакция важна в некоторых способах приготовления пищи, например для выпечки хлеба и кондитерских изделий из муки, запекания продуктов в духовом шкафу, а также для жарения. Чтобы увеличить температуру продуктов до температуры, при которой протекает эта реакция, в кулинарии используют продукты с высоким содержанием жира.
Сахар в кулинарии
Магазин помадки Maple Leaf (англ. кленовый лист) в городе Ниагара-он-те-Лейк, Онтарио, Канада
Помадку делают из молока, сахара и масла, которые смешивают и нагревают до стадии мягкого шара, то есть до температуры 116 °C (240 °F)
Удельная теплоемкость сахара еще ниже, чем у жира. Так как сахар быстро нагревается до температур более высоких, чем температура кипения воды, работа с ним на кухне требует соблюдения правил безопасности, особенно во время приготовления карамели или конфет. Необходимо быть предельно осторожным, расплавляя сахар, и не пролить его на незащищенную кожу, так как температура сахара достигает 175° C (350° F) и ожог от расплавленного сахара будет очень серьезный. В некоторых случаях необходимо проверить консистенцию сахара, но этого ни в коем случае нельзя делать голыми руками, если сахар нагрет. Часто люди забывают, как быстро и насколько сильно сахар может нагреться, поэтому и получают ожоги. В зависимости от того, для чего нужен расплавленный сахар, его консистенцию и температуру можно проверить, используя холодную воду, как описано ниже.
После того, как смесь нагрели, ее охлаждают
Свойства сахара и сахарного сиропа изменяются в зависимости от того, при какой температуре его готовить. Горячий сахарный сироп может быть жидким, как самый жидкий мед, густым, или где-то между жидким и густым. В рецептах конфет, карамели и сладких соусов обычно указана не только температура, до которой должен быть нагрет сахар или сироп, но и стадия твердости сахара, например стадия «мягкого шара» или стадия «твердого шара». Название каждой стадии соответствует консистенции сахара. Чтобы определить консистенцию кондитер капает несколько капель сиропа в ледяную воду, охлаждая их. После этого консистенцию проверяют на ощупь. Так, например, если охлажденный сироп загустел, но не затвердел, а остается мягким и из него можно слепить шарик, то считается, что сироп в стадии «мягкого шара». Если форму застывшего сиропа очень трудно, но все же можно изменить руками, то он в стадии «твердого шара». Кондитеры часто используют пищевой термометр а также проверяют консистенцию сахара вручную.
Когда помадка остыла, ее разрезают на кусочки
Пищевая безопасность
Помадка готова к продаже
Зная теплоемкость продуктов, можно определить, как долго их нужно охлаждать или нагревать, чтобы достичь температуры, при которой они не будет портиться, и при которой погибают вредные для организма бактерии. Например, чтобы достичь определенной температуры, продукты с более высокой теплоемкостью охлаждают или нагревают дольше, чем продукты с низкой теплоемкостью. То есть, продолжительность приготовления блюда зависит от того, какие в него входят продукты, а также — насколько быстро из него испаряется вода. Испарение важно, так как оно требует больших затрат энергии. Часто, чтобы проверить, до какой температуры нагрелось блюдо или продукты в нем, используют пищевой термометр. Особенно удобно использовать его во время приготовления рыбы, мяса и птицы.
Микроволновые печи
То, насколько эффективно нагревается еда в микроволновой печи, зависит, кроме других факторов, от удельной теплоемкости продуктов. Микроволновое излучение, вырабатываемое магнетроном микроволновой печи, заставляет молекулы воды, жира и некоторых других веществ двигаться быстрее, в результате чего еда нагревается. Молекулы жира легко заставить двигаться благодаря их низкой теплоемкости, и поэтому жирная еда нагревается до более высоких температур, чем еда, содержащая много воды. Достигнутая температура может быть настолько высока, что ее достаточно для реакции Майяра. Продукты с высоким содержанием воды не достигают таких температур из-за высокой теплоемкости воды, поэтому и реакция Майяра в них не протекает.
Высокие температуры, которых достигает жир в микроволновой печи, позволяют получить жареную корочку у некоторых продуктов, например бекона, но эти температуры могут представлять опасность при использовании микроволновых печей, особенно если не следовать правилам пользования печью, описанными в инструкции по эксплуатации. Например, когда в печи разогревают или готовят блюда из жирных продуктов, то не следует использовать пластмассовую посуду, так как даже посуда для микроволновых печей не рассчитана на температуры, которых достигает жир. Также следует не забывать, что жирная еда очень горяча, и есть ее осторожно, чтобы не обжечься.
Удельная теплоемкость материалов, используемых в быту
| Материал | Удельная теплоемкость, Дж/кг•K |
|---|---|
| Гелий | 5 193 |
| Вода | 4 181 |
| Алюминий | 897 |
| Бетон | 850 |
| Стекло | 840 |
| Алмаз | 509 |
| Латунь | 380 |
| Золото | 129 |
Литература
Автор статьи: Kateryna Yuri
Вы затрудняетесь в переводе единицы измерения с одного языка на другой? Коллеги готовы вам помочь. Опубликуйте вопрос в TCTerms и в течение нескольких минут вы получите ответ.
(PDF) Зависимость изобарной удельной теплоемкости водяного пара от давления и температуры
В 1995 году Международная ассоциация свойств воды и пара IAPWS приняла новую формулировку под названием «Формула IAPWS 1995 для термодинамики». природные свойства обычного водного вещества для общего и научного использования », который мы сокращаем до IAPWS-95 или IAPWS-95 для краткости. Эта формула IAPWS-95 заменяет предыдущую формулировку, принятую в 1984 году.Эта работа предоставляет информацию о выбранных экспериментальных данных термодинамических свойств воды, использованной для разработки новой рецептуры, но также предоставляется информация о более новых данных. В статье представлены все детали формулировки IAPWS-95, которая имеет форму фундаментального уравнения, явного для свободной энергии Гельмгольца. Функция остаточной части свободной энергии Гельмгольца была подогнана к выбранным данным для следующих свойств: тепловые свойства однофазной области (pT) и границы раздела фаз пар-жидкость (p T), включая условие равновесия; критерий Максвелла; b — теплотворные свойства, удельная изохорная теплоемкость, удельная изобарная теплоемкость, скорость звука, различия в удельной энтальпии и удельной внутренней энергии, коэффициент Джоуля – Томсона и коэффициент изотермического дросселирования.Применяя современные стратегии для оптимизации функциональной формы уравнения состояния и для одновременного нелинейного подгонки к данным всех упомянутых свойств, полученная формула IAPWS-95 покрывает допустимый диапазон температур от самой низкой температуры линии плавления 251,2 К. при 209,9 МПа до 1273 К и давлении до 1000 МПа. Во всем этом диапазоне достоверности IAPWS-95 представляет даже самые точные данные с точностью до экспериментальной неопределенности. В наиболее важной части жидкой области оценочная неопределенность IAPWS-95 колеблется от 0.От 001% до 0,02% по плотности, от 0,03% до 0,2% по скорости звука и 0,1% по изобарной теплоемкости. В жидкой среде при атмосферном давлении IAPWS-95 чрезвычайно точен по погрешности плотности 0,0001% и скорости звука 0,005%. На большей части газовой области оценочная погрешность по плотности колеблется от 0,03% до 0,05%, по скорости звука она составляет 0,15%, а по изобарной теплоемкости — 0,2%. В критической области IAPWS-95 очень хорошо отображает не только тепловые свойства, но и теплотворные свойства разумным образом.Особый интерес был сосредоточен на экстраполяционном поведении новой формулировки. По крайней мере, для основных свойств, таких как давление и энтальпия, IAPWS-95 можно экстраполировать до чрезвычайно высоких давлений и температур. В дополнение к формулировке IAPWS-95, приведены независимые уравнения для давления пара, плотности и наиболее важных теплотворных свойств вдоль границы пар-жидкость, а также для давления на кривой плавления и сублимации. Кроме того, также включено так называемое газовое уравнение для плотностей до 55 кг м 3.Таблицы термодинамических свойств, рассчитанных по формуле IAPWS-95, приведены в Приложении. © 2002 Американский институт физики.
Улучшение и максимум измерений изобарной удельной теплоемкости глубоко переохлажденной воды с помощью сверхбыстрой калориметрии
Значение
Важность молекулярного понимания структуры, динамики. и свойства жидкой воды признаны во многих научных дисциплинах. Здесь мы экспериментально изучаем структуру и термодинамику объемной жидкой воды при ее переохлаждении за счет испарения до ~ 228 К.Уникальным аспектом этой работы является использование сверхбыстрой калориметрии, позволяющей определять удельную теплоемкость воды при беспрецедентно низких температурах. Наблюдаемый максимум около 218 Дж / моль / К при 229 К согласуется с моделью критической точки жидкость – жидкость и поддерживает предложенный переход от хрупкого к сильному при ∼220 К, чтобы объяснить резкое уменьшение оцененного коэффициента самодиффузии. ниже 235 K.
Abstract
Знание температурной зависимости изобарической теплоемкости (C p ) при глубоком переохлаждении может дать представление об аномальных свойствах воды.Если максимум в C p существует при определенной температуре, например, при изотермической сжимаемости, это дополнительно подтвердит модель критической точки жидкость-жидкость, которая может объяснить аномальное увеличение термодинамических функций отклика. Проблема заключается в том, что соответствующий температурный диапазон попадает в область, где кристаллизация льда становится быстрой, что ранее исключало эксперименты. Здесь мы использовали методологию сверхбыстрой калориметрии, определяя скачок температуры от фемтосекундных рентгеновских импульсов после нагрева инфракрасным лазерным импульсом и с достаточно большой временной задержкой между импульсами, чтобы можно было проводить измерения при постоянном давлении.Испарительное охлаждение капель диаметром ∼15 мкм в вакууме позволило достичь температуры до ∼228 K, при этом небольшая часть капель осталась незамерзшей. Мы наблюдали резкое увеличение C p с 88 Дж / моль / К при 244 К до примерно 218 Дж / моль / К при 229 К, где виден максимум. Максимум C p находится при той же температуре, что и максимумы изотермической сжимаемости и корреляционной длины. Из измерения C p мы оценили избыточную энтропию и коэффициент самодиффузии воды, и эти свойства быстро уменьшаются ниже 235 К.
Вода — одна из самых исключительных жидкостей из-за ее важности, обилия и многих свойств, аномальных по сравнению с нормальной жидкостью (1⇓ – 3). Это аномальное поведение проявляется уже в условиях окружающей среды и усиливается, когда вода переохлаждена ниже точки замерзания в метастабильный режим (2, 4, 5). В частности, наблюдение, что изотермическая сжимаемость (κ T ), теплоемкость (C p ), коэффициент теплового расширения (α P ) и корреляционная длина (ξ), по-видимому, расходятся в сторону сингулярной температуры (T s ) около 228 К при давлении 1 бар, как оценивается по степенному закону (6, 7), привела к нескольким гипотезам о происхождении аномальных свойств воды (2, 3, 8).Одна из гипотез предполагает существование перехода жидкость – жидкость в переохлажденной воде между жидкостями с высокой плотностью (ЛПВП) и с низкой плотностью (ЛПНП), разделенными линией сосуществования фаз (8, 9) и заканчивающейся жидкостью — жидкая критическая точка (LLCP) при положительном давлении (8). За пределами LLCP при более низких давлениях для воды характерны колебания между локальными структурами ЛПВП и ЛПНП (10). Геометрическое место максимума ξ этих флуктуаций определяет линию Уидома на фазовой диаграмме давление – температура, которая исходит от LLCP как продолжение линии сосуществования фаз (11).Вблизи линии ξ Видома другие функции термодинамического отклика также могут иметь максимумы, определяющие линии Видома κ T и C p , сливающиеся с линией ξ Видома в непосредственной близости от критической точки. Такое слияние наблюдалось для максимумов в κ T и C p , а также для минимума в α P в критической точке жидкость-газ (LGCP) на основе молекулярно-динамического (МД) моделирования (12 ).
Было сложно экспериментально определить существование линии Уидома в переохлажденной воде из-за чрезвычайно быстрой кристаллизации с образованием льда при температурах ниже 235 К.Тем не менее быстрое испарительное охлаждение капель микрометровых размеров с последующим сверхбыстрым опросом рентгеновским лазером позволило нам зондировать воду при температурах до 227 К (13, 14). Недавно при использовании этого подхода максимумы ξ и κ T наблюдались при 229 K, что совпадает с температурой наиболее быстрого изменения локальной тетраэдрической структуры в жидкости (13). Другие эксперименты с использованием скорости звука в растянутой жидкой воде (15) также предсказывают максимумы κ T и C p .На основе комбинации МД-моделирования и измерений структурного фактора, зависящего от температуры, была получена согласованность, при которой α P также может иметь минимум при 229 K (16). Если бы все термодинамические функции отклика показали наличие линии Уидома с максимумами или минимумами, это подтвердило бы сценарий LLCP, тем более, если бы они находились в непосредственной близости по температуре. В настоящее время не существует измерений ниже 236 К (17) для C p , и необходимо разработать экспериментальные методы исследования воды при глубоком переохлаждении, когда происходит быстрая кристаллизация льда.Измерения значения максимума C p также позволяют нам определить, в какой степени избыточная энтропия уменьшилась при переохлаждении, и сравнить это с энтропией аморфного льда низкой плотности (LDA) при температуре стеклования (18⇓– 20). Интерес к избыточной энтропии был одним из первых мотивов исследования переохлажденной воды в 1969 г. (18). Исходя из предположения, что C p должен уменьшаться при охлаждении, избыточная энтропия должна была быстро уменьшаться, поскольку C p приближается к LDA.Однако удивительно, но вместо этого наблюдалось ускоренное увеличение (21⇓ – 23).
Здесь мы показываем, что C p может быть измерен до 228 K с использованием метода, основанного на сверхбыстрой калориметрии. Данные согласуются с существованием максимума C p при 229 K, а также с быстрым уменьшением избыточной энтропии при температурах за пределами линии Видома. На рис. 1 показана экспериментальная установка нашего метода сверхбыстрой калориметрии. Капли охлаждаются за счет испарения, а температура рассчитывается с использованием теории испарения Кнудсена и закона теплопроводности Фурье (24, 25).Этот подход к определению температуры капель оказался успешным в различных экспериментальных установках (13, 14, 26) и был подтвержден с помощью МЭ моделирования (25). Инфракрасный (ИК) импульс 2,05 мкм нагревает образец, повышая температуру капель на 0,5–1 К. Затем капли зондируются фемтосекундным рентгеновским импульсом после задержки в 1 мкс, позволяя жидкости расширяться. . Разница в диаграммах рассеяния рентгеновских лучей между включенным и выключенным ИК-лазером используется в качестве термометра. Образец каждого рентгеновского снимка также используется для определения того, появляются ли пики Брэгга из мелких кристаллов льда, чтобы кристаллизованные капли можно было исключить из анализа.Используя калибровочную кривую сигнала рассеяния в зависимости от температуры, мы оцениваем повышение температуры по импульсу нагрева и получаем теплоемкость при постоянном давлении, C p . Мы наблюдаем быстрое увеличение C p при температурах ниже 235 К с максимумом, появляющимся при 229 К, с последующим предполагаемым понижением в сторону более низких температур. Подъем и максимум C p согласуется с существованием линии Уидома для C p , как ранее наблюдалось для κ T и ξ (13).
Рис. 1.
( A ) Схема экспериментальной установки ( слева, ) и ( B ) с угловой интегральной интенсивностью рассеяния ( справа, ). Временная задержка (∆t) между ИК-лазером и рентгеновскими лучами составляет 1 мкс. ИК-лазер включается для каждого альтернативного рентгеновского импульса. Разница в профилях рассеяния импульсов включения и выключения лазера составляет ~ 2% от сигнала.
Результаты
Ключевая цель настоящего исследования — определить изменения в рассеянии рентгеновских лучей из-за нагрева, индуцированного инфракрасным излучением, и измерить, как величина этого изменения зависит от начальной температуры воды.Мы используем две стратегии для определения скачка температуры из-за лазерного нагрева.
Скачок температуры с использованием Q
1 Сдвиг пика.
Первый метод состоит в измерении положения переданного импульса (Q) первого пика рассеяния жидкой воды при интенсивности рассеяния I (Q), расположенной на ∼2 Å −1 (Q 1 ), как показано на Рис. 1. Положение Q 1 как функция температуры и изменения из-за теплового импульса показано на рис. 2.Мы используем следующее выражение для определения скачка температуры: ΔTQ1 = ΔQ1 (dQ1 / dT) OFF. [1] Производная (dQ 1 / dT) OFF вычисляется с использованием метода центральной разности, где наиболее близкие значения выше и ниже используются температуры ( SI Приложение , уравнение S1 ). Производная (dQ 1 / dT) OFF увеличивается при переохлаждении до достижения максимума при 229,4 К. ∆Q 1 увеличивается медленнее, чем (dQ 1 / dT) OFF при переохлаждении, что приводит к ∆T Q1 уменьшаться при переохлаждении.
Рис. 2.
Положение первого пика (Q 1 ) на диаграмме рассеяния рентгеновских лучей жидкой воды I (Q) для измерений в нагретом (ИК-лазер включен, крестики) и без нагрева (ИК-лазер выключен, темные кружки). Три набора представляют три различных условия пространственного перекрытия между рентгеновским и ИК-лазером.
Скачок температуры в зоне действия сигнала обогрева.
Второй метод, используемый для определения изменения температуры, основан на площади под абсолютным значением сигнала нагрева ∣I ON –I OFF , как показано на рис.3 А . Профиль интенсивности рассеяния рентгеновских лучей усредняется отдельно для выстрелов выключенного и включенного лазера. Интенсивность рассеяния для двух профилей может отличаться из-за чувствительности сигнала к рассеивающему объему, которая может быть непостоянной для каждого выстрела в зависимости от того, попадают ли рентгеновские лучи в каплю по центру или не по центру. Таким образом, интенсивность рассеяния нормирована так, чтобы профили имели одинаковую площадь в области Q = 1,5–3,5 Å –1 . После этой нормализации строится разностный профиль интенсивности рассеяния [∆I (Q)] выстрелов ВКЛ – ВЫКЛ.Эта разница, ∆I (Q), затем сравнивается с dI (Q) / dT на основе импульсов выключения лазера (dI (Q) / dT) OFF ). Формы ∆I (Q) и (dI (Q) / dT) OFF аналогичны. (dI (Q) / dT) OFF рассчитывается между двумя последовательными температурами, за исключением самой холодной температуры 228,5 K, где она экстраполируется (см. SI Приложение , рис. S2) в соответствии со следующим уравнением : (dIdT) OFF (Ti + Ti + 1) / 2 = IOFF (Ti) −IOFF (Ti + 1) Ti − Ti + 1. [2] Площадь под абсолютным значением сигнала нагрева и ∣ (dI ( Q) / dT) OFF ∣ вычисляется в области Q = 1.5–2,8 Å −1 (заштрихованная область на рис. 3 A ), чтобы получить ∆T площадь согласно уравнению. 3. Этот диапазон Q выбран после анализа разложения по сингулярным значениям ( SI Приложение , раздел 2), который предполагает, что более 65% дисперсии сигнала в этом диапазоне Q связано с нагревом, а остальные 35% могут быть отнесены на счет к шуму.ΔTarea = ∑Q | ΔI (Q) | ∑Q | (dI (Q) / dT) OFF |. [3]
Рис. 3.
( A ) Сигнал нагрева (I ON –I OFF ) при выбранных температурах.( B ) Повышение температуры (∆T) как функция температуры для трех разных наборов данных. Два значения ∆T Q1 и ∆T области дают аналогичные результаты и показаны в приложении SI , рис. S3. Среднее значение ∆T Q1 и ∆T области используется для вычисления среднего значения ∆T и показано на рисунке 3 B . Три набора данных представляют разные условия выполнения пространственного перекрытия между рентгеновским и инфракрасным лазером, и, как результат, ∆T не согласуется между разными прогонами, но согласуется в каждой серии прогонов.Планки погрешностей — это SEM, рассчитанные согласно SI Приложение , раздел 7.
Пространственное перекрытие.
Для эксперимента требуется, чтобы три объекта, а именно импульс рентгеновского излучения, ИК-лазер и капли, находились в одном и том же месте (без учета движения капель во время задержки в 1 мкс между импульсами). Мы гарантируем, что капли и рентгеновские лучи совпадают, отслеживая сигнал рассеяния рентгеновских лучей на детекторе. Мы используем флуоресцентную бумагу на держателе образца, чтобы обеспечить пространственное перекрытие между ИК-лазером и (ослабленным) рентгеновским излучением.Мы обнаружили, что пространственное перекрытие нечувствительно на расстоянии 4 мм вдоль направления распространения рентгеновских лучей. Это находится в пределах джиттера цепочки капель ± 1 мм. Три набора данных на рис. 3 B имеют разные условия пространственного перекрытия между рентгеновскими лучами и ИК-лазером, как показано на рис. 4. Необходимо компенсировать эту разницу при объединении данных. C p , рассчитанный из набора данных 1 (234 K
Рис. 4.
Схема пространственного перекрытия между рентгеновским излучением (14 мкм × 14 мкм) и ИК-лазером [305 мкм (h) на 375 мкм (v)]. ( A ) Изображение представляет поток ИК-лазера (интенсивность в произвольных единицах, показанных цветной полосой), а коричневая точка представляет положение рентгеновских лучей. ИК-лазер настраивается так, чтобы он был концентрическим с рентгеновскими лучами каждые 12 часов. ( B ) Три пунктирных кружка схематично иллюстрируют условия пространственного перекрытия для наборов 1, 2 и 3, соответственно.Набор 3 представляет собой лучшее перекрытие между рентгеновским и ИК-лазером. Это согласуется с реальными изображениями камеры пространственного перекрытия.
Удельная теплоемкость.
Подробное описание расчета C p из ∆T доступно в Cp из ∆T. На рис.5 мы видим, что C p увеличивается почти в 3 раза по измеренным температурам, возрастая от 75 Дж / моль / К при комнатной температуре до примерно 218 ± 10 (SE, SEM) Дж / моль / К при 228,9 К. При дальнейшем охлаждении до 228.5 К наблюдается падение удельной теплоемкости до среднего значения 175 ± 14 (SEM) Дж / моль / К. Это уменьшение C p наблюдается для двух независимых измерений. Набор данных 3 имеет лучшее пространственное перекрытие и самые низкие температуры в текущем эксперименте. В этом наборе данных мы проверяем дрейф прибора во времени, возвращаясь к определенным температурам и повторяя измерения. Оба измерения при 228,9 К дают более высокое значение C p , чем два измерения при 228.5 К. Модель воды с двумя состояниями (28) показывает аналогичное значение при максимуме удельной теплоемкости воды, но максимум находится при ∼226 К. Максимум для наших данных составляет 229,2 ± 1 (SEM) K, так как усредненное из максимума C p из ∆T Q1 и ∆T области . Более раннее исследование (13) с использованием почти идентичной экспериментальной установки для измерения κ T воды показало максимум при 229,2 ± 1 (SEM) K. Эта температура, о которой сообщалось ранее, была основана на экстраполированной оценке C p ниже 236 K, поскольку вход в модель испарительного охлаждения Кнудсена.Это исследование дает значение C p , которое выше, чем предыдущие оценки, что приводит к пересмотренной температуре максимумов κ T и ξ (13), которая выше на 0,8 K. Мы также упоминаем здесь, что оценка C p — это итеративный процесс, поскольку первые оценки C p используются в качестве входных данных в модели испарения Кнудсена, которая впоследствии дает новые оценки T и C p до тех пор, пока самосогласованность не произойдет в пределах 0,05 K.
Рис.
Удельная теплоемкость воды, измеренная на основе трех различных наборов данных.Коричневая линия — это ориентир для глаз. Данные Энджелла взяты из исх. 17. и данные модели с двумя состояниями взяты из исх. 28. Планки погрешностей — это SEM, рассчитанные в соответствии с SI Приложение , раздел 7.
Важно установить, может ли небольшое количество нанокристаллического льда повлиять на наши измерения. Наш порог обнаружения нанокристаллического льда оказался равным 0,11% льда по массе ( SI Приложение , рис. S7), что аналогично предыдущей оценке 0.05% в исх. 14 с использованием аналогичной экспериментальной установки. Эта фракция нанокристаллического льда приведет к снижению C p на 0,20 Дж / моль / К. Это очень небольшое число по сравнению с тем, что мы наблюдаем в наших измерениях. По нашим оценкам, критический размер ледяных кластеров составляет 2,5 нм, и нанокристаллы, которые достигают этого размера, быстро вырастут до обнаруживаемого размера 210 нм ( SI Приложение , раздел 9) в течение 10 мкс на основе скорости роста кристаллического льда, измеренной Xu et al. al. (29), что намного быстрее, чем наши рентгеновские измерения на частоте 25 Гц.Картина рассеяния с 1% нанокристаллического льда (30) привела бы к большому сдвигу Q 1 до 1,78 Å -1 , который мы не наблюдаем. Эта оценка полностью согласуется с наблюдением, что только несколько кристаллов образуются, как видно из отдельных пятен Брэгга при обнаружении льда, что указывает на условия, ограниченные зародышеобразованием (14, 31). На основании этих наблюдений мы делаем вывод, что нанокристаллический лед не влияет на наши измерения.
Избыточная энтропия и динамические свойства.
Избыточная энтропия (S ex ), то есть дополнительная энтропия, присутствующая в жидкости по отношению к ее кристаллу при той же температуре, полезна для предсказания температур стеклования жидкостей (18, 19). Оценим S ex по избыточной удельной теплоемкости при постоянном давлении Cpex = Cp, liq − Cp, Ih из следующего уравнения (32): Sex (T) = Sex (TM) −∫TTMCPexTdT, для T
Рис. 6.
( A ) Избыточная энтропия для жидкой воды. Данные Энджелла взяты из исх. 19. ( B ) Коэффициент самодиффузии жидкой воды.Данные Энджелла оцениваются путем применения уравнения Адама – Гиббса 5 к данным из A . Данные о ценах взяты из исх. 38 и Xu данные взяты из исх. 29. Планки погрешностей основаны на минимальном и максимальном значении C p и рассчитаны в соответствии с SI Приложение , раздел 7.
Мы также можем связать C p и S ex переохлажденной воды с его динамические свойства и лучше понять предлагаемый переход от хрупкого к сильному (1, 11) в воде, где прогнозируется внезапное изменение коэффициента самодиффузии воды.Мы используем уравнение Адама – Гиббса (33) для расчета коэффициента самодиффузии (D s ) воды. Ds (T) = Ds0 × exp [AT × Sconf]. [5] S conf является конфигурационным энтропия, которая получается добавлением остаточной энтропии (S res ) к избыточной энтропии. Эта оценка конфигурационной энтропии предполагает, что колебательная энтропия (S виб ) равна таковой кристалла (S кристалл ). Это предположение не является строго верным (34), поскольку ландшафты свободной энергии жидкостей и кристаллов не идентичны.Однако он широко используется (32, 35), поскольку S vib пропорционален кристаллу S и параметрам подгонки (A, D S0 ) в уравнении. 5 учитывают эту пропорциональность (32). Остаточная энтропия обусловлена протонным беспорядком (36) и была оценена как S res = R ln (3/2) = 3,47 Дж / моль / К, где R — универсальная газовая постоянная, но экспериментально установлено, что она равна 3,54 Дж / моль / К (37). Константы A и D s0 были оценены путем аппроксимации экспериментальных данных для жидкой воды в интервале температур от 373 до 237 K Mallamace et al.(35) и оказались равными A = -31,75 кДж / моль и D s0 = 1,07 × 10 -7 м 2 / с. На рис. 6 B показан коэффициент самодиффузии воды. Мы сравниваем наши данные с данными, полученными в исх. (19) из эмульгированной переохлажденной воды. Более поздние эксперименты по импульсному лазерному нагреву монослоев льда (29) и импульсному градиентному спин-эхо ЯМР на воде в капилляре (38) также показаны на рис. 6 B .
Обсуждение
Мы обнаружили, что существует максимум по температуре для изобарической удельной теплоемкости жидкой воды, который находится при той же температуре, что и максимумы в (dQ 1 / dT) OFF или ∑Q = 1.52,8 | (dI (Q) / dT) OFF |, в зависимости от метода оценки скачка температуры. Ранее мы наблюдали экспериментальное определение максимумов изотермической сжимаемости, корреляционной длины и производной первого пика структурного фактора (dS 1 / dT) (13). Это наблюдение завершает концепцию линии Видома, согласно которой действительно наблюдаются максимумы всех функций отклика, что согласуется с существованием LLCP при положительном давлении (8).
Фиг.7 показано прямое сравнение термодинамических свойств вокруг линии Уидома с пересмотренной температурой для ранее изученных κ T , ξ и dS 1 / dT (13). Величина dS 1 / dT также изменяется из-за изменения температуры и пересмотрена на том же рисунке. Как видно на рис. 7, максимумы близки по температуре. Мы также рассчитали dS 1 / dT для нашего эксперимента ( SI Приложение , раздел 6), и его максимум по температуре составляет 229.4 ± 1 К по сравнению с 230,0 ± 1 К из предыдущих результатов (13). Это обнадеживает, поскольку два разных измерения с разными детекторами, рентгеновскими установками и процедуры анализа данных дают очень похожие результаты. Наша способность точно определить максимум ограничена расстоянием между нашими последовательными точками данных, которое составляет ∼0,5 К. Хотя есть ошибки ± 1 К в абсолютной температуре из модели испарения Кнудсена, относительные ошибки в температуре в пределах эксперимента ( 13) имеет порядок ± 0.1 К. Эта относительная погрешность в первую очередь связана с колебаниями вакуума и точностью положения образца (13). В настоящее время ведутся споры о точности измерения температуры капли в этой установке испарения капель воды микрометрового размера в вакууме (26, 39, 40). Наблюдения Гоя и др. (26) согласуются с нашими наблюдениями относительно достоверности модели испарения Кнудсена, но есть разногласия с их выводом о том, что степень переохлаждения переоценивается в Sellberg et al.(14). Этот аргумент основан на наблюдаемой фракции льда по скорости образования однородного льда и нечувствительности подгонки диаметра капли в зависимости от расстояния к скорости капли в Goy et al. исследование, как обсуждается в дополнительном материале исх. 41. Мы вычисляем C p для более низкой и высокой оценки температуры ( SI Приложение , рис. S6) и по-прежнему наблюдаем максимум в C p .
Рис. 7.
Сравнение сильно переохлажденной области κ T , ξ и dS 1 / dT (13) с текущим определенным C p .Обратите внимание, что температурная шкала настроена для κ T , ξ и dS 1 / dT относительно исх. 13, учитывая изменение температуры испарительного охлаждения из-за быстрого увеличения C p , наблюдаемого в текущих измерениях. Линии приведены по степенному закону к соответствующим свойствам. Разница в максимальных температурах между C p и другими свойствами находится в пределах погрешности.
Gallo et al. (12) показали, что есть разные линии максимумов в плоскости P-T κ T , C p и α P по мере приближения к LGCP.В частности, линии максимумов C p и α P близко следуют друг за другом, тогда как линия максимума κ T отклоняется незначительно. Эти линии сходятся только при 30 К и 90 бар выше LGCP. В режиме переохлаждения максимумы κ T и C p , показанные на рис. 7, разнесены только на ∼0,8 ± 1,4 SEM K, что означает, что мы можем быть близки к LLCP) воды. Предыдущие исследования сравнивали экспериментальные данные с различными моделями молекулярного моделирования для воды, обнаруживая LLCP реальной воды при 600–1000 бар (13, 16, 28, 41, 42).
Наблюдаемый резкий рост C p при T <235 K означает быстрое увеличение флуктуаций энтропии. Мы также видим быстрое изменение положения κ T и S 1 относительно температуры при T <235 K, что коррелирует с тетраэдрическостью (16). Имеем следующую связь между κ T и C p : Cp = Cv + TαP2ρκT, [6] где ρ — плотность жидкости. Переписав αP / κT как (δPδT) V, Cp = Cv + κTTρ × (δPδT) V2. [7] Известно, что постоянная объемная теплоемкость (C v ) имеет слабую температурную зависимость в переохлажденной области (19 ) и T, ρ и (δPδT) V2 являются конечными величинами, и поэтому рост C p должен вести себя аналогично κ T вблизи предполагаемого LLCP.Этот быстрый рост и максимум C p в метастабильной воде также наблюдается в модели воды с двумя состояниями (28), когда она соответствует измеренному κ T в пределах «ничейной земли». Хотя максимум, наблюдаемый в этой модели, находится при более низкой температуре ∼226 K, сдвиг относительно κ T находится в том же направлении, что и мы.
Избыточная энтропия переохлажденной воды быстро уменьшается при переохлаждении ниже 235 К, как показано на рис. 6 A . Это быстрое уменьшение, экстраполированное на более низкие температуры, привело бы к теоретической температуре стеклования (температуре Каузмана) T ∼ 190 K.Однако было определено, что температура стеклования LDA составляет около 136 К (20) для обычной экспериментальной скорости нагрева 0,5 К / с, а при более высоких температурах была измерена поступательная диффузия сверхвязкой жидкости (29, 43). Следовательно, ожидается, что существует быстрое изменение наклона S ex по отношению к температуре ниже 227 K, указывающее на переход от хрупкого к сильному (1, 11, 44, 45). Недавние исследования (46) были проведены для понимания этого перехода в пересмотренной в 2005 г. версии переносимого потенциала взаимодействия с четырьмя точками (TIP4P / 2005) модели воды, и было предложено, что переход происходит при 220 К и связан с изменением окружающая среда воды с локальной плотностью от фазы, богатой ЛПВП, до фазы, богатой ЛПНП.Такая гипотеза согласуется с наблюдением, что жидкость быстро претерпевает структурные изменения на линии Уидома, в которых преобладают тетраэдрические структуры, как это наблюдается в данных по рассеянию рентгеновских лучей (13, 14). Однако, хотя модель TIP4P / 2005 имеет некоторые качественные особенности, напоминающие аномалии воды, значения максимумов в C p (47), а также κ T , ξ и dS 1 / dT (16 ) на линии Widom в значительной степени недооценены. Следовательно, оценка перехода от хрупкого к сильному с использованием модели TIP4P / 2005 будет далека от количественной, и необходимы дальнейшие эксперименты.
Полученный коэффициент диффузии согласуется с результатами других экспериментов, как показано на рис. 6 B . Данные Xu et al. (29) не использовали объемную воду, а, скорее, 25-монослойный слой аморфной твердой воды, который был нагрет до жидкого состояния с помощью наносекундного оптического лазера, в результате чего толщина воды составила 8 нм. Эта толщина всего в 4 раза больше среднего масштаба длины 2 нм флуктуации при 230 К, измеренной с помощью малоуглового рассеяния рентгеновских лучей (13), и, следовательно, ограничение может гасить флуктуации, что может несколько влиять на диффузионные свойства.Наши оценки D s при 229 K составляют 9,5 × 10 −12 — 2,0 × 10 −11 м 2 / с по сравнению с измерениями Сюя 2,4–4,1 × 10 −11 м 2 / с при тех же температурах. Потребуется провести более точные измерения коэффициента диффузии воды при глубоком переохлаждении, которые можно было бы получить с помощью рентгеновской фотонной корреляционной спектроскопии (43).
Выводы
Мы продемонстрировали метод проведения сверхбыстрой калориметрии, основанный на использовании ИК-накачки в качестве источника нагрева и рентгеновского лазера в качестве датчика температуры.Временная задержка между импульсами учитывает тепловое расширение и, таким образом, обеспечивает измерения теплоемкости при постоянном давлении (C p ). Поскольку мы использовали довольно небольшие скачки температуры (<1 K), C p можно оценить с точностью до 10% относительной ошибки и ± 1 K. Однако сигнал изменения рассеяния рентгеновских лучей невелик, что влияет на общее качество измерения. данные, так что каждая отдельная серия прогонов зависит от конкретного пространственного перекрытия импульсов накачки и зонда, что делает необходимым комбинировать разные прогоны вместе.Хотя точность ниже, чем при измерениях изотермической сжимаемости (κ T ), корреляционной длины (ξ) и производной структурного фактора (dS 1 / dT), все наблюдая максимумы при температуре 230 K, мы пришли к выводу, что текущие данные согласуются с C p , имеющим максимум при 229,2 ± 1 К. Поскольку разница температур между максимумами κ T и C p мала, это указывает на то, что критическая точка в температуре — Фазовая диаграмма давления может быть близка к нашим условиям измерения.
Поскольку максимум C p имеет большое значение, он будет влиять на наклон температурной зависимости избыточной энтропии в сторону более низких температур. Чтобы подключиться к стеклованию при ∼136 К, необходимо быстрое изменение наклона избыточной энтропии где-то ниже 227 К, поддерживая предложенный переход от хрупкого к сильному при несколько более низких температурах. Используя уравнение Адама – Гиббса и приближения, касающиеся конфигурационной энтропии, мы показываем, что коэффициент самодиффузии быстро уменьшается при охлаждении жидкости ниже 235 К, что дополнительно способствует динамическому переходу при температуре около 220 К.
Материалы и методы
Мы используем воду Milli-Q для наших измерений. Мы используем сверхбыстрое рентгеновское излучение, обеспечиваемое каналом Bernina (48) в SwissFEL в Институте Пауля Шеррера (PSI), с энергией фотонов 9,55 кэВ с ∆E / E <5 × 10 −3 и частотой повторения 25 Гц и энергия импульса 350–450 мкДж / импульс. Размер фокуса рентгеновского излучения измеряется методом остроконечного сканирования и составляет 14 мкм на 14 мкм по полной ширине на полувысоте (FWHM). ИК-фемтосекундный лазер с длиной волны 2.05 мкм (полоса пропускания FWHM = 0,18 мкм) и размер (FWHM) 305 мкм ± 22 мкм (по горизонтали) на 375 мкм ± 21 мкм (по вертикали) и энергия 290 ± 5 мкДж (измеренная измерителем мощности) используется для возбуждения капельки. Длина волны намеренно выбрана немного дальше от пика поглощения (49) жидкой воды (1,94 мкм при 26 ° C) из-за относительной нечувствительности коэффициента поглощения к температуре (50, 51). Капли имеют диаметр 15 мкм со скоростью 16,6 м / с и исследуются рентгеновскими лучами в различных местах вакуумной камеры, которые соответствуют разным температурам.Между ИК-лазером и рентгеновскими лучами существует постоянная задержка в 1 мкс, и ИК-лазер отключается при каждом чередующемся рентгеновском импульсе. Предполагая, что C p = 82 Дж / моль / К и коэффициент поглощения 55 см -1 (на основе спектра поглощения воды при комнатной температуре и профиля лазера), ожидается, что лазер вызовет скачок T на ∼2,6 К, если капля находится в центре лазера (1 К, если капля находится на расстоянии 1 SD в обоих направлениях). Этот скачок T не зависит от размера капли (наш самый большой источник ошибок), потому что доля энергии, поглощаемой каплей, мала (см. C p из ∆T).Картина рассеяния регистрируется с помощью 16-M детектора Юнгфрау с диапазоном Q от 0,3 до 4,3 Å -1 . Интенсивность рентгеновского излучения измеряется с помощью детектора Юнгфрау 1,5 М. T прыжок и C p показаны в SI Приложение , Таблица S1.
C
p от ∆T.
C p рассчитывается путем деления поглощенной энергии (E abs ) каплей на массу капли (м) и скачок температуры (∆T). Cp = Eabsm × ∆T = Ei × [1 −exp (−α × deff)] ρ × π6 × d3 × ΔT = Eflux × π4 × d2 × [1 − exp (−α × d × 23)] ρ × π6 × d3 × ΔT [8]
где E i = энергия, падающая на каплю, E поток = падающий инфракрасный лазерный поток на каплю воды, d = диаметр капли, d eff = эффективная длина пути ИК-излучения через каплю = 2/3 * d и α = коэффициент поглощения воды.
Мы обнаружили, что для α × d≪1 эта оценка C p не зависит от размера капли. α для воды было найдено равным 55 см -1 при 26 ° C путем свертки спектра поглощения воды (49) с полосой пропускания лазера. Температурная зависимость коэффициента поглощения оценивалась на основании измерений Jensen et al. (50) в диапазоне 30–42 ° C и сворачивая его с полосой пропускания лазера. Их исследования показывают, что более холодная вода имеет более мягкие вариации коэффициента поглощения (низкий | dα / dT |).Мы используем значение из их самых холодных измерений при 30 ° C dα / dT = −0,182 см − 1K, что дает коэффициент поглощения, изменяющийся в узком диапазоне от 65 см −1 при 244 K до 68 см −1 при 228,5 К. Таким образом, изменение α оказывает незначительное влияние на оценку C p по ∆T.
Доступность данных.
Все данные исследования включены в статью и / или приложение SI . Некоторые данные исследования доступны по запросу.
Выражение признательности
Эта работа была поддержана передовым грантом Европейского исследовательского совета в рамках проекта 667205 и Шведским исследовательским советом в рамках грантов 2013-8823, 2017-05128 и 2019-05542.Исследования, приведшие к этим результатам, также получили финансирование от исследовательской и инновационной программы Horizon 2020 Европейского Союза в рамках Соглашения о гранте 730872, проекта CALIPSOplus и Фонда Йорана Густафссона в соответствии с соглашениями о грантах 1808, 1909 и 2044 гг. SwissFEL в рамках предложения p17743, финансируемого PSI, Швейцария. К.Х.К. и C.Y. были поддержаны грантом Национального исследовательского фонда Кореи, финансируемым правительством Кореи (Grant 2020R1A5A1019141).Мы благодарим Фрэнсиса Старра за ценные обсуждения и Фредерика Кавена за предоставление данных для модели с двумя состояниями.
Сноски
Вклад авторов: H.P., A.S., H.T.L., A.R.O., P.J.M.J., Y.D., S.Z., R.M., P.B. и A.N. спланированное исследование; H.P., A.S., N.E., J.A.S., K.H.K., F.P., K.A.-W., M.L.-P., J.K., T.J.L., C.Y., H.T.L., A.R.O., P.J.M.J., R.M., P.B. и A.N. проведенное исследование; H.P., N.E., J.A.S., K.H.K., F.P. и T.J.L. проанализированные данные; и H.P., A.S., и A.Н. написал статью.
Авторы заявляют об отсутствии конкурирующей заинтересованности.
Эта статья представляет собой прямое представление PNAS.
Эта статья содержит вспомогательную информацию в Интернете по адресу https://www.pnas.org/lookup/suppl/doi:10.1073/pnas.2018379118/-/DCSupplemental.
- Авторские права © 2021 Автор (ы). Опубликовано PNAS.
Этот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере. - Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт
не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к
остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Этот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере. - Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie
потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт
не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к
остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Удельная теплоемкость | Безграничная физика
Тепловая мощность
Теплоемкость измеряет количество тепла, необходимое для повышения температуры объекта или системы на один градус Цельсия.
Цели обучения
Объясните энтальпию в системе с постоянным объемом и давлением
Основные выводы
Ключевые моменты
- Теплоемкость — это измеримая физическая величина, которая характеризует количество тепла, необходимое для изменения температуры вещества на заданную величину. Он измеряется в джоулях на Кельвин и выражается в.
- Теплоемкость — это обширное свойство, которое зависит от размера системы.
- Теплоемкость большинства систем непостоянна (хотя ее часто можно рассматривать как таковую).Это зависит от температуры, давления и объема рассматриваемой системы.
Ключевые термины
- теплоемкость : количество тепловой энергии, необходимое для повышения температуры объекта или единицы материи на один градус Цельсия; в джоулях на кельвин (Дж / К).
- энтальпия : общее количество энергии в системе, включая внутреннюю энергию и энергию, необходимую для вытеснения окружающей среды
Тепловая мощность
Теплоемкость (обычно обозначается заглавной буквой C, часто с индексами) или теплоемкость — это измеримая физическая величина, которая характеризует количество тепла, необходимое для изменения температуры вещества на заданную величину.В единицах СИ теплоемкость выражается в джоулях на кельвин (Дж / К).
Теплоемкость объекта (обозначение C ) определяется как отношение количества тепловой энергии, переданной объекту, к результирующему увеличению температуры объекта.
[латекс] \ displaystyle {\ text {C} = \ frac {\ text {Q}} {\ Delta \ text {T}}.} [/ Latex]
Теплоемкость — это обширное свойство, поэтому она масштабируется в зависимости от размера системы. Образец, содержащий в два раза больше вещества, чем другой образец, требует передачи вдвое большего количества тепла (Q) для достижения такого же изменения температуры (ΔT).Например, если для нагрева блока железа требуется 1000 Дж, то для нагрева второго блока железа, масса которого в два раза больше массы первого, потребуется 2000 Дж.
Измерение теплоемкости
Тепловая мощность большинства систем непостоянна. Скорее, это зависит от переменных состояния исследуемой термодинамической системы. В частности, это зависит от самой температуры, а также от давления и объема системы, а также от способов изменения давлений и объемов при переходе системы от одной температуры к другой.Причина этого в том, что работа системы давления и объема повышает ее температуру с помощью механизма, отличного от нагрева, в то время как работа объема давления, выполняемая системой, поглощает тепло, не повышая температуру системы. (Температурная зависимость объясняет, почему определение калории — это формально энергия, необходимая для нагрева 1 г воды с 14,5 до 15,5 ° C, а не обычно на 1 ° C.)
Таким образом, можно выполнять различные измерения теплоемкости, чаще всего при постоянном давлении и постоянном объеме.Измеренные таким образом значения обычно имеют нижний индекс (соответственно p и V) для обозначения определения. Газы и жидкости обычно также измеряются при постоянном объеме. Измерения при постоянном давлении дают более высокие значения, чем измерения при постоянном объеме, потому что значения постоянного давления также включают тепловую энергию, которая используется для выполнения работы по расширению вещества против постоянного давления при повышении его температуры. Эта разница особенно заметна для газов, где значения при постоянном давлении обычно составляют от 30% до 66.На 7% больше, чем при постоянной громкости.
Термодинамические соотношения и определение теплоемкости
Внутренняя энергия замкнутой системы изменяется либо за счет добавления тепла в систему, либо за счет выполнения системой работы. Вспоминая первый закон термодинамики,
[латекс] \ text {dU} = \ delta \ text {Q} — \ delta \ text {W} [/ latex].
За работу в результате увеличения объема системы можем написать:
[латекс] \ text {dU} = \ delta \ text {Q} — \ text {PdV} [/ latex].
Если тепло добавляется при постоянном объеме, то второй член этого соотношения исчезает и легко получается
[латекс] \ displaystyle {\ left (\ frac {\ partial \ text {U}} {\ partial \ text {T}} \ right) _ {\ text {V}} = \ left (\ frac {\ partial \ text {Q}} {\ partial \ text {T}} \ right) _ {\ text {V}} = \ text {C} _ {\ text {V}}} [/ latex].
Это определяет теплоемкость при постоянном объеме , C V . Еще одна полезная величина — теплоемкость при постоянном давлении , C P .При энтальпии системы из
[латекс] \ text {H} = \ text {U} + \ text {PV} [/ latex],
наше уравнение для d U меняется на
[латекс] \ text {dH} = \ delta \ text {Q} + \ text {VdP} [/ latex],
и, следовательно, при постоянном давлении имеем
[латекс] (\ frac {\ partial \ text {H}} {\ partial \ text {T}}) _ {\ text {P}} = (\ frac {\ partial \ text {Q}} {\ partial \ text {T}}) _ {\ text {P}} = \ text {C} _ {\ text {P}} [/ latex].
Удельная теплоемкость
Удельная теплоемкость — это интенсивное свойство, которое описывает, сколько тепла необходимо добавить к определенному веществу, чтобы повысить его температуру.
Цели обучения
Обобщите количественную взаимосвязь между теплопередачей и изменением температуры
Основные выводы
Ключевые моменты
- В отличие от общей теплоемкости, удельная теплоемкость не зависит от массы или объема. Он описывает, сколько тепла необходимо добавить к единице массы данного вещества, чтобы повысить его температуру на один градус Цельсия. Единицы измерения удельной теплоемкости — Дж / (кг ° C) или эквивалентно Дж / (кг · K).
- Теплоемкость и удельная теплоемкость связаны соотношением C = см или c = C / м.
- Масса m, удельная теплоемкость c, изменение температуры ΔT и добавленное (или вычитаемое) тепло Q связаны уравнением: Q = mcΔT.
- Значения удельной теплоемкости зависят от свойств и фазы данного вещества. Поскольку их нелегко рассчитать, они измеряются эмпирическим путем и доступны для справки в таблицах.
Ключевые термины
- удельная теплоемкость : Количество тепла, которое должно быть добавлено (или удалено) из единицы массы вещества, чтобы изменить его температуру на один градус Цельсия.Это интенсивное свойство.
Удельная теплоемкость
Теплоемкость — это обширное свойство, которое описывает, сколько тепловой энергии требуется для повышения температуры данной системы. Однако было бы довольно неудобно измерять теплоемкость каждой единицы вещества. Нам нужно интенсивное свойство, которое зависит только от типа и фазы вещества и может быть применено к системам произвольного размера. Эта величина известна как удельная теплоемкость (или просто удельная теплоемкость), которая представляет собой теплоемкость на единицу массы материала.Эксперименты показывают, что передаваемое тепло зависит от трех факторов: (1) изменения температуры, (2) массы системы и (3) вещества и фазы вещества. Последние два фактора заключены в значении удельной теплоемкости.
Теплопередача и удельная теплоемкость : Тепло Q, передаваемое для изменения температуры, зависит от величины изменения температуры, массы системы, а также от вещества и фазы. (а) Количество переданного тепла прямо пропорционально изменению температуры.Чтобы удвоить изменение температуры массы m, вам нужно добавить в два раза больше тепла. (б) Количество передаваемого тепла также прямо пропорционально массе. Чтобы вызвать эквивалентное изменение температуры в удвоенной массе, вам нужно добавить в два раза больше тепла. (c) Количество передаваемого тепла зависит от вещества и его фазы. Если требуется количество тепла Q, чтобы вызвать изменение температуры ΔT в данной массе меди, потребуется в 10,8 раз больше тепла, чтобы вызвать эквивалентное изменение температуры в той же массе воды, при условии отсутствия фазовых изменений ни в одном из веществ.
Удельная теплоемкость : В этом уроке тепло связано с изменением температуры. Мы обсуждаем, как количество тепла, необходимое для изменения температуры, зависит от массы и вещества, и это соотношение представлено удельной теплоемкостью вещества C.
Зависимость от изменения температуры и массы легко понять. Поскольку (средняя) кинетическая энергия атома или молекулы пропорциональна абсолютной температуре, внутренняя энергия системы пропорциональна абсолютной температуре и количеству атомов или молекул.Поскольку переданное тепло равно изменению внутренней энергии, тепло пропорционально массе вещества и изменению температуры. Передаваемое тепло также зависит от вещества, так что, например, количество тепла, необходимое для повышения температуры, меньше для спирта, чем для воды. Для одного и того же вещества передаваемое тепло также зависит от фазы (газ, жидкость или твердое тело).
Количественная связь между теплопередачей и изменением температуры включает все три фактора:
[латекс] \ text {Q} = \ text {mc} \ Delta \ text {T} [/ latex],
где Q — символ теплопередачи, m — масса вещества, а ΔT — изменение температуры.Символ c обозначает удельную теплоемкость и зависит от материала и фазы.
Удельная теплоемкость — это количество тепла, необходимое для изменения температуры 1,00 кг массы на 1,00 ° C. Удельная теплоемкость c — это свойство вещества; его единица СИ — Дж / (кг⋅К) или Дж / (кг⋅К). Напомним, что изменение температуры (ΔT) одинаково в единицах кельвина и градусов Цельсия. Обратите внимание, что общая теплоемкость C — это просто произведение удельной теплоемкости c и массы вещества m, i.е.,
[латекс] \ text {C} = \ text {mc} [/ latex] или [латекс] \ text {c} = \ frac {\ text {C}} {\ text {m}} = \ frac {\ текст {C}} {\ rho \ text {V}} [/ latex],
где ϱ — плотность вещества, V — его объем.
Значения удельной теплоемкости обычно нужно искать в таблицах, потому что нет простого способа их вычислить. Вместо этого они измеряются эмпирически. Как правило, удельная теплоемкость также зависит от температуры. В таблице ниже приведены типичные значения теплоемкости для различных веществ.За исключением газов, температурная и объемная зависимость удельной теплоемкости большинства веществ слабая. Удельная теплоемкость воды в пять раз больше, чем у стекла, и в десять раз больше, чем у железа, что означает, что для повышения температуры воды на такое же количество тепла требуется в пять раз больше тепла, чем у стекла, и в десять раз больше тепла для повышения температуры. воды как для железа. Фактически, вода имеет одну из самых высоких удельной теплоемкости из всех материалов, что важно для поддержания жизни на Земле.
Удельная теплоемкость : Указана удельная теплоемкость различных веществ.Эти значения идентичны в единицах кал / (г⋅C) .3. cv при постоянном объеме и 20,0 ° C, если не указано иное, и среднем давлении 1,00 атм. В скобках указаны значения cp при постоянном давлении 1,00 атм.
Калориметрия
Калориметрия — это измерение теплоты химических реакций или физических изменений.
Цели обучения
Проанализировать взаимосвязь между газовой постоянной для получения идеального выхода газа и объемом
Основные выводы
Ключевые моменты
- Калориметр используется для измерения тепла, выделяемого (или поглощаемого) в результате физических изменений или химической реакции.Наука об измерении этих изменений известна как калориметрия.
- Для проведения калориметрии очень важно знать удельную теплоемкость измеряемых веществ.
- Калориметрию можно проводить при постоянном объеме или постоянном давлении. Тип выполняемого расчета зависит от условий эксперимента.
Ключевые термины
- калориметр постоянного давления : прибор, используемый для измерения тепла, выделяемого во время изменений, не связанных с изменениями давления.
- калориметр : Устройство для измерения тепла, выделяемого или поглощаемого в результате химической реакции, изменения фазы или какого-либо другого физического изменения.
- калориметр постоянного объема : прибор, используемый для измерения тепла, выделяемого во время изменений, не связанных с изменением объема.
Калориметрия
Обзор
Калориметрия — это наука об измерении теплоты химических реакций или физических изменений. Калориметрия выполняется калориметром.Простой калориметр состоит из термометра, прикрепленного к металлическому контейнеру с водой, подвешенному над камерой сгорания. Слово калориметрия происходит от латинского слова калор , что означает тепло. Шотландский врач и ученый Джозеф Блэк, который первым осознал разницу между теплом и температурой, считается основоположником калориметрии.
Калориметрия требует, чтобы нагреваемый материал имел известные тепловые свойства, то есть удельную теплоемкость.Классическое правило, признанное Клаузиусом и Кельвином, состоит в том, что давление, оказываемое калориметрическим материалом, полностью и быстро определяется исключительно его температурой и объемом; это правило применяется для изменений, не связанных с фазовым переходом, таких как таяние льда. Есть много материалов, которые не соответствуют этому правилу, и для них требуются более сложные уравнения, чем приведенные ниже.
Ледяной калориметр : первый в мире ледяной калориметр, использованный зимой 1782-83 гг. Антуаном Лавуазье и Пьером-Симоном Лапласом для определения тепла, выделяющегося при различных химических изменениях; расчеты, основанные на предыдущем открытии скрытой теплоты Джозефом Блэком.Эти эксперименты составляют основу термохимии.
Базовая калориметрия при постоянном значении
Калориметрия постоянного объема — это калориметрия, выполняемая при постоянном объеме. Это предполагает использование калориметра постоянного объема (один из типов называется калориметром бомбы). Для калориметрии постоянного объема:
[латекс] \ delta \ text {Q} = \ text {C} _ {\ text {V}} \ Delta \ text {T} = \ text {mc} _ {\ text {V}} \ Delta \ text {T} [/ латекс]
, где δQ — приращение тепла, полученного образцом, C V — теплоемкость при постоянном объеме, c v — удельная теплоемкость при постоянном объеме, а ΔT — изменение температуры.
Измерение изменения энтальпии
Чтобы найти изменение энтальпии на массу (или на моль) вещества A в реакции между двумя веществами A и B, эти вещества добавляют в калориметр и определяют начальную и конечную температуры (до начала реакции и после ее завершения. ) отмечены. Умножение изменения температуры на массу и удельную теплоемкость веществ дает значение энергии, выделяемой или поглощаемой во время реакции:
[латекс] \ delta \ text {Q} = \ Delta \ text {T} (\ text {m} _ {\ text {A}} \ text {c} _ {\ text {A}} + \ text { m} _ {\ text {B}} \ text {c} _ {\ text {B}}) [/ latex]
Разделение изменения энергии на количество присутствующих граммов (или молей) A дает изменение энтальпии реакции.Этот метод используется в основном в академическом обучении, поскольку он описывает теорию калориметрии. Он не учитывает потери тепла через контейнер или теплоемкость термометра и самого контейнера. Кроме того, объект, помещенный внутри калориметра, показывает, что объекты передают свое тепло калориметру и жидкости, а тепло, поглощаемое калориметром и жидкостью, равно теплу, отдаваемому металлами.
Калориметрия постоянного давления
Калориметр постоянного давления измеряет изменение энтальпии реакции, протекающей в растворе, в течение которой атмосферное давление остается постоянным.Примером может служить калориметр кофейной чашки, который состоит из двух вложенных друг в друга чашек из пенополистирола и крышки с двумя отверстиями, в которую можно вставить термометр и стержень для перемешивания. Внутренняя чашка содержит известное количество растворенного вещества, обычно воды, которое поглощает тепло от реакции. Когда происходит реакция, внешняя чашка обеспечивает изоляцию. Тогда
[латекс] \ text {C} _ {\ text {P}} = \ frac {\ text {W} \ Delta \ text {H}} {\ text {M} \ Delta \ text {T}} [/ латекс]
, где C p — удельная теплоемкость при постоянном давлении, ΔH — энтальпия раствора, ΔT — изменение температуры, W — масса растворенного вещества, а M — молекулярная масса растворенного вещества.Измерение тепла с помощью простого калориметра, такого как калориметр для кофейной чашки, является примером калориметрии постоянного давления, поскольку давление (атмосферное давление) остается постоянным во время процесса. Калориметрия постоянного давления используется для определения изменений энтальпии, происходящих в растворе. В этих условиях изменение энтальпии равно теплоте (Q = ΔH).
Удельная теплоемкость идеального газа при постоянном давлении и объеме
Идеальный газ имеет различную удельную теплоемкость при постоянном объеме или постоянном давлении.
Цели обучения
Объясните, как рассчитать индекс адиабаты
Основные выводы
Ключевые моменты
- Удельная теплоемкость газа при постоянном объеме задается как [латекс] (\ frac {\ partial \ text {U}} {\ partial \ text {T}}) _ {\ text {V}} = \ text {c} _ {\ text {v}} [/ latex].
- Удельная теплоемкость при постоянном давлении для идеального газа задается как [латекс] (\ frac {\ partial \ text {H}} {\ partial \ text {T}}) _ {\ text {V}} = \ text {c} _ {\ text {p}} = \ text {c} _ {\ text {v}} + \ text {R} [/ latex].
- Коэффициент теплоемкости (или индекс адиабаты) — это отношение теплоемкости при постоянном давлении к теплоемкости при постоянном объеме.
Ключевые термины
- Фундаментальное термодинамическое соотношение : В термодинамике фундаментальное термодинамическое соотношение выражает бесконечно малое изменение внутренней энергии в терминах бесконечно малых изменений энтропии и объема для замкнутой системы, находящейся в тепловом равновесии, следующим образом: dU = TdS-PdV. Здесь U — внутренняя энергия, T — абсолютная температура, S — энтропия, P — давление, V — объем.
- Индекс адиабаты : Отношение теплоемкости при постоянном давлении к теплоемкости при постоянном объеме.
- удельная теплоемкость : Отношение количества тепла, необходимого для повышения температуры единицы массы вещества на единицу градуса, к количеству тепла, необходимому для повышения температуры той же массы воды на такое же количество.
Удельная теплоемкость идеального газа при постоянном давлении и объеме
Теплоемкость при постоянном объеме nR = 1 Дж · К −1 любого газа, включая идеальный, равна:
[латекс] (\ frac {\ partial \ text {U}} {\ partial \ text {T}}) _ {\ text {V}} = \ text {c} _ {\ text {v}} [/ латекс]
Это безразмерная теплоемкость при постоянном объеме; обычно это функция температуры из-за межмолекулярных сил.При умеренных температурах постоянная для одноатомного газа c v = 3/2, а для двухатомного газа c v = 5/2 (см.). Макроскопические измерения теплоемкости дают информацию о микроскопической структуре молекул.
Молекулярные внутренние колебания : Когда газ нагревается, поступательная киентная энергия молекул в газе увеличивается. Кроме того, молекулы газа могут улавливать множество характерных внутренних колебаний. Потенциальная энергия, хранящаяся в этих внутренних степенях свободы, вносит вклад в удельную теплоемкость газа.
Теплоемкость идеального газа при постоянном давлении 1 Дж · К −1 составляет:
[латекс] (\ frac {\ partial \ text {H}} {\ partial \ text {T}}) _ {\ text {V}} = \ text {c} _ {\ text {p}} = \ текст {c} _ {\ text {v}} + \ text {R} [/ latex]
где H = U + pV — энтальпия газа.
Измерение теплоемкости при постоянном объеме может быть чрезвычайно трудным для жидкостей и твердых тел. То есть небольшие изменения температуры обычно требуют больших давлений для поддержания постоянного объема жидкости или твердого вещества (это означает, что содержащий сосуд должен быть почти жестким или, по крайней мере, очень прочным).Легче измерить теплоемкость при постоянном давлении (позволяющем материалу свободно расширяться или сжиматься) и определить теплоемкость при постоянном объеме, используя математические соотношения, выведенные из основных законов термодинамики.
Используя фундаментальную термодинамическую связь, мы можем показать:
[латекс] \ text {C} _ {\ text {p}} — \ text {C} _ {\ text {V}} = \ text {T} (\ frac {\ partial \ text {P}} { \ partial \ text {T}}) _ {\ text {V}, \ text {N}} (\ frac {\ partial \ text {V}} {\ partial \ text {T}}) _ {\ text { p}, \ text {N}} [/ latex]
, где частные производные взяты при постоянном объеме и постоянном количестве частиц, а также при постоянном давлении и постоянном количестве частиц, соответственно.
Коэффициент теплоемкости или показатель адиабаты — это отношение теплоемкости при постоянном давлении к теплоемкости при постоянном объеме. Иногда его также называют коэффициентом изоэнтропического расширения:
.
[латекс] \ gamma = \ frac {\ text {C} _ {\ text {P}}} {\ text {C} _ {\ text {V}}} = \ frac {\ text {c} _ { \ text {p}}} {\ text {c} _ {\ text {v}}} [/ latex]
Для идеального газа оценка приведенных выше частных производных в соответствии с уравнением состояния, где R — газовая постоянная для идеального газа, дает:
[латекс] \ text {pV} = \ text {RT} [/ латекс]
[латекс] \ text {C} _ {\ text {p}} — \ text {C} _ {\ text {V}} = \ text {T} (\ frac {\ partial \ text {P}} { \ partial \ text {T}}) _ {\ text {V}} (\ frac {\ partial \ text {V}} {\ partial \ text {T}}) _ {\ text {p}} [/ latex ]
[латекс] \ text {C} _ {\ text {p}} — \ text {C} _ {\ text {V}} = — \ text {T} (\ frac {\ partial \ text {P}} {\ partial \ text {V}}) _ {\ text {V}} (\ frac {\ partial \ text {V}} {\ partial \ text {T}}) _ {\ text {p}} ^ { 2} [/ латекс]
[латекс] \ text {P} = \ frac {\ text {RT}} {\ text {V}} \ text {n} \ to (\ frac {\ partial \ text {P}} {\ partial \ text {V}}) _ {\ text {T}} = \ frac {- \ text {RT}} {\ text {V} ^ {2}} = \ frac {- \ text {P}} {\ text { V}} [/ латекс]
[латекс] \ text {V} = \ frac {\ text {RT}} {\ text {P}} \ text {n} \ to (\ frac {\ partial \ text {V}} {\ partial \ text {T}}) ^ {2} _ {\ text {p}} = \ frac {\ text {R} ^ {2}} {\ text {P} ^ {2}} [/ latex]
заменяющий:
[латекс] — \ text {T} (\ frac {\ partial \ text {P}} {\ partial \ text {V}}) _ {\ text {V}} (\ frac {\ partial \ text {V }} {\ partial \ text {T}}) _ {\ text {p}} ^ {2} = — \ text {T} \ frac {- \ text {P}} {\ text {V}} \ frac {\ text {R} ^ {2}} {\ text {P} ^ {2}} = \ text {R} [/ latex]
Это уравнение сводится просто к тому, что известно как соотношение Майера:
Юлиус Роберт Майер : Юлиус Роберт фон Майер (25 ноября 1814 — 20 марта 1878), немецкий врач и физик, был одним из основоположников термодинамики.Он известен прежде всего тем, что в 1841 году сформулировал одно из первоначальных заявлений о сохранении энергии (или то, что сейчас известно как одна из первых версий первого закона термодинамики): «Энергия не может быть ни создана, ни уничтожена. В 1842 году Майер описал жизненно важный химический процесс, который теперь называют окислением, как основной источник энергии для любого живого существа. Его достижения не были замечены, и заслуга в открытии механического эквивалента тепла была приписана Джеймсу Джоулю в следующем году.фон Майер также предположил, что растения превращают свет в химическую энергию.
[латекс] \ text {C} _ {\ text {P}} — \ text {C} _ {\ text {V}} = \ text {R} [/ latex].
Это простое уравнение, связывающее теплоемкость при постоянной температуре и при постоянном давлении.
Решение задач калориметрии
Калориметрия используется для измерения количества тепла, выделяемого или потребляемого в химической реакции.
Цели обучения
Объясните, что калориметр бомбы используется для измерения тепла, выделяемого в реакции горения
Основные выводы
Ключевые моменты
- Калориметрия используется для измерения количества тепла, передаваемого веществу или от него.
- Калориметр — это устройство, используемое для измерения количества тепла, участвующего в химическом или физическом процессе.
- Это означает, что количество тепла, производимого или потребляемого в реакции, равно количеству тепла, поглощаемого или теряемого раствором.
Ключевые термины
- теплота реакции : изменение энтальпии в химической реакции; количество тепла, которое система отдает своему окружению, чтобы она могла вернуться к исходной температуре.
- горение : процесс, в котором два химических вещества объединяются для получения тепла.
Калориметры
предназначены для минимизации обмена энергией между исследуемой системой и ее окружением. Они варьируются от простых калориметров для кофейных чашек, используемых студентами начального курса химии, до сложных калориметров-бомб, используемых для определения энергетической ценности пищи.
Калориметрия используется для измерения количества тепла, передаваемого веществу или от него. Для этого происходит обмен тепла с калиброванным объектом (калориметром).Изменение температуры измерительной части калориметра преобразуется в количество тепла (поскольку предыдущая калибровка использовалась для определения его теплоемкости). Измерение теплопередачи с использованием этого подхода требует определения системы (вещества или веществ, подвергающихся химическому или физическому изменению) и ее окружения (других компонентов измерительного устройства, которые служат либо для обеспечения теплом системы, либо для поглощения тепла от система). Знание теплоемкости окружающей среды и тщательные измерения масс системы и окружающей среды, а также их температуры до и после процесса позволяют рассчитать передаваемое тепло, как описано в этом разделе.
Калориметр — это устройство, используемое для измерения количества тепла, участвующего в химическом или физическом процессе. Например, когда в растворе в калориметре происходит экзотермическая реакция, тепло, выделяемое в результате реакции, поглощается раствором, что увеличивает его температуру. Когда происходит эндотермическая реакция, необходимое тепло поглощается тепловой энергией раствора, что снижает его температуру. Затем изменение температуры, а также удельная теплоемкость и масса раствора можно использовать для расчета количества тепла, задействованного в любом случае.
Калориметры для кофейных чашек
Студенты-общехимики часто используют простые калориметры, изготовленные из полистирольных стаканчиков. Эти простые в использовании калориметры типа «кофейная чашка» обеспечивают больший теплообмен с окружающей средой и, следовательно, дают менее точные значения энергии.
Структура калориметра постоянного объема (или «бомбы»)
Калориметр бомбы : Это изображение типичной установки калориметра бомбы.
Калориметр другого типа, который работает с постоянным объемом, в просторечии известный как калориметр бомбы, используется для измерения энергии, производимой реакциями, которые дают большое количество тепла и газообразных продуктов, таких как реакции горения.(Термин «бомба» происходит из наблюдения, что эти реакции могут быть достаточно интенсивными, чтобы напоминать взрывы, которые могут повредить другие калориметры.) Этот тип калориметра состоит из прочного стального контейнера («бомба»), который содержит реагенты и сам является погружен в воду. Образец помещается в бомбу, которая затем заполняется кислородом под высоким давлением. Для воспламенения образца используется небольшая электрическая искра. Энергия, произведенная в результате реакции, улавливается стальной бомбой и окружающей водой.Повышение температуры измеряется и, наряду с известной теплоемкостью калориметра, используется для расчета энергии, производимой в результате реакции. Калориметры бомбы требуют калибровки для определения теплоемкости калориметра и обеспечения точных результатов. Калибровка выполняется с использованием реакции с известным q, например измеренного количества бензойной кислоты, воспламененного искрой от никелевой плавкой проволоки, которая взвешивается до и после реакции. Изменение температуры, вызванное известной реакцией, используется для определения теплоемкости калориметра.Калибровка обычно выполняется каждый раз перед использованием калориметра для сбора данных исследования.
Пример: идентификация металла путем измерения удельной теплоемкости
Кусок металла весом 59,7 г, погруженный в кипящую воду, был быстро перенесен в 60,0 мл воды при начальной температуре 22,0 ° C. Конечная температура составляет 28,5 ° C. Используйте эти данные, чтобы определить удельную теплоемкость металла. Используйте этот результат, чтобы идентифицировать металл.
Решение
Предполагая идеальную теплопередачу, тепло, выделяемое металлом, является отрицательной величиной тепла, поглощаемого водой, или:
[латекс] \ text {q} _ {\ text {metal}} = — \ text {q} _ {\ text {water}} [/ latex]
В развернутом виде это:
[латекс] \ text {c} _ {\ text {metal}} \ times \ text {m} _ {\ text {metal}} \ times \ left (\ text {T} _ {\ text {f, металл }} — \ text {T} _ {\ text {i, metal}} \ right) = \ text {c} _ {\ text {water}} \ times \ text {m} _ {\ text {water}} \ times \ left (\ text {T} _ {\ text {f, water}} — \ text {T} _ {\ text {i, water}} \ right) [/ latex]
Отметим, что, поскольку металл был погружен в кипящую воду, его начальная температура была 100.{\ text {o}} \ text {C} [/ latex]
Наша экспериментальная удельная теплоемкость наиболее близка к значению для меди (0,39 Дж / г ° C), поэтому мы идентифицируем металл как медь.
Теплоемкость — Веб-формулы
Краткое описание:
Теплоемкость определяется как:
d T : изменение температуры
d ‘ Q : тепло добавлено в систему
Теплоемкость (постоянный объем)
Для постоянного объема теплоемкость определяется как:
C v = d U / d T
Теплоемкость (постоянное давление)
Для постоянного давления теплоемкость определяется как:
C p = d ‘ Q / d T
Подробнее о теплоемкости:
The теплоемкость тела — это количество энергии, необходимое для изменения его температуры на 1 o C.Теплоемкость C системы — это отношение тепла, добавляемого к системе или отводимого из системы, к результирующему изменению температуры:
C = q / Δ T = δ q / dT [Дж / град]
Теплоемкость тела зависит от того, из какого вещества оно состоит, а также от массы различных веществ в теле. Удельная теплоемкость вещества — это количество энергии, необходимое для изменения температуры 1 кг вещества на 1 o C.
Это определение действительно только при отсутствии фазовых переходов.
Единицы удельной теплоемкости — джоуль
кг -1 или C -1 .
Новое состояние системы не определяется только T, необходимо указать или ограничить вторую переменную:
: теплоемкость при постоянном объеме
: теплоемкость при постоянном давлении
Тот факт, что δ q не функция состояния и зависит от пути, что отражается в зависимости теплоемкости на пути, cp ≠ cv
(Обратите внимание, что малый c используется для производного интенсивного количества на массу, на объем или на моль, по сравнению с заглавная C означает экстенсивное количество.Для системы, содержащей n моль, C p = nc p и C v = nc v , где c v и c p являются молярными значениями).
c v и c p можно измерить экспериментально
изобарный процесс: dH = δq = c p dT
изохорный процесс: dU = δq = c v dT
H и U можно рассчитать из c p и c v
c v VS c p
Если материалу позволяют расширяться при нагревании, как это влияет на его теплоемкость?
Так как U = U (V, T)
Дифференциация по T при постоянном P дает:
: работа расширения при постоянном P из-за повышения температуры на dT
: работа расширения по сравнению с внутренним силы сцепления из-за повышения температуры на dT
Расчет энтальпии по теплоемкости
Для P = constant и dH = c p dT интегрирование дает:
Пример (1)
Пусть найдем энтальпию меди при 500 К.
c p ≈ 24,4 Джмоль -1 K -1 для меди при 1 атм.
Из первого закона мы можем рассчитать только разность ΔH — нужна эталонная энтальпия при 1 атм, а 298 K называется энтальпией образования , h398. Для чистых элементов в их состояниях равновесия H 298 = 0.
Энтальпия веществ, отличных от чистых элементов, также может быть рассчитана.
Энтальпия соединения при 298 К = 9 · 1026 условная теплота образования 9 · 1027 вещества из элементов.
Пример (2)
Для окисления меди при 25 o C: Cu твердый + 1 / 2C 2 газ = CuO твердый
Реакция экзотермическая — тепло и / или произведены работы.
Пример (3)
Какова удельная теплоемкость воды?
Ответ: Удельная теплоемкость воды S вода = 4200 джоулей кг -1 o C -1 (приблизительно)
Пример (4) каковы два основных конкретных (или молярных) ) теплоемкости газов?
Ответ: Два основных принципа удельной (или молярной) теплоемкости газов:
Удельная (или молярная) теплоемкость при постоянном объеме, C v
Удельная (или молярная) теплоемкость при постоянном давлении, C р
3.6. Теплоемкость идеального газа
Цели обучения
К концу этого раздела вы сможете:
- Определите теплоемкость идеального газа для конкретного процесса
- Вычислить удельную теплоемкость идеального газа для изобарического или изохорного процесса
- Объясните разницу между теплоемкостью идеального газа и реального газа
- Оценить изменение удельной теплоемкости газа в диапазоне температур
Мы узнали об удельной теплоемкости и молярной теплоемкости ранее; однако мы не рассматривали процесс, в котором добавляется тепло.Мы делаем это в этом разделе. Сначала мы исследуем процесс, в котором система имеет постоянный объем, затем сравниваем его с системой с постоянным давлением и показываем, как связаны их удельные температуры.
Начнем с рисунка \ (\ PageIndex {1} \), на котором показаны два сосуда A и B , каждый из которых содержит 1 моль идеального газа одного и того же типа при температуре T и объеме . V . Единственное различие между двумя сосудами состоит в том, что поршень в верхней части A зафиксирован, тогда как поршень в верхней части B может свободно перемещаться против постоянного внешнего давления p .Теперь рассмотрим, что происходит, когда температура газа в каждом сосуде медленно повышается до \ (T + dT \) с добавлением тепла.
Рисунок \ (\ PageIndex {1} \): Два сосуда идентичны, за исключением того, что поршень наверху A зафиксирован, тогда как поршень на вершине B может свободно перемещаться против постоянного внешнего давления p.
Поскольку поршень сосуда A неподвижен, объем заключенного газа не изменяется. Следовательно, газ не работает, а у нас из первого закона
\ [dE_ {int} = dQ — dW = dQ.\]
Мы представляем тот факт, что теплообмен при постоянном объеме осуществляется записью
\ [dQ = C_VndT, \] где \ (C_V \) — молярная теплоемкость при постоянном объеме газа. Кроме того, поскольку \ (dE_ {int} = dQ \) для этого конкретного процесса,
\ [dE_ {int} = C_VndT. \ label {3.9} \]
Мы получили это уравнение, предполагая, что объем газа фиксирован. Однако внутренняя энергия — это функция состояния, которая зависит только от температуры идеального газа.Следовательно, \ (dE_ {int} = C_VndT \) дает изменение внутренней энергии идеального газа для любого процесса, включающего изменение температуры dT .
Когда газ в сосуде B нагревается, он расширяется относительно подвижного поршня и совершает работу \ (dW = pdV \). В этом случае тепло добавляется при постоянном давлении, и мы пишем \ [dQ = C_ {p} ndT, \], где \ (C_p \) — молярная теплоемкость при постоянном давлении газа. Кроме того, поскольку идеальный газ расширяется при постоянном давлении,
\ [d (pV) = d (RnT) \] становится \ [pdV = RndT.\]
Наконец, вставляя выражения для dQ и pdV в первый закон, получаем
\ [dE_ {int} = dQ — pdV = (C_ {p} n — Rn) dT. \]
Мы нашли \ (dE_ {int} \) как для изохорного, так и для изобарного процесса. Поскольку внутренняя энергия идеального газа зависит только от температуры, \ (dE_ {int} \) должно быть одинаковым для обоих процессов. Таким образом,
\ [C_ {V} ndT = (C_ {p} n — Rn) dT, \]
и
\ [C_p = C_V + R.\ label {eq50} \]
Вывод уравнения \ ref {eq50} был основан только на законе идеального газа. Следовательно, это соотношение приблизительно справедливо для всех разбавленных газов, будь то одноатомные, такие как He, двухатомные, такие как \ (O_2 \), или многоатомные, такие как \ (CO_2 \) или \ (NH_3 \).
В предыдущей главе мы обнаружили, что молярная теплоемкость идеального газа при постоянном объеме равна
.
\ [C_V = \ dfrac {d} {2} R, \]
, где d — число степеней свободы молекулы в системе.В таблице \ (\ PageIndex {1} \) показаны молярные теплоемкости некоторых разбавленных идеальных газов при комнатной температуре. Теплоемкость реальных газов несколько выше, чем предсказывается выражениями \ (C_V \) и \ (C_p \), приведенными в уравнении \ ref {eq50}. Это указывает на то, что колебательные движения в многоатомных молекулах значительны даже при комнатной температуре. Тем не менее, разница в молярных теплоемкостях \ (C_p — C_V \) очень близка к R даже для многоатомных газов.
| \ (C_p \) | \ (C_V \) | \ (C_p — C_V \) | ||
|---|---|---|---|---|
| Тип молекулы | Газ | (Дж / моль К) | (Дж / моль К) | (Дж / моль К) |
| Одноатомный | Идеал | \ (\ frac {5} {2} R = 20.79 \) | \ (\ frac {3} {2} R = 12,47 \) | \ (R = 8,31 \) |
| Двухатомный | Идеал | \ (\ frac {7} {2} R = 29,10 \) | \ (\ frac {5} {2} R = 20,79 \) | \ (R = 8,31 \) |
| Многоатомный | Идеал | \ (4R = 33,26 \) | \ (3R = 24,04 \) | \ (R = 8. |

 00
00 00
00 001139
001139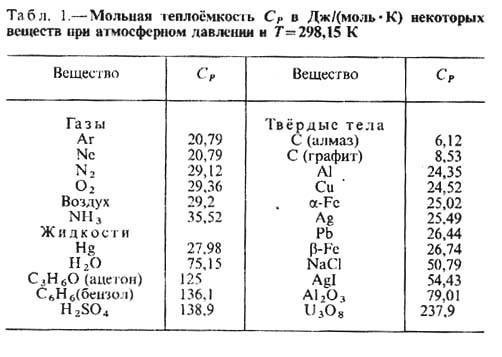 34
34 178
178 36
36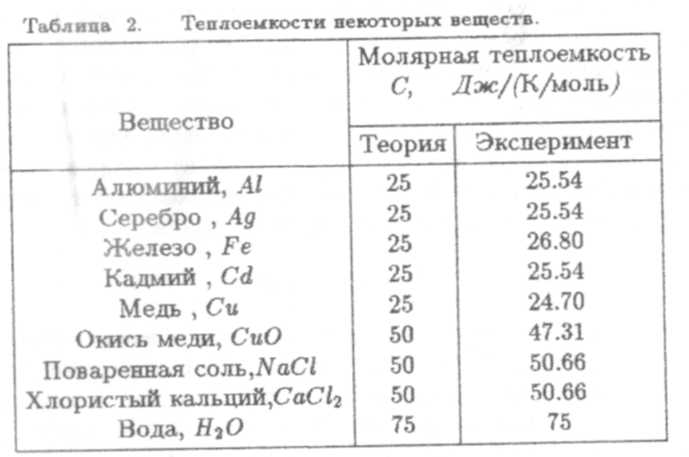 36
36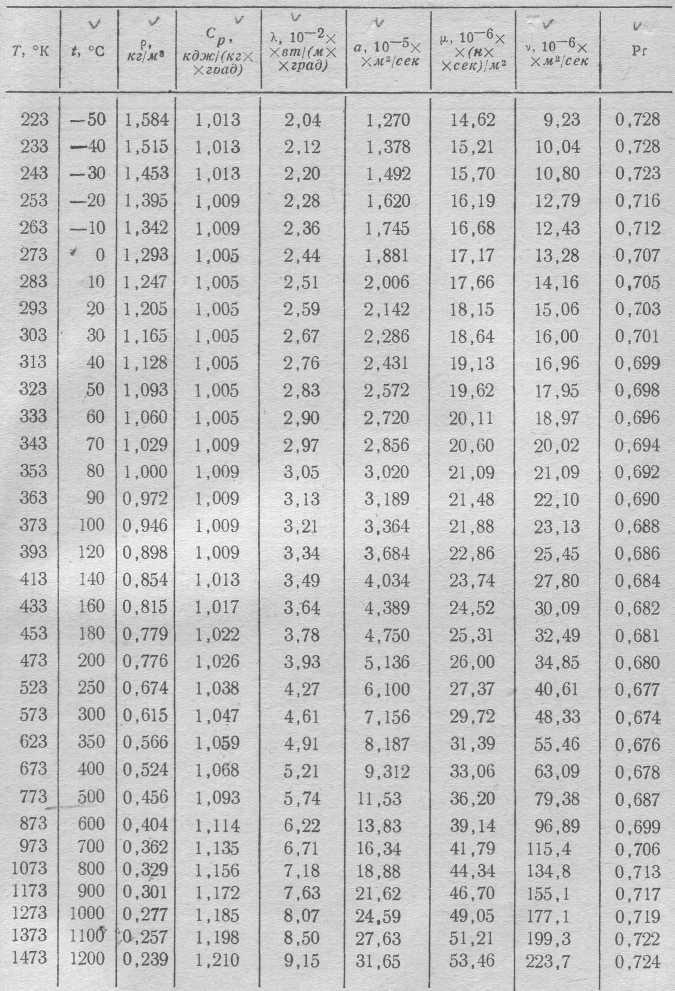 00
00 000453
000453 001
001 00
00 73
73 00
00
 Динамическая вязкость воды (=dynamic viscosity). Зависимость от температуры. Вариант для печати.
Динамическая вязкость воды (=dynamic viscosity). Зависимость от температуры. Вариант для печати. 70
70 51
51 29
29 998
998