Удельная теплоемкость — это… Что такое Удельная теплоемкость?
- Удельная теплоемкость
Уде́льная теплоёмкость (обозначается как c) вещества определяется как количество тепловой энергии, необходимой для повышения температуры одного килограмма вещества на один кельвин.
Единицей СИ для удельной теплоёмкости является Джоуль на килограмм-Кельвин ().
Следовательно, удельную теплоёмкость можно рассматривать как теплоёмкость единицы массы вещества. На значение удельной теплоёмкости влияет температура вещества. К примеру, измерение удельной теплоёмкости воды даст разные результаты при 20 °C и 60 °C.
Формула расчёта удельной теплоёмкости: , где — удельная теплоёмкость, — количество теплоты, полученное веществом при нагреве (или выделившееся при охлаждении), — масса нагреваемого (охлаждающегося) вещества, — разность температур, на которую нагрели вещество.
Значения удельной теплоёмкости некоторых веществ
Таблица I: Стандартные значения удельной теплоёмкости Элемент Агрегатное состояние Удельная
теплоёмкость
кДж·кг-1·K-1воздух (сухой) газ 1,005 воздух (100 % влажность) газ ≈ 1,030 алюминий твёрдое тело 0,930 бериллий твёрдое тело 1,824 латунь твёрдое тело 0,377 медь твёрдое тело 0,385 алмаз твёрдое тело 0,502 этанол жидкость 2,460 золото твёрдое тело 0,129 графит твёрдое тело 0,720 гелий газ 5,190 водород газ 14,300 железо твёрдое тело 0,444 литий твёрдое тело 3,582 ртуть жидкость 0,139 азот газ 1,042 масло жидкость ≈ 2,000 кислород газ 0,920 кварцевое стекло твёрдое тело 0,703 вода 373К газ 2,020 сусло пивное жидкость 3,9269 вода жидкость 4,183 вода твёрдое тело (0 °C) 2,060 Значения приведены для стандартных условий, если это не оговорено особо. Таблица II: Значения удельной теплоёмкости для некоторых строительных материалов Вещество Агрегатное состояние Удельная
теплоёмкость
кДж·кг-1·K-1Удельная
теплоёмкость
кДж·см³-1·K-1асфальт твёрдое тело 0,92 1,012-1,38 полнотелый кирпич твёрдое тело 0,84 1,344 силикатный кирпич твёрдое тело 1 1,2 — 2,2 бетон твёрдое тело 0,88 1,584 — 2,156 кронглас (стекло) твёрдое тело 0,67 1,709 флинт (стекло) твёрдое тело 0,503 1,761 — 2,414 оконное стекло твёрдое тело 0,84 2,016 — 2,268 гранит твёрдое тело 0,790 2,014 — 2,22 гипс твёрдое тело 1,09 2,507 мрамор, слюда твёрдое тело 0,880 2,305 — 2,5 песок твёрдое тело 0,835 1,19 — 1,336 сталь твёрдое тело 0,47 3,713 почва твёрдое тело 0,80 древесина твёрдое тело 1,7 0,68 — 1,36 См. также
Wikimedia Foundation.
2010.
- Удельная электролитическая проводимость
- Удельное вращение
Смотреть что такое «Удельная теплоемкость» в других словарях:
УДЕЛЬНАЯ ТЕПЛОЕМКОСТЬ — (обозначение с), тепло, необходимое для того, чтобы поднять температуру 1 кг вещества на 1К. Измеряется в Дж/К.кг (где Дж ДЖОУЛЬ). Вещества с высокой удельной теплоемкостью, такие как вода, требуют большего количества энергии для поднятия… … Научно-технический энциклопедический словарь
удельная теплоемкость — См. heat capacity. [http://www.oceanographers.ru/index.php?option=com glossary Itemid=238] Тематики океанология EN specific heat … Справочник технического переводчика
удельная теплоемкость — 3.1.4 удельная теплоемкость: Отношение теплоемкости материала к его массе. Источник … Словарь-справочник терминов нормативно-технической документации
удельная теплоемкость — savitoji šiluminė talpa statusas T sritis Standartizacija ir metrologija apibrėžtis Vienetinės masės medžiagos šiluminė talpa. atitikmenys: angl. heat capacity per unit mass; massic heat capacity; specific heat; specific heat capacity vok.… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
удельная теплоемкость — savitoji šiluminė talpa statusas T sritis Standartizacija ir metrologija apibrėžtis Šiluminė talpa, padalyta iš masės. atitikmenys: angl. heat capacity per unit mass; massic heat capacity; specific heat; specific heat capacity vok. Eigenwärme, f; … Penkiakalbis aiškinamasis metrologijos terminų žodynas
удельная теплоемкость — savitoji šiluminė talpa statusas T sritis Standartizacija ir metrologija apibrėžtis Šilumos kiekis, kurį reikia suteikti 1 kg medžiagos, kad jos temperatūra pakiltų vienu kelvinu. atitikmenys: angl. heat capacity per unit mass; massic heat… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
удельная теплоемкость — savitoji šiluminė talpa statusas T sritis Energetika apibrėžtis Vienetinės masės medžiagos šiluminė talpa. atitikmenys: angl. massic heat capacity; specific heat capacity vok. Eigenwärme, f; spezifische Wärme, f; spezifische Wärmekapazität, f rus … Aiškinamasis šiluminės ir branduolinės technikos terminų žodynas
удельная теплоемкость — savitoji šiluminė talpa statusas T sritis Energetika apibrėžtis Šiluminė talpa, padalyta iš masės. atitikmenys: angl. massic heat capacity; specific heat capacity vok. Eigenwärme, f; spezifische Wärme, f; spezifische Wärmekapazität, f rus.… … Aiškinamasis šiluminės ir branduolinės technikos terminų žodynas
удельная теплоемкость — savitoji šiluminė talpa statusas T sritis Energetika apibrėžtis Šilumos kiekis, kurį reikia suteikti 1 kg medžiagos, kad jos temteratūra pakiltų vienu kelvinu. atitikmenys: angl. massic heat capacity; specific heat capacity vok. Eigenwärme, f;… … Aiškinamasis šiluminės ir branduolinės technikos terminų žodynas
удельная теплоемкость — Теплоемкость единицы количества вещества (единицы массы) … Политехнический терминологический толковый словарь
Конспект «Количество теплоты. Удельная теплоёмкость»
«Количество теплоты. Удельная теплоёмкость»
Количество теплоты
Изменение внутренней энергии путём совершения работы характеризуется величиной работы, т.е. работа является мерой изменения внутренней энергии в данном процессе. Изменение внутренней энергии тела при теплопередаче характеризуется величиной, называемой количествоv теплоты.
Количество теплоты – это изменение внутренней энергии тела в процессе теплопередачи без совершения работы. Количество теплоты обозначают буквой Q.
Работа, внутренняя энергия и количество теплоты измеряются в одних и тех же единицах — джоулях (Дж), как и всякий вид энергии.

В тепловых измерениях в качестве единицы количества теплоты раньше использовалась особая единица энергии — калория (кал), равная количеству теплоты, необходимому для нагревания 1 грамма воды на 1 градус Цельсия (точнее, от 19,5 до 20,5 °С). Данную единицу, в частности, используют в настоящее время при расчетах потребления тепла (тепловой энергии) в многоквартирных домах. Опытным путем установлен механический эквивалент теплоты — соотношение между калорией и джоулем: 1 кал = 4,2 Дж.
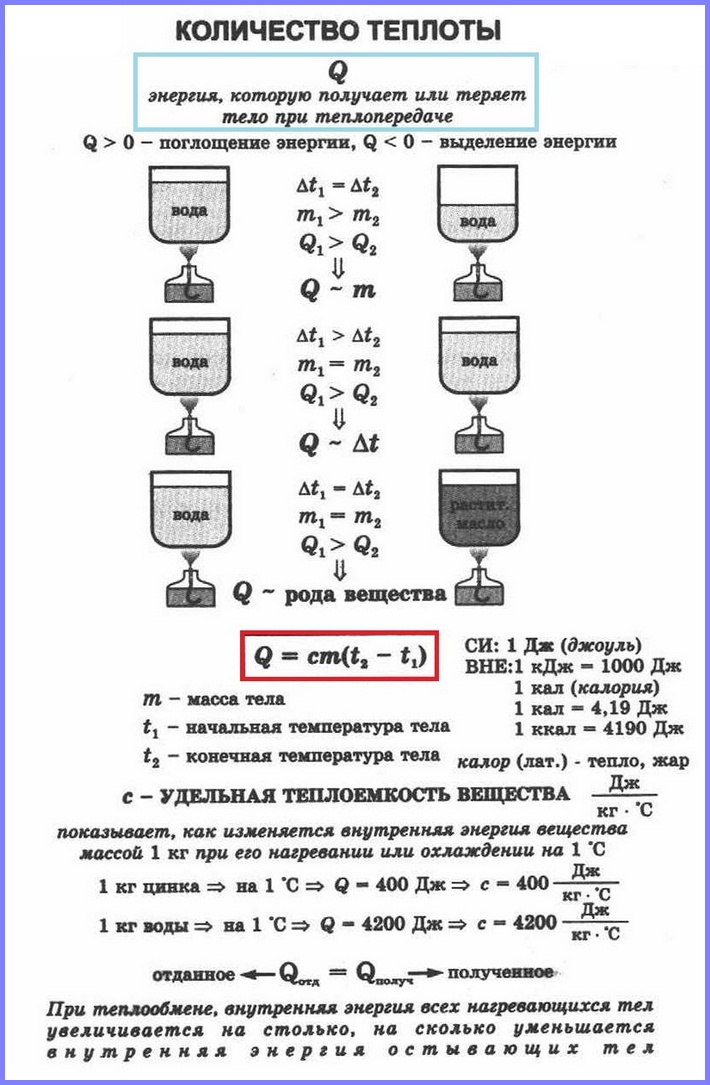
При передаче телу некоторого количества теплоты без совершения работы его внутренняя энергия увеличивается, если тело отдаёт какое-то количество теплоты, то его внутренняя энергия уменьшается.
Если в два одинаковых сосуда налить в один 100 г воды, а в другой 400 г при одной и той же температуре и поставить их на одинаковые горелки, то раньше закипит вода в первом сосуде. Таким образом, чем больше масса тела, тем большее количество тепла требуется ему для нагревания. То же самое и с охлаждением.

Количество теплоты, необходимое для нагревания тела зависит еще и от рода вещества, из которого это тело сделано. Эта зависимость количества теплоты, необходимого для нагревания тела, от рода вещества характеризуется физической величиной, называемой удельной теплоёмкостью вещества.
Удельная теплоёмкость
Удельная теплоёмкость – это физическая величина, равная количеству теплоты, которое необходимо сообщить 1 кг вещества для нагревания его на 1 °С (или на 1 К). Такое же количество теплоты 1 кг вещества отдаёт при охлаждении на 1 °С.
Удельная теплоёмкость обозначается буквой с. Единицей удельной теплоёмкости является 1 Дж/кг °С или 1 Дж/кг °К.
Значения удельной теплоёмкости веществ определяют экспериментально. Жидкости имеют большую удельную теплоёмкость, чем металлы; самую большую удельную теплоёмкость имеет вода, очень маленькую удельную теплоёмкость имеет золото.
Поскольку кол-во теплоты равно изменению внутренней энергии тела, то можно сказать, что удельная теплоёмкость показывает, на сколько изменяется внутренняя энергия 1 кг вещества при изменении его температуры на 1 °С. В частности, внутренняя энергия 1 кг свинца при его нагревании на 1 °С увеличивается на 140 Дж, а при охлаждении уменьшается на 140 Дж.
Количество теплоты Q, необходимое для нагревания тела массой m от температуры t1°С до температуры t2°С, равно произведению удельной теплоёмкости вещества, массы тела и разности конечной и начальной температур, т.е.
Q = c ∙ m (t2 — t1)
По этой же формуле вычисляется и количество теплоты, которое тело отдаёт при охлаждении. Только в этом случае от начальной температуры следует отнять конечную, т.е. от большего значения температуры отнять меньшее.

Это конспект по теме «Количество теплоты. Удельная теплоёмкость». Выберите дальнейшие действия:
ЗАДАЧНИК ОНЛ@ЙН БИБЛИОТЕКА 1 БИБЛИОТЕКА 2 Удельная теплоёмкость — это физическая величина, которая равно количеству теплоты, которое необходимо передать телу массой 1 кг, чтобы его температура изменилась на 1 градус по Цельсию. Удельная теплоемкость обозначается буквой с и измеряется в Дж/кг*градус по Цельсию. | Удельная теплоемкость расплавленных металлов и сжиженных газов. Удельная | ||||
Расплавленный металл или сжиженный газ | Температура, оС | Удельная теплоемкость | |
кДж/(кг К) | ккал/(кг оС) | ||
| Азот | -200,4 | 2,01 | 0,48 |
| Алюминий | 660-1000 | 1,09 | 0,26 |
| Водород | -257,4 | 7,41 | 1,77 |
| Воздух | -193,0 | 1,97 | 0,47 |
| Гелий | -269,0 | 4,19 | 1,00 |
| Золото | 1065-1300 | 0,14 | 0,034 |
| Кислород | -200,3 | 1,63 | 0,39 |
| Натрий | 100 | 1,34 | 0,33 |
| Олово | 250 | 0,25 | 0,060 |
| Свинец | 327 | 0,16 | 0,039 |
| Серебро | 960-1300 | 0,29 | 0,069 |
Удельная теплоемкость металлов и сплавов
Металл иои сплав | Температура, оС | Удельная теплоемкость | |
кДж/(кг К) | ккал/(кг оС) | ||
| Алюминий | 0-200 | 0,92 | 0,22 |
| Вольфрам | 0-1600 | 0,15 | 0,036 |
| Железо | 0-100 | 0,46 | 0,11 |
| 0-500 | 0,54 | 0,13 | |
| Золото | 0-1000 | 0,13 | 0,032 |
| Иридий | 0-500 | 0,15 | 0,037 |
| Магний | 0-500 | 1,10 | 0,27 |
| Медь | 0-300 | 0,40 | 0,097 |
| Никель | 0-300 | 0,50 | 0,12 |
| Олово | 0-200 | 0,23 | 0,056 |
| Платина | 0-500 | 0,14 | 0,033 |
| Свинец | 0-300 | 0,14 | 0,033 |
| Серебро | 0-500 | 0,25 | 0,059 |
| Сталь | 50-300 | 0,50 | 0,12 |
| Цинк | 0-300 | 0,40 | 0,097 |
| Чугун | 0-200 | 0,54 | 0,13 |
Удельная темлоемкость твердых веществ
| Вещество | Удельная теплоемкость | Вещество | Удельная теплоемкость | ||
кДж/(кг К) | ккал/(кг оС) | кДж/(кг К) | ккал/(кг оС) | ||
| Азот твердый (при t=-250 oC) | 0,46 | 0,11 | Кислород твердый (при t=-200,3 oC) | 1,60 | 0,39 |
| Бетон (при t=20 oC) | 0,88 | 0,21 | Лед (в интервале от -40 до 0oC) | 2,10 | 0,50 |
| Бумага (при t=20 oC) | 1,50 | 0,36 | Нафталин (при t=20 oC) | 1,30 | 0,31 |
| Воздух твердый (при t=-193 oC) | 2,0 | 0,47 | Парафин (при t=20 oC) | 2,89 | 0,69 |
| Графит | 0,75 | 0,18 | Пробка | 2,00 | 0,48 |
| Дерево: | Стекло: | ||||
| дуб | 2,40 | 0,57 | обыкновенное | 0,67 | 0,16 |
| ель, сосна | 2,70 | 0,65 | зеркальное | 0,79 | 0,19 |
| Каменная соль | 0,92 | 0,22 | лабораторное | 0,84 | 0,20 |
| Камень | 0,84 | 0,20 | Фарфор | 1,10 | 0,26 |
| Кирпич (при t=0 oC) | 0,88 | 0,21 | Шифер (при t=20 oC) | 0,75 | 0,18 |
Удельная теплоемкость металлов и сплавов
(при нормальном атмосферном давлении)
Металл или сплав | Температура, оС | Удельная теплоемкость | |
кДж/(кг К) | ккал/(кг оС) | ||
| Алюминий | 0-200 | 0,92 | 0,22 |
| Вольфрам | 0-1600 | 0,15 | 0,036 |
| Железо | 0-100 | 0,46 | 0,11 |
| 0-500 | 0,54 | 0,13 | |
| Золото | 0-1000 | 0,13 | 0,032 |
| Иридий | 0-500 | 0,15 | 0,037 |
| Магний | 0-500 | 1,10 | 0,27 |
| Медь | 0-300 | 0,40 | 0,097 |
| Никель | 0-300 | 0,50 | 0,12 |
| Олово | 0-200 | 0,23 | 0,056 |
| Платина | 0-500 | 0,14 | 0,033 |
| Свинец | 0-300 | 0,14 | 0,033 |
| Серебро | 0-500 | 0,25 | 0,059 |
| Сталь | 50-300 | 0,50 | 0,12 |
| Цинк | 0-300 | 0,40 | 0,097 |
| Чугун | 0-200 | 0,54 | 0,13 |
Удельная теплоемкость жидкостей
(при нормальном атмосферном давлении)
Жидкость | Температура, оС | Удельная теплоемкость | |
кДж/(кг К) | ккал/(кг оС) | ||
| Бензин (Б-70) | 20 | 2,05 | 0,49 |
| Вода | 1-100 | 4,19 | 1,00 |
| Глицерин | 0-100 | 2,43 | 0,58 |
| Керосин | 0-100 | 2,09 | 0,50 |
| Масло машинное | 0-100 | 1,67 | 0,40 |
| Масло подсолнечное | 20 | 1,76 | 0,42 |
| Мед | 20 | 2,43 | 0,58 |
| Молоко | 20 | 3,94 | 0,94 |
| Нефть | 0-100 | 1,67-2,09 | 0,40-0,50 |
| Ртуть | 0-300 | 0,138 | 0,033 |
| Спирт | 20 | 2,47 | 0,59 |
| Эфир | 18 | 3,34 | 0,56 |
…
Удельная теплоемкость формула ℹ️ определения, обозначение и единицы измерения, физический смысл, от чего зависит, критерии нахождения величины, таблица значений и примеры задач с вычислениями
Определение термина
Физическая величина, характеризующая, сколько тепловой энергии требуется на единицу вещества, и есть удельная теплоемкость, или энтальпия. Также она позволяет определить, сколько тепла необходимо отвести от единицы того или иного соединения, чтобы изменить на 1 градус его температуру. Неважно, по какой системе измеряется этот параметр:
- Кельвина;
- Цельсия;
- Фаренгейта.
Единицей измерения удельной теплоемкости является джоуль, поделенный на килограмм и градус Кельвина. Есть и особая, внесистемная единица, представляющая собой показатель калорий, который имеет вид произведения килограммов и градусов Цельсия. Обозначается теплоемкость удельного типа посредством специальных индексов. Допустим, в ситуации, когда наблюдаются постоянные отметки давления, используется индекс p. Когда постоянство сохраняет объем, его место занимает буква v. Единица, в которой измеряется удельная теплоёмкость — килоджоуль.
Молярная теплоёмкость – отдельный показатель. Это количество тепловой энергии, которое показывает требующееся для нагрева 1 моль вещества на каждый градус. Во время плавления выделяется также определенный объем тепловой энергии. Теплопроводность — разновидность теплопередачи, когда энергия перемещается от нагретой области вещества к более холодной, посредством передвижения частиц. На уроках физики проводится объяснение физического смысла теплоёмкости. Ее размерность обозначена так:
Физическая величина может быть охарактеризована различными способами. В частности, допускается формулировка, согласно которой ее можно представить в виде комбинации теплоемкости вещества к его массе.
Теплоемкость, в свою очередь, это физическая величина. Она отображает объем тепла, который надо подвести либо отвести от вещества для изменения показателя его температуры. Если это объект, масса которого превышает 1 кг, определять этот показатель надо, как для единичного значения.
Примеры для тех или иных веществ
Путем экспериментов удалось выяснить, что показатель является различным для тех или иных веществ. Например, в отношении воды имеется показатель 4,187 кДж. Наибольшим он является у водорода. Для него установлено нормальное значение 14,300 кДж. Наименьшее оно у золота — 0,129 кДж.
Благодаря современным достижениям науки можно увеличить скорость обнаружения интересующих значений и свойств. Если раньше приходилось искать по справочнику соответствующую таблицу, то теперь на любом телефоне появилась опция для поиска через интернет. Наиболее примечательные вещества, теплоёмкость которых представляет интерес чаще всего это:
- воздушные массы (идеальные и реальные газы) — 1,005 кДж;
- металл алюминий — 0,930 кДж;
- медь — 0,385 кДж.
Лабораторная работа
На школьных уроках определяется теплоемкость в отношении твердых веществ. Ее удаётся подсчитать при сравнении с тем показателем, который уже известен. Таблица удельной теплоемкости создана специально для удобства подсчетов.
Берут воду и твердый объект в нагретом состоянии, после чего производят замер температуры обоих. Отпускают твердое тело в жидкость и дожидаются момента теплового равновесия. Чтобы организовать такой эксперимент, необходим колориметр. Соответственно, имея такой прибор, можно пренебрегать небольшими потерями энергии.
В дальнейшем записывается формула объёма тепла, которая переходит в воду при взаимодействии с твёрдым объектом. Второе равенство отображает энергию, передаваемую твёрдым веществом при снижении температуры. Указанные показатели равны. После вычислений можно выявить теплоемкость компонентов, из которых состоит твердый объект. При этом обычно смотрят на данные таблицы, пытаясь таким образом определить, из какого вещества оно было сделано.
Первая задача
Допустим, металл меняет свои показатели температуры в пределах 20-24°. Внутренняя энергия этого вещества увеличивается одновременно на 152 кДж. Необходимо рассчитать, сколько составляет теплоёмкость металлического объекта при условии, что его масса составляет 100 г.
Для решения этой задачи надо воспользоваться специальной формулой. Достаточно подставить имеющиеся значения, но перед этим следует перевести массу в килограммы. Если этого не сделать, ответ будет неверным. В каждом килограмме насчитывается 1000 г. По этой причине 100 г необходимо поделить на 1000. Получается значение, равное 0,1 кг.
После произведенных подсчетов с использованием формулы получается такой результат:
Другие условия
Согласно 2 задаче, даётся энергия внесистемной единицы. Следует выявить температуру, при которой вода в количестве 5 л остынет, если её первоначально возьмут при температуре кипения. При этом она выделяет 1684 кДж тепла. Это количество переводится в джоули = 1680000 Дж.
Чтобы найти ответ, надо воспользоваться формулой, в которой используется масса. С другой стороны, в задаче она не приводится. Но несмотря на это, указан объем жидкости, соответственно, для нахождения критерия допустимо подставить уравнение с коэффициентами:
Плотность ее составляет 1000 кг на м3. Но надо подставлять объём в кубических метрах. Для перевода исходного значения надо поделить его на 1000. Получается число, равное 0,005 м3.
Производятся дальнейшие расчеты, и на выходе получается выражение:
В дальнейшем применяется формула:
Получается отметка, равная 20 ºС.
Другая задача: имеется стакан, в который налито 50 г воды. Сам он имеет массу 100 г. Температура жидкости первоначально имеет показатели 0°. Необходимо найти объем тепла, необходимого для доведения воды до кипения.
Для решения этой задачи надо ввести подходящие параметры. Можно дать условное обозначение характеристикам, которые касаются стакана, в виде единицы. Всё, что касается воды, обозначается индексом 2. Далее следует найти цифры, соответствующие теплоемкости, через таблицу. Если это тара, выполненная из лабораторного стекла, то у нее будут показатели с1 = 840 Дж/ (кг * ºС). Точный показатель для воды будет иметь вид:
Масса в этой задаче приводится в граммах. После перевода получаются показатели:
Начальная температура равна 0°. Необходимо найти параметры, соответствующие температуре кипения — 100°. Стакан нагревается одновременно с жидкостью, которая наполнена им. Поэтому начальное количество теплоты необходимо получить при складывании несколько показателей. Это параметр, получаемый при нагревании стекла, а второй показатель обнаруживается после нагрева воды. Составляется формула такого вида:
Сюда подставляются имеющееся значения, после чего она принимает следующий облик:
Те или иные материалы с одинаковой массой предполагают разные объемы тепла, необходимые для нагрева. Этот показатель обычно больше у металлов, нежели у древесины, например, алюминия или поверхности из штукатурки. То есть вид материала влияет на этот показатель в той же степени, что и масса. Чтобы нагреть бетон в объеме 1 кг требуется примерно 1000 Дж.
Показатели воздуха
Теплоемкость воздуха отличается, в зависимости от сопутствующих условий. Её величина влияет на объём тепла, который требуется для подведения при постоянном давлении к 1 кг воздуха. При этом задается цель — увеличить температуру на градус. Если газ имеет температуру 20°С, то необходимо подведение 1005 джоулей тепла, чтобы нагреть 1 кг этого вещества.
По мере роста температуры повышается удельная теплоемкость. Но здесь имеет место нелинейная зависимости. Средняя теплоемкость почти не меняется, если не отмечается воздействия экстремального холода и других критичных явлений. Но от температуры окружающего пространства зависит удельная теплоемкость вещества не так явно, если сравнивать с вязкостью. Иногда такие связи изображают в виде графиков для лучшего понимания.
При нагреве газов теплоемкость способна возрастать в 1,2 раз.
У влажного воздуха такой параметр является более высоким, нежели у сухого. Вода по сравнению с ним имеет большие значения теплоемкости. Соответственно, когда капли воды висят в воздухе, его теплоемкость становится больше.
Теплоёмкость — Википедия
Материал из Википедии — свободной энциклопедии
Теплоёмкость — физическая величина, определяемая как количество теплоты, которое необходимо подвести к телу в данном процессе, чтобы его температура возросла на один кельвин[1][2]:
C=δQdT.{\displaystyle C={\delta Q \over dT}.}
Во многих важных случаях приращение температуры тела прямо пропорционально сообщённому ему количеству теплоты и теплоёмкость тела является константой. В общем случае теплоёмкость тела может зависеть от параметров состояния этого тела, например его температуры или объёма[1][2].
Удельная, молярная и объёмная теплоёмкости
Очевидно, что чем больше масса тела, тем больше требуется теплоты для его нагревания, и теплоёмкость тела пропорциональна количеству вещества, содержащегося в нём. Количество вещества может характеризоваться массой или количеством молей. Поэтому удобно пользоваться понятиями удельной теплоёмкости (теплоёмкости единицы массы тела):
- c=Cm{\displaystyle c={C \over m}}
и молярной теплоёмкости (теплоёмкости одного моля вещества):
- Cμ=Cν,{\displaystyle C_{\mu }={C \over \nu },}
где ν=mμ{\displaystyle \nu ={m \over \mu }} — количество вещества в теле; m{\displaystyle m} — масса тела; μ{\displaystyle \mu } — молярная масса. Молярная и удельная теплоёмкости связаны соотношением Cμ=cμ{\displaystyle C_{\mu }=c\mu }[1][2].
Объёмная теплоёмкость (теплоёмкость единицы объёма тела):
- C′=CV.{\displaystyle C’={C \over V}.}
Теплоёмкость для различных процессов и состояний вещества
Понятие теплоёмкости определено как для веществ в различных агрегатных состояниях (твёрдых тел, жидкостей, газов), так и для ансамблей частиц и квазичастиц (в физике металлов, например, говорят о теплоёмкости электронного газа).
Теплоёмкость идеального газа
Теплоёмкость системы невзаимодействующих частиц (например, идеального газа) определяется числом степеней свободы частиц.
Молярная теплоёмкость при постоянном объёме:
- CV=dUdT=i2R,{\displaystyle C_{V}={dU \over dT}={\frac {i}{2}}R,}
где R{\displaystyle R} ≈ 8,31 Дж/(моль·К) — универсальная газовая постоянная, i{\displaystyle i} — число степеней свободы молекулы[1][2].
Молярная теплоёмкость при постоянном давлении[1][2]:
- CP=dUdT+PdVdT=i+22R.{\displaystyle C_{P}={dU \over dT}+{PdV \over dT}={{i+2} \over 2}R.}
Теплоёмкость кристаллов
Теория теплоёмкости
Сравнение моделей Дебая и Эйнштейна для теплоёмкости твёрдого тела
Существует несколько теорий теплоёмкости твердого тела:
Существующие теории теплоёмкости не охватывают всех особенностей поведения теплоёмкости различных твёрдых тел. В первую очередь это относится к аномальным пикам на кривых теплоёмкости, а также росту в высокотемпературной области удельной теплоёмкости над уровнем 3R нормальной (колебательной) составляющей. Возникновение некоторых из перечисленных аномалий детально исследовано и имеет своё физическое объяснение. Это в первую очередь относится к лямбда-пикам, связанным с ферромагнитными и ориентационными переходами, а также с переходами от упорядоченных к неупорядоченным структурам. Аномальные отклонения над уровнем 3R кривой теплоёмкости графита и алмаза в высокотемпературной области (Т > 3000 K) обусловлены процессами термодеструкции с переходом в плавление. Аномальные пики на кривых теплоёмкости германия и гафния объясняются процессами в кристаллической решетке, контролируемыми больцмановским фактором exp(-E/RT).
Примечания
- ↑ 1 2 3 4 5 Никеров. В. А. Физика: учебник и практикум для академического бакалавриата. — Юрайт, 2015. — С. 127—129. — 415 с. — ISBN 978-5-9916-4820-2.
- ↑ 1 2 3 4 5 Ильин В. А. Физика: учебник и практикум для прикладного бакалавриата. — Юрайт, 2016. — С. 142—143. — 399 с. — ISBN 978-5-9916-6343-4.
Литература
По какой формуле можно произвести расчёт удельной теплоёмкости вещества (Cp)
Удельная теплоёмкость — это энергия, которая требуется для увеличения температуры 1 грамма чистого вещества на 1°. Параметр зависит от его химического состава и агрегатного состояния: газообразное, жидкое или твёрдое тело. После его открытия начался новый виток развития термодинамики, науки о переходных процессах энергии, которые касаются теплоты и функционирования системы.
Как правило, удельная теплоёмкость и основы термодинамики используются при изготовлении радиаторов и систем, предназначенных для охлаждения автомобилей, а также в химии, ядерной инженерии и аэродинамике. Если вы хотите узнать, как рассчитывается удельная теплоёмкость, то ознакомьтесь с предложенной статьёй.
Формула
Перед тем, как приступить к непосредственному расчёту параметра следует ознакомиться с формулой и её компонентами.
Формула для расчёта удельной теплоёмкости имеет следующий вид:
Знание величин и их символических обозначений, использующихся при расчёте, крайне важно. Однако необходимо не только знать их визуальный вид, но и чётко представлять значение каждого из них. Расчёт удельной теплоёмкости вещества представлен следующими компонентами:
ΔT – символ, означающий постепенное изменение температуры вещества. Символ «Δ» произносится как дельта.
ΔT можно рассчитать по формуле:
ΔT = t2–t1, где
- t1 – первичная температура;
- t2 – конечная температура после изменения.
m – масса вещества используемого при нагреве (гр).
Q – количество теплоты (Дж/J)
На основании Цр можно вывести и другие уравнения:
- Q = m*цp*ΔT – количество теплоты ;
- m = Q/цр*(t2 — t1) – массы вещества;
- t1 = t2–(Q/цp*m) – первичной температуры;
- t2 = t1+(Q/цp*m) – конечной температуры.
Инструкция по расчёту параметра
Рассчитать с вещества достаточно просто и чтобы это сделать нужно, выполнить следующие шаги:
- Взять расчётную формулу: Теплоемкость = Q/(m*∆T)
- Выписать исходные данные.
- Подставить их в формулу.
- Провести расчёт и получим результат.
В качестве примера произведём расчёт неизвестного вещества массой 480 грамм обладающего температурой 15ºC, которая в результате нагрева (подвода 35 тыс. Дж) увеличилась до 250º.
Согласно инструкции приведённой выше производим следующие действия:
Выписываем исходные данные:
- Q = 35 тыс. Дж;
- m = 480 г;
- ΔT = t2–t1 =250–15 = 235 ºC.
Берём формулу, подставляем значения и решаем:
с=Q/(m*∆T)=35тыс.Дж/(480 г*235º)=35тыс.Дж/(112800 г*º)=0,31 Дж/г*º.

Расчёт
Выполним расчёт CP воды и олова при следующих условиях:
- m = 500 грамм;
- t1 =24ºC и t2 = 80ºC – для воды;
- t1 =20ºC и t2 =180ºC – для олова;
- Q = 28 тыс. Дж.
Для начала определяем ΔT для воды и олова соответственно:
- ΔТв = t2–t1 = 80–24 = 56ºC
- ΔТо = t2–t1 = 180–20 =160ºC
Затем находим удельную теплоёмкость:
- с=Q/(m*ΔТв)= 28 тыс. Дж/(500 г *56ºC) = 28 тыс.Дж/(28 тыс.г*ºC) = 1 Дж/г*ºC.
- с=Q/(m*ΔТо)=28тыс.Дж/(500 гр*160ºC)=28 тыс.Дж/(80 тыс.г*ºC)=0,35 Дж/г*ºC.
Таким образом, удельная теплоемкость воды составила 1 Дж/г *ºC, а олова 0,35 Дж/г*ºC. Отсюда можно сделать вывод о том, что при равном значении подводимого тепла в 28 тыс. Дж олово нагрется быстрее воды, поскольку его теплоёмкость меньше.
Теплоёмкостью обладают не только газы, жидкости и твёрдые тела, но и продукты питания.
Как рассчитать теплоемкость продуктов питания
При расчёте емкости питания уравнение примет следующий вид:
с=(4.180*w)+(1.711*p)+(1.928*f)+(1.547*c)+(0.908 *a), где:
- w – количество воды в продукте;
- p – количество белков в продукте;
- f – процентное содержание жиров;
- c – процентное содержание углеводов;
- a – процентное содержание неорганических компонентов.
Определим теплоемкость плавленого сливочного сыра Viola. Для этого выписываем нужные значения из состава продукта (масса 140 грамм):
- вода – 35 г;
- белки – 12,9 г;
- жиры – 25,8 г;
- углеводы – 6,96 г;
- неорганические компоненты – 21 г.
Затем находим с:
- с=(4.180*w)+(1.711*p)+(1.928*f)+(1.547*c)+(0.908*a)=(4.180*35)+(1.711*12,9)+(1.928*25,8) + (1.547*6,96)+(0.908*21)=146,3+22,1+49,7+10,8+19,1=248 кДж /кг*ºC.

Полезные советы
Всегда помните, что:
- процесс нагревания металла проходит быстрее, чем у воды, так как он обладает CP в 2,5 раза меньше;
- по возможности преобразуйте полученные результаты в более высокий порядок, если позволяют условия;
- в целях проверки результатов можно воспользоваться интернетом и посмотреть с для расчётного вещества;
- при равных экспериментальных условиях более значительные температурные изменения будут наблюдаться у материалов с низкой удельной теплоёмкостью.
Видео
Разобраться в этой теме вам поможет видео урок.
28. Теплоёмкость. Молярная и удельная теплоёмкости. Связь между ними. Формула Майера.
Количество
тепла, при получении которого температура
тела повышается на один градус, называется
теплоемкостью. Согласно этому определению.
Теплоемкость,
отнесенная к единице массы, называется
удельной
теплоемкостью.
Теплоемкость, отнесенная к одному молю,
называется моляpной
теплоемкостью.
Итак,
теплоемкость опpеделяется чеpез понятие
количества теплоты. Но последнее, как
и pабота, зависит от пpоцесса. Значит и
теплоемкость зависит от пpоцесса.
Сообщать теплоту — нагpевать тело — можно
пpи pазличных условиях. Однако пpи
pазличных условиях на одно и то же
увеличение темпеpатуpы тела потpебуется
pазличное количество теплоты. Следовательно,
тела можно хаpактеpизовать не одной
теплоемкостью, а бесчисленным множеством
(столько же, сколько можно пpидумать
всевозможных пpоцессов, пpи котоpых
пpоисходит теплопеpедача). Однако на
пpактике обычно пользуются опpеделением
двух теплоемкостей: теплоемкости пpи
постоянном объеме и теплоемкости пpи
постоянном давлении.
Теплоемкость
различается в зависимости от того, при
каких условиях происходит нагревание
тела — при постоянном объеме или при
постоянном давлении.
Если
нагревание тела происходит при постоянном
объеме, т. е. dV
= 0, то работа
равна нулю. В этом случае передаваемое
телу тепло идет только на изменение его
внутренней энергии, dQ
= dE,
и в этом случае теплоемкость равна
изменению внутренней энергии при
изменении температуры на 1 К, т. е.
.Поскольку
для газа
,
то.Эта
формула определяет теплоемкость 1 моля
идеального газа, называемую молярной.
При нагревании газа при постоянном
давлении его объем меняется, сообщенное
телу тепло идет не только на увеличение
его внутренней энергии, но и на совершение
работы, т.е.dQ
= dE
+ PdV.
Теплоемкость при постоянном давлении
.
Для
идеального газа PV
= RT
и поэтому
PdV =
RdT.
Учитывая
это, найдем.Отношение
представляет собой величину, характерную
для каждого газа и определяемую числом
степеней свободы молекул газа. Измерение
теплоемкости тела есть, таким образом,
способ непосредственного измерения
микроскопических характеристик
составляющих его молекул.
Формулы
для теплоемкости идеального газа
приблизительно верно описывают
эксперимент, причем, в основном, для
одноатомных газов. Согласно формулам,
полученным выше, теплоемкость не должна
зависеть от температуры. На самом деле
наблюдается картина, изображенная на
рис., полученная опытным путем для
двухатомного газа водорода. На участке
1 газ ведет себя как система частиц,
обладающих лишь поступательными
степенями свободы, на участке 2 возбуждается
движение, связанное с вращательными
степенями свободы и, наконец, на участке
3 появляются две колебательные степени
свободы. Ступеньки на кривой хорошо
согласуются с формулой (2.35), однако между
ними теплоемкость растет с температурой,
что соответствует как бы нецелому
переменному числу степеней свободы.
Такое поведение теплоемкости указывает
на недостаточность используемого нами
представления об идеальном газе для
описания реальных свойств вещества.
Связь
молярной теплоёмкости с удельной
теплоёмкостьюС=M•с,
где с —
удельная
теплоёмкость,
М —
молярная
масса.Формула
Майера.
Для
любого идеального газа справедливо
соотношение Майера:
,где
R —
универсальная
газовая постоянная,
—
молярная
теплоемкость при постоянном давлении,
—
молярная
теплоемкость при постоянном объёме.
Удельная теплоемкость и вода
- БЕСПЛАТНАЯ ЗАПИСЬ КЛАСС
- КОНКУРСНЫЕ ЭКЗАМЕНА
- BNAT
- Классы
- Класс 1-3
- Класс 4-5
- Класс 6-10
- Класс 110003 CBSE
- Книги NCERT
- Книги NCERT для класса 5
- Книги NCERT, класс 6
- Книги NCERT для класса 7
- Книги NCERT для класса 8
- Книги NCERT для класса 9
- Книги NCERT для класса 10
- NCERT Книги для класса 11
- NCERT Книги для класса 12
- NCERT Exemplar
- NCERT Exemplar Class 8
- NCERT Exemplar Class 9
- NCERT Exemplar Class 10
- NCERT Exemplar Class 11
9plar
- Книги NCERT
- RS Aggarwal
- RS Aggarwal Решения класса 12
- RS Aggarwal Class 11 Solutions
- RS Aggarwal Решения класса 10
- Решения RS Aggarwal класса 9
- Решения RS Aggarwal класса 8
- Решения RS Aggarwal класса 7
- Решения RS Aggarwal класса 6
- RD Sharma
- RD Sharma Class 6 Решения
- RD Sharma Class 7 Решения
- Решения RD Sharma Class 8
- Решения RD Sharma Class 9
- Решения RD Sharma Class 10
- Решения RD Sharma Class 11
- Решения RD Sharma Class 12
- PHYSICS
- Механика
- Оптика
- Термодинамика
- Электромагнетизм
- ХИМИЯ
- Органическая химия
- Неорганическая химия
- Периодическая таблица
- MATHS
- Статистика
- 9000 Pro Числа
- Числа
- 9000 Pro Числа Тр Игонометрические функции
- Взаимосвязи и функции
- Последовательности и серии
- Таблицы умножения
- Детерминанты и матрицы
- Прибыль и убытки
- Полиномиальные уравнения
- Деление фракций
- Microology
- 0003000
- FORMULAS
- Математические формулы
- Алгебраные формулы
- Тригонометрические формулы
- Геометрические формулы
- КАЛЬКУЛЯТОРЫ
- Математические калькуляторы
- 000 CALCULATORS
- 000
- 000 Калькуляторы по химии 900 Образцы документов для класса 6
- Образцы документов CBSE для класса 7
- Образцы документов CBSE для класса 8
- Образцы документов CBSE для класса 9
- Образцы документов CBSE для класса 10
- Образцы документов CBSE для класса 1 1
- Образцы документов CBSE для класса 12
0003000
- Вопросники предыдущего года CBSE
- Вопросники предыдущего года CBSE, класс 10
- Вопросники предыдущего года CBSE, класс 12
- HC Verma Solutions
- HC Verma Solutions Класс 11 Физика
- HC Verma Solutions Класс 12 Физика
- Решения Лакмира Сингха
- Решения Лахмира Сингха класса 9
- Решения Лахмира Сингха класса 10
- Решения Лакмира Сингха класса 8
9000 Класс
9000BSE 9000 Примечания3 2 6 Примечания CBSE
Примечания
- Дополнительные вопросы по математике класса 8 CBSE
- Дополнительные вопросы по науке 8 класса CBSE
- Дополнительные вопросы по математике класса 9 CBSE
- Дополнительные вопросы по математике класса 9 CBSE Вопросы
- CBSE Class 10 Дополнительные вопросы по математике
- CBSE Class 10 Science Extra questions
- Class 3
- Class 4
- Class 5
- Class 6
- Class 7
- Class 8 Класс 9
- Класс 10
- Класс 11
- Класс 12
- Решения NCERT для класса 11
- Решения NCERT для класса 11 по физике
- Решения NCERT для класса 11 Химия
- Решения NCERT для биологии класса 11
- Решение NCERT s Для класса 11 по математике
- NCERT Solutions Class 11 Accountancy
- NCERT Solutions Class 11 Business Studies
- NCERT Solutions Class 11 Economics
- NCERT Solutions Class 11 Statistics
- NCERT Solutions Class 11 Commerce
- NCERT Solutions for Class 12
- Решения NCERT для физики класса 12
- Решения NCERT для химии класса 12
- Решения NCERT для биологии класса 12
- Решения NCERT для математики класса 12
- Решения NCERT, класс 12, бухгалтерский учет
- Решения NCERT, класс 12, бизнес-исследования
- NCERT Solutions Class 12 Economics
- NCERT Solutions Class 12 Accountancy Part 1
- NCERT Solutions Class 12 Accountancy Part 2
- NCERT Solutions Class 12 Micro-Economics
- NCERT Solutions Class 12 Commerce
- NCERT Solutions Class 12 Macro-Economics
- NCERT Solut Ионы Для класса 4
- Решения NCERT для математики класса 4
- Решения NCERT для класса 4 EVS
- Решения NCERT для класса 5
- Решения NCERT для математики класса 5
- Решения NCERT для класса 5 EVS
- Решения NCERT для класса 6
- Решения NCERT для математики класса 6
- Решения NCERT для науки класса 6
- Решения NCERT для класса 6 по социальным наукам
- Решения NCERT для класса 6 Английский язык
- Решения NCERT для класса 7
- Решения NCERT для математики класса 7
- Решения NCERT для науки класса 7
- Решения NCERT для социальных наук класса 7
- Решения NCERT для класса 7 Английский язык
- Решения NCERT для класса 8
- Решения NCERT для математики класса 8
- Решения NCERT для науки 8 класса
- Решения NCERT для социальных наук 8 класса ce
- Решения NCERT для класса 8 Английский
- Решения NCERT для класса 9
- Решения NCERT для класса 9 по социальным наукам
- Решения NCERT для математики класса 9
- Решения NCERT для математики класса 9 Глава 1
- Решения NCERT для математики класса 9, глава 2
- для математики класса 9, глава 3
- Решения NCERT для математики класса 9, глава 4
- Решения NCERT для математики класса 9, глава 5
- для математики класса 9, глава 6
- Решения NCERT для математики класса 9, глава 7
- для математики класса 9, глава 8
- Решения NCERT для математики класса 9, глава 9
- Решения NCERT для математики класса 9, глава 10
- для математики класса 9, глава 11
- NCERT для математики класса 9 Глава 12
- для математики класса 9 Глава 13
- NCER Решения T для математики класса 9 Глава 14
- Решения NCERT для математики класса 9 Глава 15
Решения NCERT
Решения NCERT
Решения NCERT
Решения NCERT
Решения
Решения NCERT
- Решения NCERT для науки класса 9
- Решения NCERT для науки класса 9 Глава 1
- Решения NCERT для науки класса 9 Глава 2
- Решения NCERT для науки класса 9 Глава 3
- Решения NCERT для науки класса 9 Глава 4
- Решения NCERT для науки класса 9 Глава 5
- Решения NCERT для науки класса 9 Глава 6
- Решения NCERT для науки класса 9 Глава 7
- Решения NCERT для науки класса 9 Глава 8
- Решения NCERT для науки класса 9 Глава 9
- Решения NCERT для науки класса 9 Глава 10
- Решения NCERT для науки класса 9 Глава 12
- Решения NCERT для науки класса 9 Глава 11
- Решения NCERT для науки класса 9 Глава 13
- для науки класса 9 Глава 14
- Решения NCERT для класса 9 по науке Глава 15
Решения NCERT
- Решения NCERT для класса 10
- Решения NCERT для класса 10 по социальным наукам
- Решения NCERT для математики класса 10
- Решения NCERT для класса 10 по математике Глава 1
- Решения NCERT для математики класса 10, глава 2
- Решения NCERT для математики класса 10, глава 3
- Решения NCERT для математики класса 10, глава 4
- Решения NCERT для математики класса 10, глава 5
- Решения NCERT для математики класса 10, глава 6
- Решения NCERT для математики класса 10, глава 7
- Решения NCERT для математики класса 10, глава 8
- Решения NCERT для математики класса 10, глава 9
- Решения NCERT для математики класса 10, глава 10
- Решения NCERT для математики класса 10 Глава 11
- Решения NCERT для математики класса 10 Глава 12
- Решения NCERT для математики класса 10 Глава ter 13
- Решения NCERT для математики класса 10, глава 14
- Решения NCERT для математики класса 10, глава 15
- Решения NCERT для науки класса 10
- Решения NCERT для класса 10, наука, глава 1
- Решения NCERT для класса 10 Наука, глава 2
- Решения NCERT для класса 10, глава 3
- Решения NCERT для класса 10, глава 4
- Решения NCERT для класса 10, глава 5
- Решения NCERT для класса 10, глава 6
- Решения NCERT для класса 10 Наука, глава 7
- Решения NCERT для класса 10, глава 8
- Решения NCERT для класса 10, глава 9
- Решения NCERT для класса 10, глава 10
- Решения NCERT для класса 10, глава 11
- Решения NCERT для класса 10 Наука Глава 12
- Решения NCERT для класса 10 Наука Глава 13
- NCERT S Решения для класса 10 по науке Глава 14
- Решения NCERT для класса 10 по науке Глава 15
- Решения NCERT для класса 10 по науке Глава 16
- Программа NCERT
- NCERT
- Class 11 Commerce Syllabus
- Учебный план класса 11
- Учебный план класса 11
- Учебный план экономического факультета 11
- Учебный план по коммерции класса 12
- Учебный план класса 12
- Учебный план класса 12
- Учебный план
- Класс 12 Образцы документов для коммерции
- Образцы документов для коммерции класса 11
- Образцы документов для коммерции класса 12
- TS Grewal Solutions
- TS Grewal Solutions Class 12 Accountancy
- TS Grewal Solutions Class 11 Accountancy
- Отчет о движении денежных средств 9 0004
- Что такое предпринимательство
- Защита прав потребителей
- Что такое основные средства
- Что такое баланс
- Что такое фискальный дефицит
- Что такое акции
- Разница между продажами и маркетингом
- ICC
- Образцы документов ICSE
- Вопросы ICSE
- ML Aggarwal Solutions
- ML Aggarwal Solutions Class 10 Maths
- ML Aggarwal Solutions Class 9 Maths
- ML Aggarwal Solutions Class 8 Maths
- ML Aggarwal Solutions Class 7 Maths Решения Математика класса 6
- Решения Селины
- Решения Селины для класса 8
- Решения Селины для класса 10
- Решение Селины для класса 9
- Решения Фрэнка
- Решения Фрэнка для математики класса 10
- Франк Решения для математики 9 класса
9000 4
- ICSE Class
- ICSE Class 6
- ICSE Class 7
- ICSE Class 8
- ICSE Class 9
- ICSE Class 10
- ISC Class 11
- ISC Class 12
03
- 900 Экзамен по IAS
- Мок-тест IAS 2019 1
- Мок-тест IAS4
2
- Экзамен KPSC KAS
- Экзамен UPPSC PCS
- Экзамен MPSC
- Экзамен RPSC RAS
- TNPSC Group 1
- APPSC Group 1
- Экзамен BPSC
- Экзамен WPSC
- Экзамен
- Экзамен GPSC
- Ответный ключ UPSC 2019
- Коучинг IAS Бангалор
- Коучинг IAS Дели
- Коучинг IAS Ченнаи
- Коучинг IAS Хайдарабад
- Коучинг IAS Мумбаи
9000 JEE 9000 JEE 9000 Advanced
- Программа BYJU NEET
- NEET 2020
- NEET Eligibility
- NEET Eligibility
- NEET Eligibility 2020 Подготовка
- NEET Syllabus
- Support
- Разрешение жалоб
- Служба поддержки
- Центр поддержки
- GSEB
- GSEB Syllabus
GSEB Образец
003 GSEB Books
- MSBSHSE Syllabus
- MSBSHSE Учебники
- MSBSHSE Образцы статей
- MSBSHSE Вопросы
- 9000
- AP 2 Year Syllabus
- MP Board Syllabus
- MP Board Образцы документов
- MP Board Учебники
- Assam Board Syllabus
- Assam Board
- Assam Board
- Assam Board Документы
- Bihar Board Syllabus
- Bihar Board Учебники
- Bihar Board Question Papers
- Bihar Board Model Papers
- Odisha Board
- Odisha Board
- Odisha Board
- ПСЕБ 9 0002
- PSEB Syllabus
- PSEB Учебники
- PSEB Вопросы и ответы
- RBSE
- Rajasthan Board Syllabus
- RBSE Учебники
- RBSE
- 000 RBSE
- 000 HPOSE
- 000 HPOSE
- 000
- 000
000 HPOSE
000 HPOSE
000
- 000 HPOSE
- 000
000 HPOSE
000 Контрольные документы
- JKBOSE Syllabus
- JKBOSE Образцы документов
- JKBOSE Образец экзамена
- TN Board Syllabus
9000 Papers 9000 TN Board Syllabus
9000 Книги
- Программа обучения JAC
- Учебники JAC
- Вопросы JAC
- Telangana Board Syllabus
- Telangana Board Textbook
- Telangana Board Textbook
- Telangana Board Textbook
- KSEEB
- KSEEB Syllabus
- KSEEB Model Question Papers
- KBPE
- KBPE Syllabus
- Учебники KBPE
- KBPE
0
- Вопросы к Правлению UP
9000 UPMS Board UPMS
- Совет по Западной Бенгалии
- Учебный план Совета по Западной Бенгалии
- Учебники по Совету по Западной Бенгалии
- Вопросы по Совету по Западной Бенгалии
- UBSE
- TBSE
- Гоа Совет
- MBSE
- Meghalaya Board
- Manipur Board
- Haryana Board
- Банковские экзамены
- Экзамены SBI
- Экзамены IBPS
- 10 Экзамены IBPS
- RbI Экзамены
- SSC JE
- SSC GD
- SSC CPO
- SSC CHSL
- SSC CGL
- Экзамены RRB
- RRB JE
- RRB NTPC
- RRB Экзамены ALP
- 9102
- RRB ALP
- 5
000 LIC ADO
- Class 1
- Class 2
- Class 3
- Вопросы по физике
- Вопросы по физике
- Вопросы по биологии
- Вопросы по математике
- Вопросы по естествознанию
- Вопросы для общего доступа
- Онлайн-обучение
- Домашнее обучение
- Полная форма
- Общая полная форма
- Физика
- Физика
- Биология Полные формы
- Полные формы обучения
- Полные формы банковского дела
- Полные формы технологий
- Физика
- CAT
- Программа BYJU CAT
- Программа CAT
- Экзамен CAT
- Бесплатная подготовка CAT
- Экзамен
- CAT4 2020 CAT
- Общая полная форма
- КУПИТЬ КУРС
- +919243500460
- Химия
- Органическая химия
- Неорганическая химия
- 00030003 Биохимия
- Химия
- Биохимия
- Химия
- Пищевая химия
- Статьи по химии
- Учебный план по химии
- Формулы химии
- Формулы химических соединений
- Различия между химией
- Химические реакции
- Химические реакции
- Химия
- Периодическая таблица
- Элементы периодической таблицы
- Периодичность в свойствах элементов
- Периодическая таблица Менделеева
- Современная периодическая таблица и закон
- Таблица элементов
- Электронная конфигурация элементов
- Периодическая энтальпия элементов
- Тенденции в энтальпии усиления электронов
- Октавы и триады Доберейнера Ньюланда
- Именованные реакции
- Конденсация альдола
- Реакция Канниццаро
- Реакция Финкельштиена
- Аллелирование
Фридел-аффтстиена Реакция Фольхарда-Зелинского
- Озонолиз
- Реакция Перкина
- Реакция Дильса-Альдера
- Закон Бойля
- Закон Авогадро
- Закон постоянной массы
- Закон постоянных пропорций 9000 9000 04
- Законы химического соединения
- Закон Кольрауша
- Закон Гей-Люссака
- Принцип Ауфбау
- Правило Марковникова
- Важные вопросы по классу 11 124
- 000 Важные вопросы по химии
Важные вопросы CBSE Chemistry
- Химия
- Термодинамика
- Удельная теплоемкость воды
.
Измерение удельной теплоемкости и теплопроводности графена на подложке и в подвешенном состоянии комплексным оптотермическим методом комбинационного рассеяния света
В последнее десятилетие наблюдается стремительный рост исследований двумерных (2D) материалов, представленных графеном, но исследования их теплофизических свойств все еще далеки от достаточных из-за экспериментальных проблем. Здесь мы сообщаем о первом измерении теплоемкости многослойного и монослойного графена как в поддерживаемой, так и в подвешенной геометрии.Их теплопроводность также была одновременно измерена с использованием комплексного рамановского оптотермического метода без необходимости знать лазерное поглощение. Для нагрева образцов использовались как непрерывные (CW), так и импульсные лазеры с учетом переменного радиуса лазерного пятна и длительности импульса, а также теплопроводности внутри подложки. Ошибка, связанная с поглощением лазерного излучения, была устранена путем сравнения измеренных комбинационным методом повышения температуры для различных радиусов пятна и длительностей импульсов.Теплопроводность и удельная теплоемкость были получены путем аналитического подбора отношений повышения температуры в зависимости от размера пятна и длительности импульса соответственно. Измеренная удельная теплоемкость составила около 700 Дж (кг · К) −1 при комнатной температуре, что соответствует теоретическим предсказаниям, а измеренные значения теплопроводности находились в диапазоне 0,84–1,5 × 10 3 Вт (м · К) −1 . Продемонстрированный здесь метод измерения может быть использован для исследования in situ и всестороннего изучения теплофизических свойств многих других появляющихся 2D материалов.
У вас есть доступ к этой статье
Подождите, пока мы загрузим ваш контент…
Что-то пошло не так. Попробуй снова?
.
