Свойства воды при температурах 0 — 100°С при атмосферном давлении. Плотность воды. Давление насыщенных паров воды (=saturation vapor pressure). Удельная энтальпия воды (=specific enthalpy). Теплоемкость воды (=specific heat). Объемная теплоемкость воды
| Адрес этой страницы (вложенность) в справочнике dpva.ru: главная страница / / Техническая информация / / Рабочие среды / / Вода, лед и снег (хладагент R718) / / Свойства воды при температурах 0 — 100°С при атмосферном давлении. Плотность воды. Давление насыщенных паров воды (=saturation vapor pressure). Удельная энтальпия воды (=specific enthalpy). Теплоемкость воды (=specific heat). Поделиться:
Поиск в инженерном справочнике DPVA. Введите свой запрос: | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Если Вы не обнаружили себя в списке поставщиков, заметили ошибку, или у Вас есть дополнительные численные данные для коллег по теме, сообщите , пожалуйста. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Коды баннеров проекта DPVA.ru Консультации и техническая | Проект является некоммерческим. Информация, представленная на сайте, не является официальной и предоставлена только в целях ознакомления. Владельцы сайта www.dpva.ru не несут никакой ответственности за риски, связанные с использованием информации, полученной с этого интернет-ресурса. Free xml sitemap generator | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ВОДА Теплоемкость — Зависимость от температуры и давления
Данные о зависимости теплоемкости воды от температуры и давления приведены в табл. 41 в табл. 42 приводятся данные о теплоемкости различных жидкостей.
[c.38]
Теплоемкость Ср с ростом температуры в зависимости от параметров состояния может возрастать или убывать. Зависимость Ср от температуры и давления для воды см. в п. 2.4.5.
[c.119]
Зависимость Ср от температуры и давления для воды см. в п. 2.4.5.
[c.119]
Тепловые характеристики. Удельная теплоемкость воды составляет 4180 Дж,/(кг- С) при 0°С. Она изменяется в зависимости от температуры и достигает минимума при +35°С. Удельная теплота плавления при переходе льда в жидкое состояние составляет 330 кДж/кг, удельная теплота парообразования — 2250 кДж/кг при нормальном давлении и температуре 100°С. Вследствие значительных величин теплоемкости и скрытой теплоты трансформации воды огромные ее объемы на поверхности Земли представляют собой аккумуляторы тепла. Эти же свойства воды обусловливают ее использование в промышленности в качестве теплоносителя. Тепловые характеристики воды являются одними из важнейших факторов термической стабильности биосферы. [c.6]
Значения удельного объема, энтальпии и энтропии воды и водяного пара в состояниях насыщения приведены в табл. I (в зависимости от температуры) и табл. II (в зависимости от давления), а величины их изобарной теплоемкости в этих состояниях — в табл.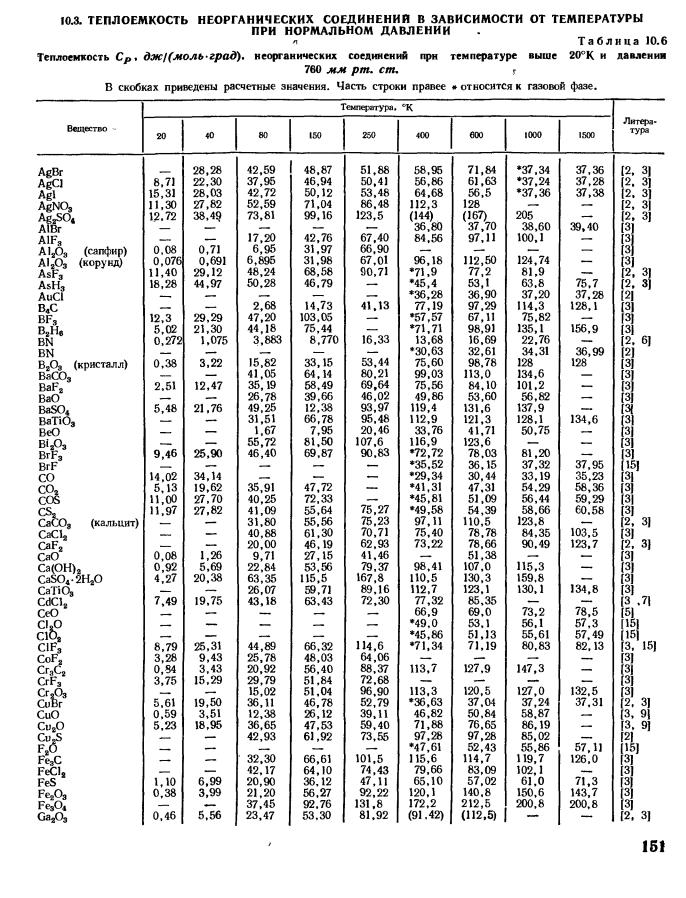 VI. В этой же таблице помещены и значения коэффициента поверхностного натяжения воды.
[c.13]
VI. В этой же таблице помещены и значения коэффициента поверхностного натяжения воды.
[c.13]
Теплоемкость воды (а в ккал/гсГ град) в зависимости от температур- 1 и давления [2″)) [c.38]
Теплоемкость морской воды в зависимости от солености и температуры (при атмосферном давлении) [c.296]
При составлении нелинейной модели использовались зависимости, связывающие давление, энтальпию, внутреннюю -энергию, плотность пара и воды на линии насыщения с температурой, а также зависимости плотности и теплоемкости раствора от температуры и концентрации. Данные по воде и пару аппроксимировались в интервале температур 55—140° С полиномами с погрешностью, не превышающей 5% (аппроксимация проводилась методом наименьших квадратов). Для моделирования нелинейной системы дифференциальных уравнений выпарной установки составлена программа применительно к машине Раздан . [c.108]
Теплоемкость воды в зависимости от температуры (от О до 140° С) и давления-до 300 ama по Коху выражается следующим образом
[c. 191]
191]
Представление о характере зависимости теплоемкости от / и р дает рис. 3-3, на котором приведены данные для воды и водяного пара, В сверхкритической области теплоемкость Ср при некоторых значениях температуры, зависящих от давления, проходит через максимум. В критической точке Ср = оо. При р>ркр значения Ср в точках максимума убывают с ростом давления. Вблизи точек максимума теплоемкость может изменяться в десятки раз в узком интервале температуры и давления. [c.33]
Теплоемкость Ср может и возрастать, и убывать с ростом температуры в зависимости от параметров состояния. При этом понижение с , при возрастании температуры обычно сменяется ростом при дальнейшем повышении температуры. В качестве иллюстрации на рис. 6-7 приведен график зависимости теплоемкости воды от температуры при различных давлениях. Как видно из этого графика, теплоемкость воды имеет минимум при температуре около 20° С. Из этого графика видно также, что с приближением к линии насыщения (значения на изобарах в точках их пересечения с линией насыщения соединены пунктирной линией) теплоемкость заметно возрастает.
[c.169]
Из этого графика видно также, что с приближением к линии насыщения (значения на изобарах в точках их пересечения с линией насыщения соединены пунктирной линией) теплоемкость заметно возрастает.
[c.169]
Термодинамика системы воздух — вода — пар проста поэтому такая система удобна для иллюстрации задач массопереноса, в которых в L-состоянии находится жидкость, а в О- и оо-состояниях — газ. Мы рассмотрим сначала расчет этой системы, затем — систем с химическими реакциями и, наконец, некоторые специальные случаи. Если считать газ совершенным и для определения парциальных давлений использовать только закон Гиббса—Дальтона, то термодинамическое состояние рассматриваемой системы однозначно определяется заданием следующих параметров кривой зависимости давления насыщенных паров воды от температуры, скрытой теплоты испарения Н2О при некоторой определяющей температуре, а также удельных теплоемкостей воды, водяного пара и воздуха. [c.389]
В области докритических давлений ниже линии насыщения, где существует только жидкая фаза Н2О, повышение температуры сопровождается снижением вязкости, плотности и диэлектрической проницаемости воды теплоемкость при постоянном давлении Ср несколько возрастает. При температурах выше точки насыщения ts, где существу ет только газообразная фаза Н2О, перегрев пара сопровождается снижением его плотности и теплоемкости Ср и незначительным увеличением вязкости. На линии насыщения существуют обе фазы — пар и вода, различающиеся по плотности, вязкости, диэлектрической проницаемости и другим показателям. Зависимость плотности пара и воды и их диэлектрической проницаемости от давления на линии насыщения по казана на рис. В.6. Из этого рисунка видно, что разность между плот-
[c.16]
При температурах выше точки насыщения ts, где существу ет только газообразная фаза Н2О, перегрев пара сопровождается снижением его плотности и теплоемкости Ср и незначительным увеличением вязкости. На линии насыщения существуют обе фазы — пар и вода, различающиеся по плотности, вязкости, диэлектрической проницаемости и другим показателям. Зависимость плотности пара и воды и их диэлектрической проницаемости от давления на линии насыщения по казана на рис. В.6. Из этого рисунка видно, что разность между плот-
[c.16]
Приведены таблицы значений удельного объема, энтальпии, энтропии, изобарной теплоемкости, скорости звука, поверхностного натяжения, динамической вязкости, теплопроводности и числа Прандтля для воды и водяного пара, рассчитанных по уравнениям, рекомендованным Международной ассоциацией по свойствам воды и водяного пара для применения в промышленных расчетах. Таблицы термодинамических свойств охватывают область параметров до температуры 800 °С и давления 100 МПа (до 1000 °С при давлениях ниже 10 МПа), включая состояния насыщения. Для этой же области параметров даны и значения динамической вязкости. Предельная температура области применения данных о теплопроводности в зависимости от давления — от 800 до 500 °С.
[c.2]
Для этой же области параметров даны и значения динамической вязкости. Предельная температура области применения данных о теплопроводности в зависимости от давления — от 800 до 500 °С.
[c.2]
Этим способом можно для всех индивидуальных веществ установить зависимость энтропии от температуры, определив теплоемкости и энтальпии фазовых переходов во всем интервале температур, допустимом для измерений вплоть до непосредственной близости к абсолютному нулю. При этом остается неопределенной ее константа интегрирования. Обычно ее выбирают по соглашению из соображений удобства. В таблицах водяного пара, в частности, энтропия жидкой воды при температуре 0°С и соответствующем давлении насыщения принята за нуль. Для газов исходным состоянием обычно считается 0° С и 1 физ. ат. В случае аммиака и углекислоты удельную энтропию жидкости при 0° С и соответствующем давлении насыщения принимают равной I ккал/кг град, для того чтобы избежать отрицательных значений энтропии в важной для холодильной техники области отрицательных температур. Неопределенность константы интегрирования для энтропии устраняется только теоремой Нернста, которую мы рассмотрим далее.
[c.327]
Неопределенность константы интегрирования для энтропии устраняется только теоремой Нернста, которую мы рассмотрим далее.
[c.327]
Зависимость теплоемкости жидкостей от давления при температурах много меньших, чем критические, крайне мала, и в большинстве случаев ею можно пренебречь. Для воды при комнатной температуре теплоемкость Ср уменьшается на 5% при увеличении давления от 0,1 до 100 МПа (от 1 до 1000 кгс/см ).
[c.172]
Водный теплоноситель. Вода — наиболее дешевый и распространенный жидкий теплоноситель. Обладая хорошим сочетанием теплофизических свойств теплопроводности, удельной теплоемкости, плотности и вязкости, вода способна отводить большое количество тепла от поверхности нагрева реактора даже при небольшой скорости. Увеличение скорости воды, например, от 0,3 до 5 м/с повышает коэффициент теплоотдачи в 10 раз. Вода радиационно устойчива и требует умеренного расхода энергии на транспорт по контуру. Основной недостаток водного теплоносителя — низкая температура насыщенного пара и ее медленный рост с повышением давления это ограничивает рабочее давление перед турбиной (7—10 МПа). Малая зависимость плотности воды от давления ограничивает возможности самозащиты первого контура при повышении в нем давления поэтому в первом контуре предусматривают газовые компенсаторы объема. Вода — коррозионно-активное вещество и, взаимодействуя с конструкционными материалами, загрязняется продуктами коррозии. Вода также хороший растворитель минеральных примесей. Наличие в воде первого контура продуктов коррозии и минеральных примесей при прохождении через реактор приводит к образованию долгоживущих изотопов, распространяющихся вместе с водным теплоносителем по контуру, что затрудняет ревизию и ремонт оборудования.
[c.340]
Малая зависимость плотности воды от давления ограничивает возможности самозащиты первого контура при повышении в нем давления поэтому в первом контуре предусматривают газовые компенсаторы объема. Вода — коррозионно-активное вещество и, взаимодействуя с конструкционными материалами, загрязняется продуктами коррозии. Вода также хороший растворитель минеральных примесей. Наличие в воде первого контура продуктов коррозии и минеральных примесей при прохождении через реактор приводит к образованию долгоживущих изотопов, распространяющихся вместе с водным теплоносителем по контуру, что затрудняет ревизию и ремонт оборудования.
[c.340]
Особенно сложна проблема учета переменности свойств теплоносителя при анализе и расчете теплообмена в околокритической области состояния, где теплофизические свойства среды резко и своеобразно изменяются в зависимости от температуры и давления удельная теплоемкость, число Прандтля и коэффициент термического расширения имеют резко выраженные максимумы, немонотонно изменяются теплопроводность и вязкость, резко изменяется плотность среды. При этом коэффициент теплоотдачи зависит от плотности теплового потока или, точнее, от соотношения плотности теплового потока и массовой скорости теплоносителя, причем наряду с нормальными режимами теплообмена, когда температура стенки монотонно (при = onst) изменяется вдоль потока в соответствии с изменением температуры теплоносителя, наблюдаются и так называемые режимы ухудшенной (улучшенной) теплоотдачи, при которых температура стенки трубы имеет немонотонный (при ухудшенных режимах — пиковый) характер изменения. К настоящему времени предложено множество эмпирических формул и расчетных схем. Для расчета теплоотдачи при вязкостно-инерционном течении однофазных теплоносителей с околокри-тическими параметрами (т е. в отсутствие влияния естественной конвекции) широкое распространение получила формула [46], основанная на данных опытов с водой и диоксидом углерода. Однако применима она к нормальным и лишь частично к ухудшенным режимам теплоотдачи.
[c.222]
При этом коэффициент теплоотдачи зависит от плотности теплового потока или, точнее, от соотношения плотности теплового потока и массовой скорости теплоносителя, причем наряду с нормальными режимами теплообмена, когда температура стенки монотонно (при = onst) изменяется вдоль потока в соответствии с изменением температуры теплоносителя, наблюдаются и так называемые режимы ухудшенной (улучшенной) теплоотдачи, при которых температура стенки трубы имеет немонотонный (при ухудшенных режимах — пиковый) характер изменения. К настоящему времени предложено множество эмпирических формул и расчетных схем. Для расчета теплоотдачи при вязкостно-инерционном течении однофазных теплоносителей с околокри-тическими параметрами (т е. в отсутствие влияния естественной конвекции) широкое распространение получила формула [46], основанная на данных опытов с водой и диоксидом углерода. Однако применима она к нормальным и лишь частично к ухудшенным режимам теплоотдачи.
[c.222]
В книге Даны новые значения теплоемкости пара в идеальном состоянии, таблицы средних теплоемкостей пара й таблицы значений истинных теплоеМкортей при постоянном давлении и при постоянном объеме, вязкости и теплопроводности воды и водяного пара и их зависимости от температуры и давления. [c.2]
[c.2]
Примечание. При рассматриваемых давлениях и температурах следует учитывать зависимость теплоемкости воды от температуры и давления. Поэтому температуру воды на выходе нужно определять по измененню энтальпии воды по длине канала [c.94]
В закритической области вещество находится в однородном состоянии, и в нем отсутствует резкое разделение на отдельные фазы, что имеет место при пересечении пограничной кривой вдали от критической точки. Различие между жидкостью и паром в этой области носит лишь количественный характер, поскольку между ними можно осуществить непрерывный переход без выделения или поглощения скрытой теплоты изменения агрегатного состояния. Однако в указанных переходах непрерывный ряд микроскопических однородных состояний содержит области максимальной микроскопической неоднородности флуктуац ионного характера. Существование такой микроскопической неоднородности связано с падением термодинамической устойчивости первоначальной фазы и с возникновением внутри >нее островков более устойчивой фазы.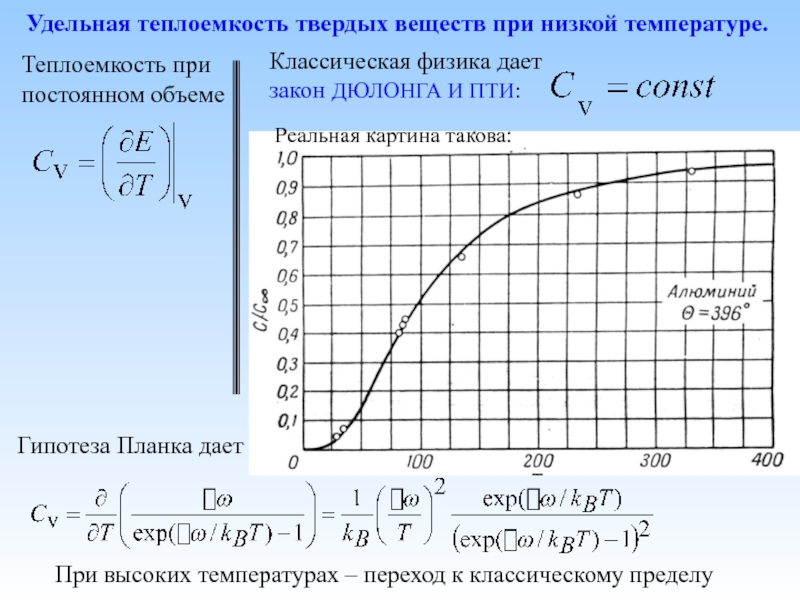 Указанная внутренняя перестройка вещества, несмотря на свою нелрерывность, имеет узкие участки наибольшего сосредоточения, которые обусловливают появление резких скачков теплоемкости, сжимаемости, коэффициента объемного расширения, вязкости и других свойств вещества. Эти явления демонстрировались рис. 1-5, где был показан характер изменения критерия Прандтля для воды, и перегретого водяного пара от температуры и давления, и рис. 1-6 — для кислорода в зависимости от температуры при закритическом давлении. Из графиков следует, что при около- и закритиче-ских давлениях наряду с областями резкого изменения физических параметров имеются области, где они изменяются с температурой незначительно. При высоких давлениях в области слабой зависимости тепловых параметров от температуры теплоотдача подчиняется обычным критериальным зависимостям. В этом случае при проведении опытов можно не опасаться применения значительных температурных перепадов между стенкой и потоком жидкости, обработка опытных данныл также не
[c.
Указанная внутренняя перестройка вещества, несмотря на свою нелрерывность, имеет узкие участки наибольшего сосредоточения, которые обусловливают появление резких скачков теплоемкости, сжимаемости, коэффициента объемного расширения, вязкости и других свойств вещества. Эти явления демонстрировались рис. 1-5, где был показан характер изменения критерия Прандтля для воды, и перегретого водяного пара от температуры и давления, и рис. 1-6 — для кислорода в зависимости от температуры при закритическом давлении. Из графиков следует, что при около- и закритиче-ских давлениях наряду с областями резкого изменения физических параметров имеются области, где они изменяются с температурой незначительно. При высоких давлениях в области слабой зависимости тепловых параметров от температуры теплоотдача подчиняется обычным критериальным зависимостям. В этом случае при проведении опытов можно не опасаться применения значительных температурных перепадов между стенкой и потоком жидкости, обработка опытных данныл также не
[c. 205]
205]
Погрешность значений. теплоемкости охлаждающёй воды бср,в составляет около 0,1 % Однако здесь следует обратить внимание на то, что теплоемкость воды при атмосферном давлении несколько изменяется в зависимости от температуры. Так, пр и температуре 10 X Ср,в=4,192, а при 20°С соответственно Ср,в=4,182 кДж/(кг-К), т. е. изменение теплоемкости составляет 0,25 %. Поэтому при точном измерении энтальпии, если опыт проводится при значительном подогреве охлаждающей воды i»—t, количество теплоты, полученной 1 кг охлаждающей воды, равно
[c.205]
Величину Y — соотношение теплоемкостей при постоянном давлении и постоянном объеме— довольно трудно определить для многоатомных молекул, таких, например, как молекула воды (HjO), и это соотношение следует найти эмпирическим путем. Для водяного пара в интервале температур, близких к 0°С, оно составляет около 1,05. Зависимость температуры от парциального давления приводит к тому, что, когда смесь воздуха с водяным паром охлаждается при подъеме в атмосферу, количество водяного пара в смеси должно уменьшиться, чтобы сохранилось соответствующее парциальное давление. Но, поскольку при этом значения температур и давлений лежат за пределами тройной точки, водяной пар вымерзает и превращается в ледяные кристаллы. Вот отчего тропопаузный минимум температуры часто называют ледяной ловушкой . Температура воздуха над тропопаузой снова
[c.302]
Но, поскольку при этом значения температур и давлений лежат за пределами тройной точки, водяной пар вымерзает и превращается в ледяные кристаллы. Вот отчего тропопаузный минимум температуры часто называют ледяной ловушкой . Температура воздуха над тропопаузой снова
[c.302]
Характер нижней пограничной кривой на диаграмме T — s напоминает логарифмическую кривую, которая идет в области довольно высоких температур это видно из приближенного уравнения (234). Однако при температурах, близких к критической, это уравнение становится неверным, так как теплоемкость кипящей воды будет существенно меняться в зависимости от температуры. Поэтому характер протекания нижней погранично кривой при этих температурах будет другим. Изобары жидкости вплоть до давлений, близких к критическому, практически совпадают с нижней пограничной кривой (линия аЪ, рис. 110). Поэтому для не очень точных расчетов можно считать, что нижняя пограничная кривая является также и совокупностью изобар жидкости (точка а совпадает с точко Со). В области между верхней и нижней пограничными
[c.176]
В области между верхней и нижней пограничными
[c.176]
Вода обладает многими специфическими свойствами, имеющими ярко выраженный аномальный характер. Все они — следствие особенностей структуры воды и развитости в ней водородных связей. Плавление твердой воды — льда — сопровождается не расширением, а сжатием, а при замерзании воды объем льда значительно увеличивается. Как известно, подавляющее большинство веществ при плавлении расширяется, а при затвердевании, наоборот, уменьшает свой объем. Аномально также влияние температуры на изменение плотности воды при росте температуры от 273 до 277 К плотность увеличивается, при 277 К она достигает максимальной величины, и только при дальнейшем повышении температуры плотность воды начинает уменьшаться. Зависимость теплоемкости воды от температуры имеет экстремальный характер. Минимальная теплоемкость достигается при температуре 308,5 К и вдвое превышает теплоемкость льда, а при плавлении других твердых тел тегаюемкость изменяется незначительно. Удельная теплоемкость воды аномально велика, она равна 4,2 Дж/(г К). Вязкость воды в отличие от вязкости других веществ растет с повьцнением давления в интервале температур от 273 до 303 К. Вода имеет температуру плавления и кипения, значитель-
[c.186]
Удельная теплоемкость воды аномально велика, она равна 4,2 Дж/(г К). Вязкость воды в отличие от вязкости других веществ растет с повьцнением давления в интервале температур от 273 до 303 К. Вода имеет температуру плавления и кипения, значитель-
[c.186]
Наибольшее значение термического КПД цикла может быть получено при максимально высоких температурах подводимой теплоты, что подтверждается проведенным выше анализом зависимости КПД паровых циклов от параметров рабочего агента. Однако для создания реальных циклов и реализации указанных преимуществ требуются особые природные свойства рабочего тела, так как в отличие от цикла Карно в цикле Ренкина качество рабочего тела существенно влияет на термический КПД установки. Наиболее часто в качестве рабочего тела в современных энергетических паровых установках испольаус-ся водяной пар. Однако вода по своим свойствам не может удовлетворять всем требованиям, предъявляемым к рабочим телам о целью увеличения КПД. Прежде всего она имеет низкую критическую темпера-туру (Т р 647. 15 К) и при этом достаточно большое критическое давление р р = 22,219 МПа. При таких физических свойствах воды и водяного пара при росте температуры перегрева не удается существенно повысить среднюю температуру подводимой теплоты. Вода имеет слишком большое значение удельной теплоемкости, а это, как
[c.318]
15 К) и при этом достаточно большое критическое давление р р = 22,219 МПа. При таких физических свойствах воды и водяного пара при росте температуры перегрева не удается существенно повысить среднюю температуру подводимой теплоты. Вода имеет слишком большое значение удельной теплоемкости, а это, как
[c.318]
Теплоемкость рабочего тела сравнительно мало зависит от давления (в пределах ожидаемых из1Мбнений в нестационарном режиме), но заметно изменяется при изменении температуры, особенно если состояние потока близко к насыщению при доиритичеаком давлении или к области фазового перехода при шерхйритическом давлении. Удельная теплоемкость воды Св с повышением температуры возрастает, а пара—падает. Неучет зависимости n=f t) может существенно исказить температурную информацию как в динамике, так и в статике. [c.137]
Пример 2. Построение графика зависимости удельной изобарной теплоемкости воды и водяного пара от давления и температуры в Math ad Professional. [c.129]
[c.129]
Удельная теплоемкость паров — Справочник химика 21
Удельная теплота конденсации бензола при 50°С равна —414,7 Дж/г и при 80°С —397,1 Дж/г. Удельная теплоемкость жидкого бензола в этом интервале температур 1,745 Дж/(г-К). Вычислить удельную теплоемкость паров бензола в этом интервале температур и рассчитать расхождение между полученным и табличным значением 1,047 Дж/(г-К). [c.46]
Наиболее важные физические константы метанола представлены в табл. 1 [1]. В табл. 2 приведены давления паров метанола при различных температурах, а в табл. 3 — плотности водных растворов метанола при 25°С. В табл. 4 дана удельная теплоемкость паров метанола, а в табл. 5 — температуры замерзания его водных растворов. Вязкости смесей метанола с водой представлены в табл. 6, а бинарные азеотропные смеси метанола — в табл. 7. [c.211]
При конденсации перегретого пара необходимо учитывать теплоту перегрева Д/пер = /т — = Ср Т — Та), где /т — удельная энтальпия перегретого пара, соответствующая температуре перегрева Г /н —удельная энтальпия пара при температуре насыщения Гн Ср — удельная теплоемкость пара при постоянном давлении. [c.145]
[c.145]
Определите изменение энтропии, если 100-10 кг воды, взятой при 273 К, превращается в пар при 390 К. Удельная теплота испарения воды при 373 К равна 2263,8-10 Дж/кг удельная теплоемкость жидкой воды 4,2 Дж/(кг-К) удельная теплоемкость пара при постоянном давлении 2,0-10 Дж/(кг-К). [c.89]
Удельная теплоемкость (пара), кал/(г-°С) [c.182]
В ЭТИХ уравнениях С и С. —удельные теплоемкости пара и жидкости, дж/кг град г — теплота испарения, дж/кг. [c.368]
Удельная теплоемкость паров топлив зависит от их состава, температуры и давления. При 0°С она примерно одинакова для всех моторных топлив и составляет i n. =l,5-i-l,7 кДж/(кг-К). При других температурах теплоемкость паров топлив может быть определена [в кДж/ кг-К)] по формуле [c.104]
Здесь Сгт и С,к — средние удельные теплоемкости пара и жидкости, Дж/(кг-К) 11 и /нтемпература насыщения пара, К г — удельная теплота парообразования, Дж/кг.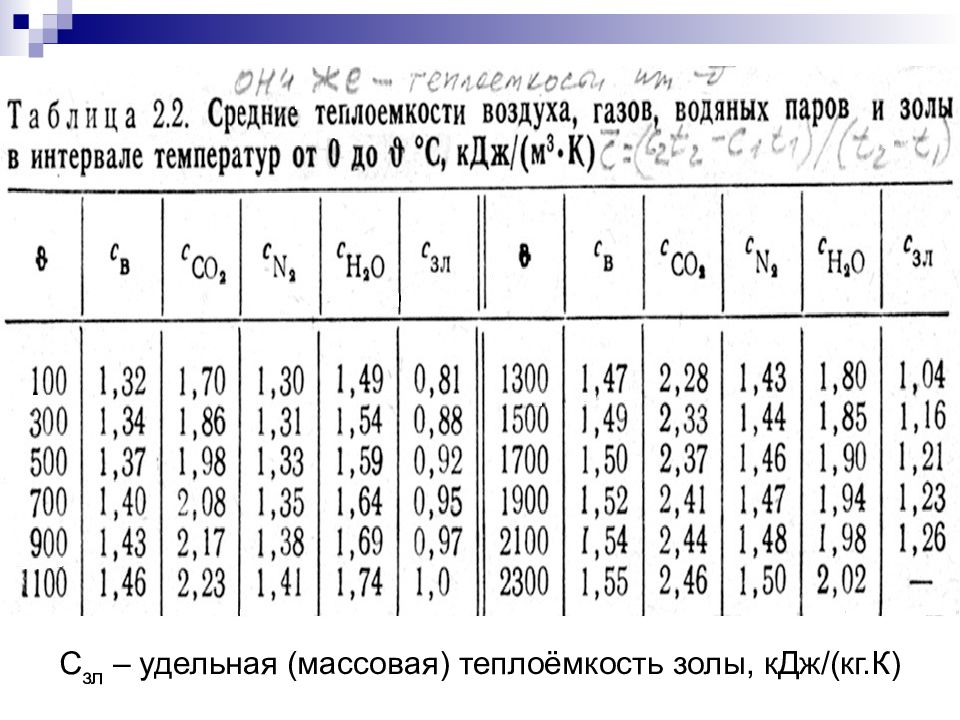 [c.122]
[c.122]
Обычно одновременно с измерением теплоты испарения измеряется удельная теплоемкость пара. Как отмечалось в разд. 2.10, зная зависимость теплоемкости Ср от давления, можно получить данные по вириальным коэффициентам. В частности, вторая производная В может быть получена из соотношения [c.113]
Низшая теплота сгорания соответствует следующему условию содержащийся в продуктах сгорания водяной пар охлаждается от 100 до 20 °С. При этом высвобождается удельное количество тепла, равное 1-2,0087 (100—20) = 160,7 кДж/кг, где 2,0087 кДж/(кг-°С)—удельная теплоемкость паров воды. [c.55]
Удельная теплоемкость паров при 25 °С и атмосферном давлении, кДж/(кг К) 0,734 0,724 0,745 0,852 [c.41]
Мольная теплота испарения бензола при 0° С 7810 кал/моль. Средняя удельная теплоемкость паров бензола в пределах от О до 80° С равна 0,299 кал/град-г.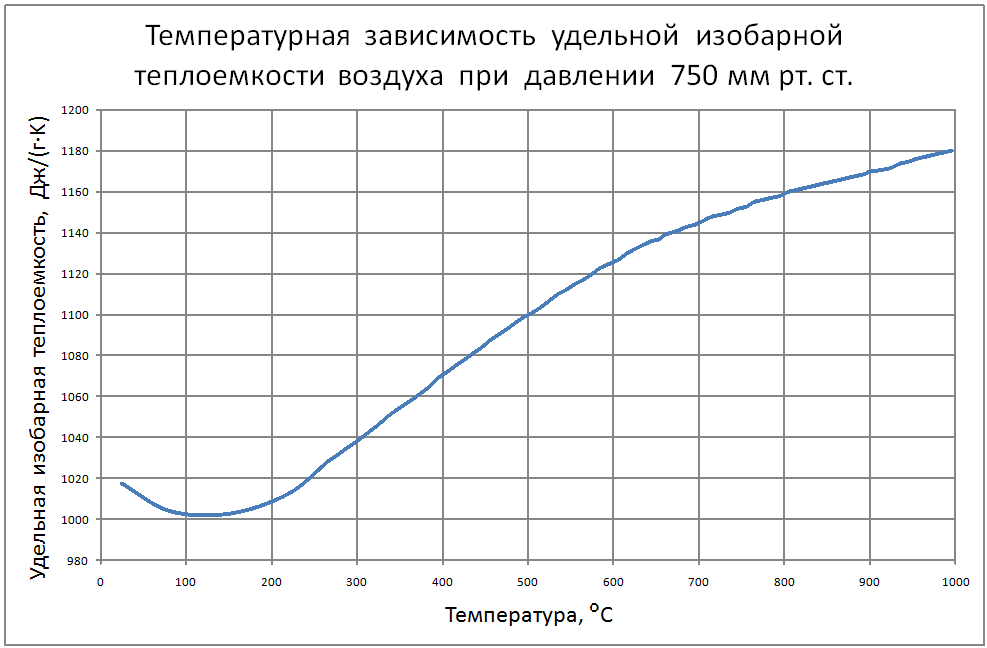 Средняя удельная теплоемкость жидкого бензола в том же температурном интервале 0,411 кал/град-г. Определить. мольную теплоту испарения бензола при 80° С. Ответ. 7093 кал/моль. [c.88]
Средняя удельная теплоемкость жидкого бензола в том же температурном интервале 0,411 кал/град-г. Определить. мольную теплоту испарения бензола при 80° С. Ответ. 7093 кал/моль. [c.88]
Средняя удельная теплоемкость паров бензола в пределах от О до 80° С 0,411 кал/град-г. Средняя мольная теплоемкость паров ацетилена в том же температурном интервале 10,43 кал/град-моль. Теплота реакции [c.88]
Удельная теплоемкость паров при 25 °С и атмосферном давлении, кДж/(кг К) Давление паров насыщенной жидкости при 25 °С, кПа (абс.) [c.50]
Здесь с — удельная теплоемкость сухого газа, Дж/(кг К) — удельная теплоемкость пара, Дж/(кг К). [c.216]
Перегретый водяной пар имеет ряд существенных преимуществ перед другими теплоносителями, используемыми в качестве агентов конвективной сушки [89] возможность использования вторичного пара и сохранение основного пара в контуре рециркуляции (в связи с этим высокий энергетический к.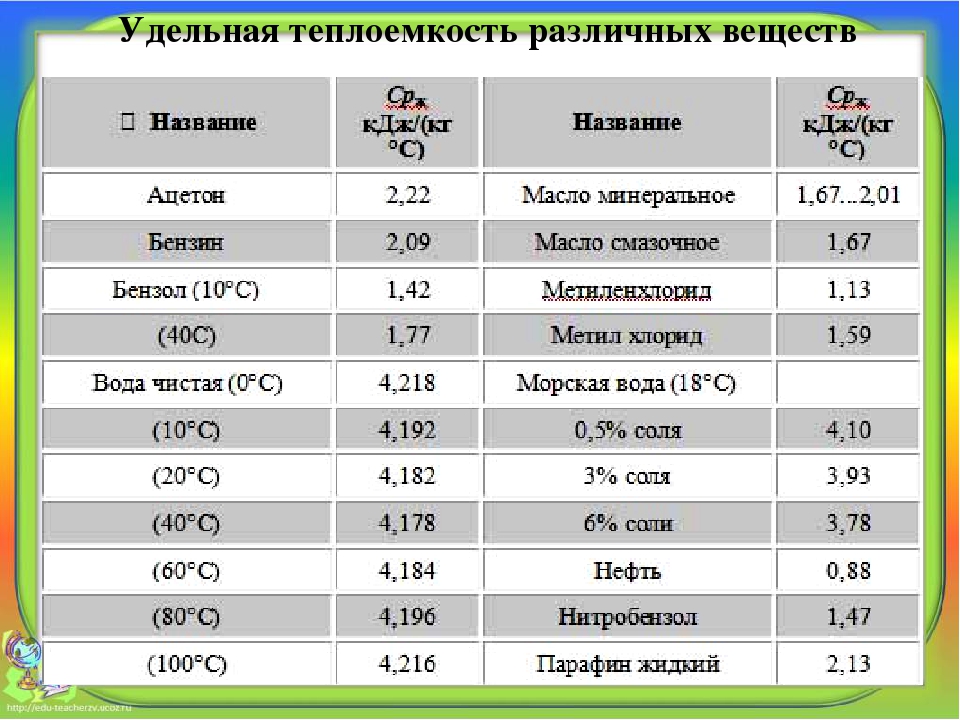 п.д. процесса) уменьшение требуемого количества пара в контуре циркуляции (так как удельная теплоемкость пара в два раза выше теплоемкости воздуха) более высокая интенсивность сушки за счет интенсификации фазового испарения (испарение влаги происходит в режиме кипения) отсутствие кислорода в сушильной среде, что позволяет значительно повысить температуру сушки. [c.109]
п.д. процесса) уменьшение требуемого количества пара в контуре циркуляции (так как удельная теплоемкость пара в два раза выше теплоемкости воздуха) более высокая интенсивность сушки за счет интенсификации фазового испарения (испарение влаги происходит в режиме кипения) отсутствие кислорода в сушильной среде, что позволяет значительно повысить температуру сушки. [c.109]
Удельная теплоемкость паров сероуглерода [34] [c.13]
Необходимые данные взять из примера ХП.2 принять, что удельная теплоемкость паров равна 0,72 ккал/(кг °С), а скрытая теплота парообразования нефтепродуктов составляет 80 ккал/кг. [c.353]
Если данные об удельной теплоемкости паров исследуемого азеотропа отсутствуют, величина может быть принята [c.175]
Как и во всякой химической реакции скорость горения определяется изменением во времени концентрации реагирующих веществ или образующихся продуктов реакции. Она зависит от химических и физических свойств реагирующих веществ, а также от условий протекания реакции (теплота сгорания, теплота парообразования, удельная теплоемкость паров топлива, температура, объем и поверхность реакционного пространства, давление и др. ). [c.300]
). [c.300]
НОМОГРАММЫ ДЛЯ РАСЧЕТА УДЕЛЬНОЙ ТЕПЛОЕМКОСТИ ПАРОВ [c.115]
Определить истинную изобарную удельную теплоемкость паро для нефтепродукта удельного веса dJs=0,780 при температуре i = 300° и атмосферном давлении. [c.71]
Удельная теплоемкость паров кап/(г °С) 0,161 (60°С) 0,170 [c.167]
Ср» —удельная теплоемкость пара, кДж/(кг-К) г — удельная теплота испарения, кДж/кг [c.18]
Сп=1,97-10 — удельная теплоемкость пара, дж1кг-град (в условиях сушки может быть принята постоянной). [c.738]
Пэтрик и Кемпер[ з] пришли к аналогичному выводу на основании измерений удельных теплоемкостей. Они нользовалисьметодом теплопроводности Эндрюса[в ] и измеряли удельные теплоемкости паров воды, нафталина, бензола и / -нитротолуола, адсорбированных на силикагеле. Пример полученных резз льтатов приведен на рис. 150, Ординаты пропорциональны теплоемкостям системы силикагель — нафталин, абсциссы пропорциональны температурам.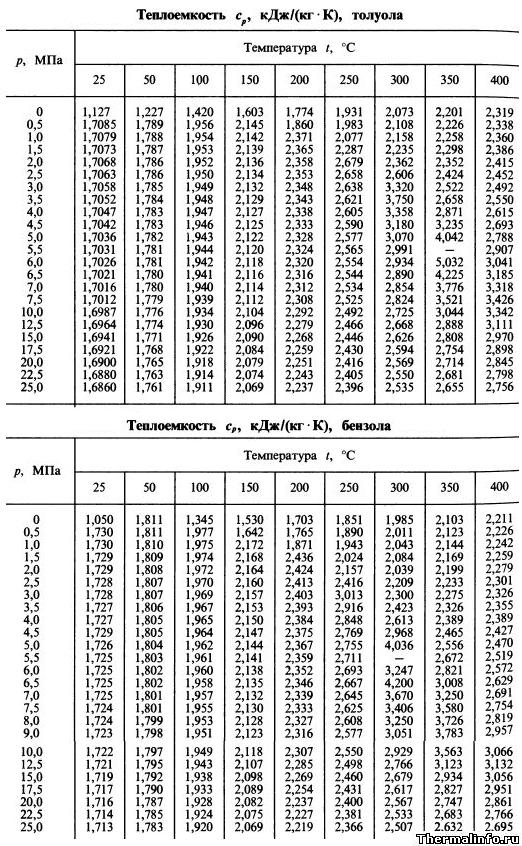 Малый горб на опытной кривой получается вследствие плавления избытка [c.602]
Малый горб на опытной кривой получается вследствие плавления избытка [c.602]
Физические свойства воды :: HighExpert.RU
Вода (обычная) — вещество, описываемое химической формулой H2O, самое распространенное соединение на земле, состоящее из двух атомов водорода и одного атома кислорода, растворитель минеральных солей.
Плотность воды при различной температуре
| Температура воды | Плотность воды |
| оС | кг/м3 |
| 0 | 999,9 |
| 5 | 1000 |
| 10 | 999,7 |
| 20 | 998,2 |
| 30 | 995,7 |
| 40 | 992,2 |
| 50 | 988,1 |
| 60 | 983,2 |
| 70 | 977,8 |
| 80 | 971,8 |
| 90 | 965,3 |
| 100 | 958,4 |
Динамическая и кинематическая вязкость воды при различной температуре
| Температура | Динамическая вязкость, μ | Кинематическая вязкость, ν |
| оС | (Н • c/м 2) • 103 — [сПуаз] | м2/с • 106 — [сСтокс] |
| 0 | 1,787 | 1,787 |
| 5 | 1,519 | 1,519 |
| 10 | 1,307 | 1,307 |
| 20 | 1,002 | 1,004 |
| 30 | 0,798 | 0,801 |
| 40 | 0,653 | 0,658 |
| 50 | 0,547 | 0,658 |
| 60 | 0,467 | 0,475 |
| 70 | 0,404 | 0,413 |
| 80 | 0,355 | 0,365 |
| 90 | 0,315 | 0,326 |
| 100 | 0,282 | 0,294 |
Основные физические свойства воды при различной температуре
| Температура | Плотность, ρ | Удельная теплоёмкость, Cp | Коэффициент температурного линейного расширения, α | Число Прандтля, Pr |
| оС | кг/м3 | кДж / (кг • К) | (1 / K) x 103 | — |
| 0 | 999,9 | 4,217 | -0,07 | 13,67 |
| 20 | 998,2 | 4,182 | 0,207 | 7,01 |
| 40 | 992,1 | 4,179 | 0,385 | 4,34 |
| 60 | 983,2 | 4,185 | 0,523 | 2,99 |
| 80 | 971,8 | 4,197 | 0,643 | 2,23 |
| 100 | 958,4 | 4,216 | 0,752 | 1,75 |
Температура кипения воды в зависимости от давления
1,013 бар
1,379 бар
2,068 бар
2,758 бар
3,585 бар
4,826 бар
6,205 бар
7,929 бар
10,34 бар
15,51 бар
Формулы физических свойств воды
При проведении инженерных расчетов удобнее использовать приближённые формулы для определения физических свойств воды⋆.
Плотность воды
⋆ [ кг/м3 ]
Теплоёмкость воды
⋆ [ Дж/(кг • К) ]
Теплопроводность воды
⋆ [ Вт/(м • K) ]
Динамическая вязкость воды
[ Па • c ]
Кинематическая вязкость воды
⋆ [ м2/с ]
Температуропроводность воды
⋆ [ м2/с ]
Число Прандтля воды
[ — ]
⋆ Приближённые формулы физических свойств воды получены авторами настоящего сайта.
Размерность величин: температура — К (Кельвин).
Приближённые формулы действительны в диапазоне температур воды от 283 К до 373 К.
7.2: Удельная теплоемкость и скрытая теплоемкость воды
Удельная теплоемкость
Материалы различаются по своей способности накапливать тепловую энергию. Например, такой материал, как медь, нагревается намного быстрее, чем вода или дерево. Удельная теплоемкость является мерой энергии, необходимой для нагрева 1 грамма вещества на 1°C . Удельная теплоемкость записывается в « калорий» для «массы в граммах » (и «джоулей в кг»).
Например, такой материал, как медь, нагревается намного быстрее, чем вода или дерево. Удельная теплоемкость является мерой энергии, необходимой для нагрева 1 грамма вещества на 1°C . Удельная теплоемкость записывается в « калорий» для «массы в граммах » (и «джоулей в кг»).
На рис. 7.11 удельная теплоемкость различных металлов сравнивается с удельной теплоемкостью льда, воды и пара.Для нагрева воды требуется значительно больше энергии, чем для других материалов, включая лед и пар. Из-за высокой удельной теплоемкости воды океаны способны накапливать огромное количество энергии солнечного нагрева. Тепло, поглощаемое в экваториальных районах, может переноситься на большие расстояния и переноситься океанскими течениями, прежде чем высвобождается в полярных регионах.
Рисунок 7.11. Сравнение удельной теплоемкости различных веществ со льдом, паром и жидкой водой.
Высокая скрытая теплоемкость воды
Когда любой материал нагревается до температуры, при которой он изменяет состояние (превращается из твердого в жидкое или из жидкого в газообразное), температура будет оставаться неизменной до тех пор, пока весь материал не изменит свое состояние.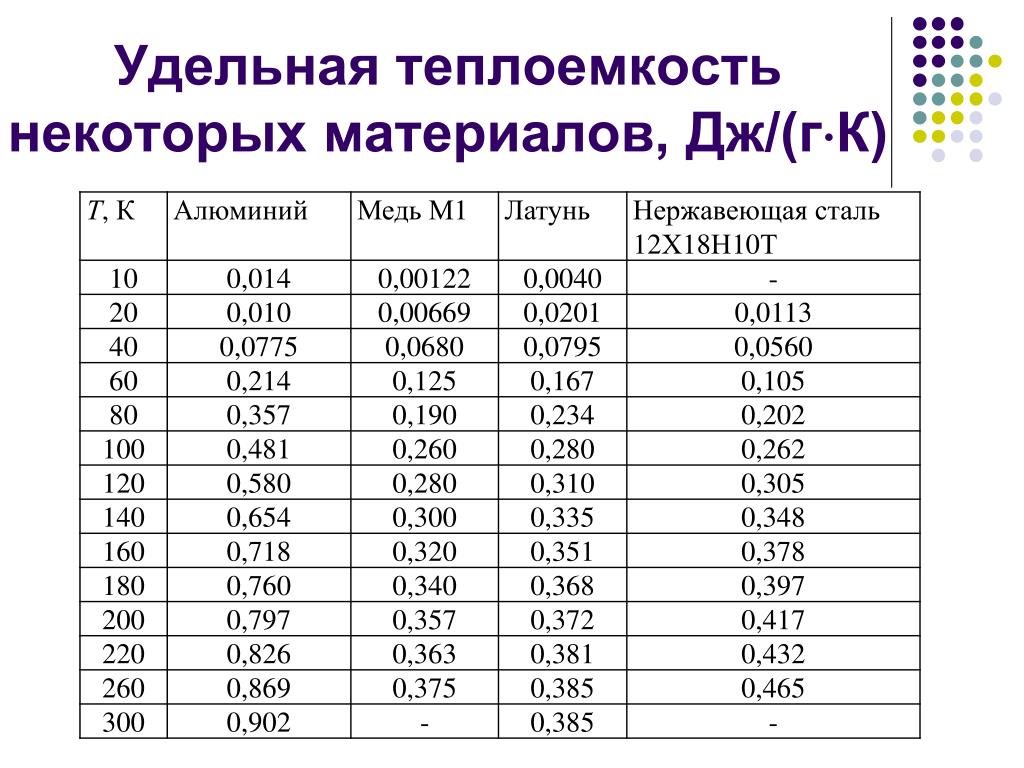 Поскольку для преобразования вещества из одного физического состояния в другое (твердое в жидкое или жидкое в газообразное) требуется больше энергии, эти переходы требуют большего количества энергии. Скрытая теплота — это теплота, необходимая (измеряемая в сожженных калориях) для превращения твердого вещества в жидкость или пар или жидкости в пар, без изменения температуры . Например, кастрюля с водой на плите будет постепенно нагреваться до тех пор, пока температура воды не приблизится к 212° F (или 100° C) — она будет оставаться при этой температуре, пока вся вода не выкипит.То же самое верно, как вода замерзает. Когда вода остынет, она достигнет 32°F (или 0°C) и будет оставаться при этой температуре до тех пор, пока вся вода не замерзнет (рис. 7.12).
Поскольку для преобразования вещества из одного физического состояния в другое (твердое в жидкое или жидкое в газообразное) требуется больше энергии, эти переходы требуют большего количества энергии. Скрытая теплота — это теплота, необходимая (измеряемая в сожженных калориях) для превращения твердого вещества в жидкость или пар или жидкости в пар, без изменения температуры . Например, кастрюля с водой на плите будет постепенно нагреваться до тех пор, пока температура воды не приблизится к 212° F (или 100° C) — она будет оставаться при этой температуре, пока вся вода не выкипит.То же самое верно, как вода замерзает. Когда вода остынет, она достигнет 32°F (или 0°C) и будет оставаться при этой температуре до тех пор, пока вся вода не замерзнет (рис. 7.12).
Чтобы преобразовать 1 грамм льда при 0°C в 1 грамм воды при 0°C 8000 калорий. |
| Для преобразования 1 грамм воды при 100°C в 1 грамм пара при 100°C калорий требуется 540009 0. |
Когда любой материал нагревается до температуры, при которой он меняет свое состояние, температура остается неизменной до тех пор, пока весь материал не изменит свое состояние. Это означает, что ледяная вода будет оставаться при температуре 0 ° C ( 32 ° F ) до тех пор, пока все лед не растает. То же самое относится и к охлаждению материалов. Причина в том, что для перехода из твердого состояния в жидкое или из жидкого в газообразное необходимо затратить энергию. Точно так же энергия должна быть изъята для изменения состояния при охлаждении материала.Количество необходимой энергии называется скрытой теплотой замерзания или кипения.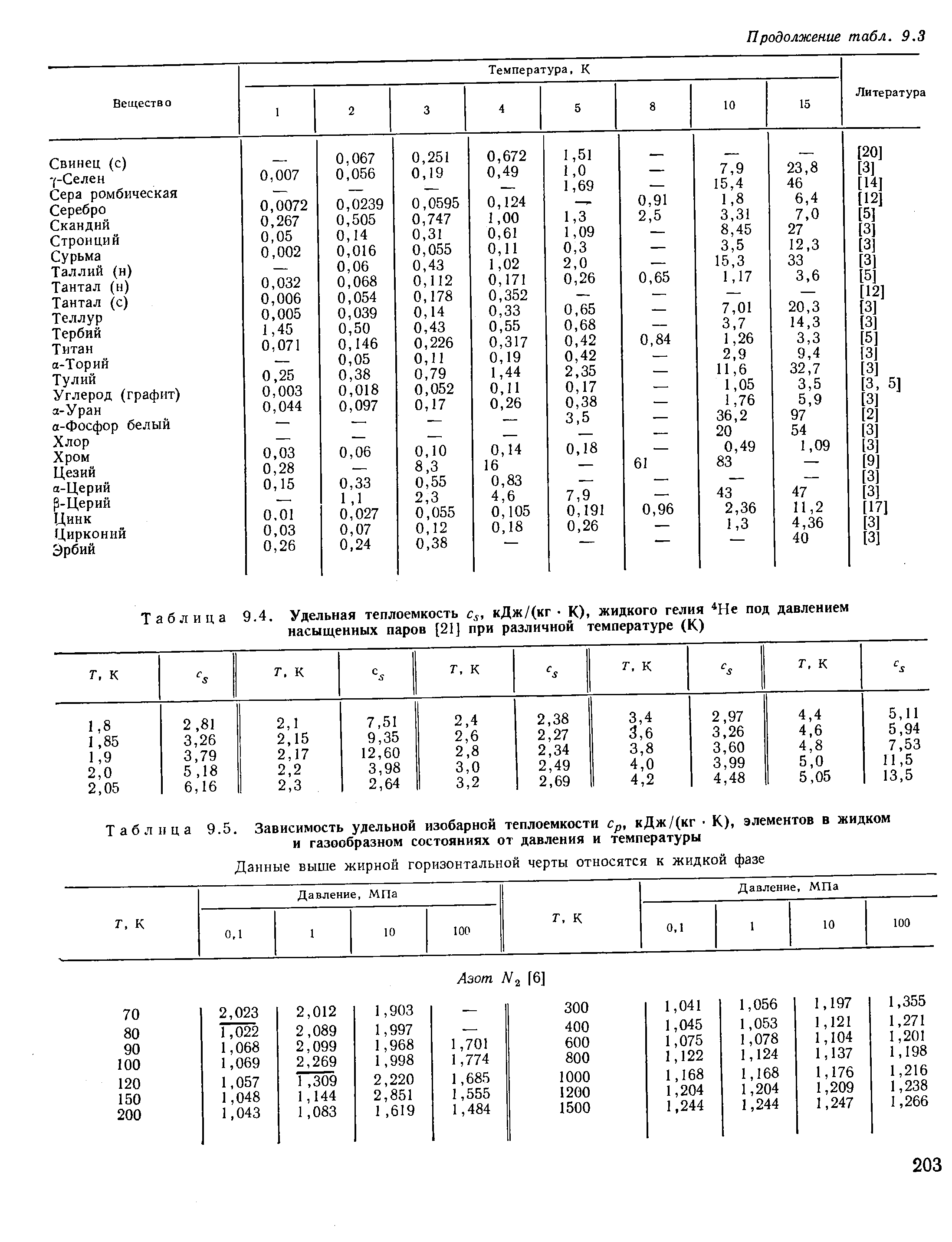
Рисунок 7.12. Диаграмма, показывающая тепло, необходимое для нагревания воды от твердого льда до жидкой воды и пара (пара). Для превращения льда в пар требуется как удельная теплота, так и скрытая теплота, выделяемая поэтапно!
Свойства воды Удельная теплоемкость воды
Связанные ресурсы: физика
Свойства воды Удельная теплоемкость воды
Термодинамика
Свойства воды
- Удельная теплоемкость воды
- Теплопроводность воды
- Вязкость воды
Темп.(°F) | Удельная теплоемкость | Теплопроводность | Вязкость | ||||||
C p (БТЕ/фунт °R) | к ( БТЕ / час фут ° F | мкм (фунт/час фут) | |||||||
Сатур. | 1000 | 2000 | Сатур. | 1000 | 2000 | Сатур. | 1000 | 2000 | |
80 | 0.9975 | 0,9943 | 0,9912 | 0,3532 | 0,3537 | 0,3570 | 2,084 | 2,084 | 2,083 |
100 | 0.9976 | 0,9932 | 0,9897 | 0,3641 | 0,3659 | 0,3680 | 1. | 1,654 | 1,658 |
200 | 1.0047 | 1.0008 | 0,9958 | 0,3935 | 0,3957 | 0,3980 | 0,738 | 0,748 | 0,757 |
300 | 1.0289 | 1.0232 | 1.0166 | 0,3952 | 0,3981 | 0,4013 | 0,425 | 0,460 | 0,468 |
400 | 1.0794 | 1,074 | 1,062 | 0,3809 | 0,3840 | 0,3880 | 0,327 | 0,330 | 0,335 |
420 | 1. | 1,087 | 1,075 | 0,3753 | 0,3787 | 0,3833 | 0,310 | 0,312 | 0,317 |
440 | 1.1114 | 1.105 | 1,091 | 0,3693 | 0,3728 | 0,3776 | 0,294 | 0,296 | 0,301 |
460 | 1.1319 | 1,124 | 1.109 | 0,3640 | 0,3664 | 0,3713 | 0,280 | 0,282 | 0,286 |
480 | 1.1345 | 1,149 | 1.131 | 0,3575 | 0,3595 | 0,3642 | 0,267 | 0,270 | 0,273 |
500 | 1. | 1,176 | 1,154 | 0,3494 | 0,3510 | 0,3562 | 0,256 | 0,257 | 0,260 |
520 | 1.23 | 1,21 | 1,188 | 0,3397 | 0,3410 | 0,3475 | 0,246 | 0,246 | 0,249 |
540 | 1.28 | — | 1,225 | 0,3298 | — | 0,3371 | 0,235 | — | 0,239 |
|---|---|---|---|---|---|---|---|---|---|
560 | 1.34 | — | 1,278 | 0,3189 | — | 0,3256 | 0,225 | — | 0,231 |
580 | 1. | — | 1,341 | 0,3064 | — | 0,3118 | 0,217 | — | 0,222 |
600 | 1.51 | — | 1,448 | 0,2919 | — | 0,2962 | 0,210 | — | 0,212 |
620 | 1.65 | — | 1,62 | 0,2753 | — | 0,2778 | 0,200 | — | 0,202 |
640 | 1.88 | — | — | 0,2565 | — | — | 0,190 | — | — |
660 | 2. | — | — | 0,2335 | — | — | 0,177 | — | — |
680 | 3.5 | — | — | 0,2056 | — | — | 0,161 | — | — |
Удельная теплоемкость воды в зависимости от температуры (p = 1 бар)
Удельная теплоемкость воды по сравнению сУдельная теплоемкость песка | Научный проект
Как можно наблюдать и измерять удельную теплоемкость различных веществ?
- Настольная лампа
- Коробка
- Канцелярский нож или ножницы
- 2 не бумажных стаканчика
- 2 термометра
- Песок
- Вода
- Попросите взрослого помочь вам отрезать одну сторону коробки.
 Вы хотите максимально сохранить тепловую энергию лампы, заключенной в области вашего эксперимента.
Вы хотите максимально сохранить тепловую энергию лампы, заключенной в области вашего эксперимента. - Наполните одну из чашек песком, а другую водой комнатной температуры.
- Поместите чашки рядом на дно коробки.
- Поместите лампу за коробку и наклоните головку так, чтобы при включении свет падал на чашки. Лампочка должна находиться на одинаковом расстоянии от каждой чашки. Почему это важно?
- Пока не включайте лампу.
- Поместите термометр примерно на один дюйм в песок.Поместите второй термометр примерно на один дюйм в воду.
- Запишите начальные температуры песка и воды в таблицу данных, подобную следующей.
Время в минутах | Температура воды | Температурный песок |
0 |
|
|
2 |
|
|
4 |
|
|
6 |
|
|
8 |
|
|
10 |
|
|
12 |
|
|
14 |
|
|
16 |
|
|
18 |
|
|
20 |
|
|
- Включите свет.

- Записывайте температуру песка и воды каждые две минуты в течение не менее 20 минут. Будьте осторожны, чтобы чашки не расплавились под лампочкой. Если кажется, что температура не сильно меняется, попробуйте переместить свет ближе к чашкам или использовать лампочку большей мощности.
Песок прогревается быстрее, чем вода.
Было важно убедиться, что свет находится на одинаковом расстоянии от песка и воды, потому что вы хотели, чтобы каждая чашка получала одинаковое количество энергии от света.Это контролируемый эксперимент , и единственная переменная, которую вы хотите протестировать, — это тип вещества в чашке. Одна из причин, по которой песок нагревается быстрее, заключается в том, что удельная теплоемкость песка ниже, чем удельная теплоемкость воды. Вот почему для изменения его температуры требовалось меньше энергии света.
Какие еще свойства определяют скорость нагревания вещества? Попробуйте провести тот же эксперимент со светлым и темным камнем или разными типами жидкостей. Вы также можете провести эксперимент в обратном порядке, измеряя, как разные вещества остывают с течением времени.
Вы также можете провести эксперимент в обратном порядке, измеряя, как разные вещества остывают с течением времени.
Отказ от ответственности и меры предосторожности
Education.com предоставляет идеи проекта научной ярмарки для ознакомления
только цели. Education.com не дает никаких гарантий или заявлений
относительно идей проекта научной ярмарки и не несет ответственности за
любые убытки или ущерб, прямо или косвенно вызванные использованием вами таких
Информация. Получая доступ к идеям проекта научной ярмарки, вы отказываетесь и
отказаться от каких-либо претензий к Образованию.com, которые возникают из-за этого. Кроме того, ваш
доступ к веб-сайту Education.com и проектным идеям научной ярмарки покрывается
Политика конфиденциальности Education.com и Условия использования сайта, включая ограничения
об ответственности Education.com.
Настоящим предупреждаем, что не все проектные идеи подходят для всех
отдельных лиц или во всех обстоятельствах. Реализация любой идеи научного проекта
Реализация любой идеи научного проекта
следует проводить только в соответствующих условиях и с соответствующими родителями.
или другой надзор.Чтение и соблюдение мер предосторожности всех
материалы, используемые в проекте, является исключительной ответственностью каждого человека. Для
дополнительную информацию см. в справочнике по научной безопасности вашего штата.
Свойства воды при атмосферном давлении
Свойства воды приведены ниже в таблице в метрических единицах СИ для температур от 0°C до 100°C при атмосферном давлении 101,325 кПа. часто называют свойствами насыщенной воды, насыщенной жидкости или теплофизическими свойствами.В таблице указаны плотность, динамическая вязкость, кинематическая вязкость, удельная теплоемкость, теплопроводность и число Прандтля. Под таблицей находится версия файла изображения для просмотра в автономном режиме
.
Свойства указаны для чуть выше точки замерзания и чуть ниже точки кипения.
Примечание: Обратите внимание на единицы измерения вязкости.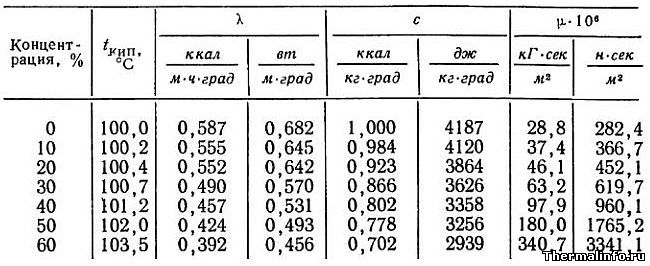 Пример: 1,7292×10 -6 м 2 /с = 0,0000017292 м 2 /с
Пример: 1,7292×10 -6 м 2 /с = 0,0000017292 м 2 /с
| Температура (T) | Плотность (ρ) | Динамическая вязкость (мк) | Кинематическая вязкость (v) | Удельная теплоемкость (cp) | Теплопроводность (k) | Число Прандтля (Pr) |
|---|---|---|---|---|---|---|
| ◦с | кг/м 3 | x 10 -3 Па.с | x 10 -6 м 2 /с | кДж/кг.К | Вт/м.К | – |
| 0 | 999,84 | 1,792 | 1,792 | 4.219 | 0,561 | 13,47 |
| 5 | 999,97 | 1,518 | 1,518 | 4.205 | 0,571 | 11.19 |
| 10 | 999,70 | 1.306 | 1.306 | 4,195 | 0,580 | 9,45 |
| 15 | 999.10 | 1,138 | 1,139 | 4. 189 189 | 0,589 | 8.09 |
| 20 | 998.21 | 1,002 | 1.003 | 4,185 | 0,598 | 7,00 |
| 25 | 997.05 | 0,890 | 0,893 | 4.182 | 0,607 | 6.13 |
| 30 | 995,65 | 0,797 | 0,801 | 4.180 | 0,616 | 5,41 |
| 35 | 994.04 | 0,719 | 0,724 | 4.179 | 0,623 | 4,82 |
| 40 | 992,22 | 0,653 | 0,658 | 4.179 | 0,631 | 4,33 |
| 45 | 990.22 | 0,596 | 0,602 | 4.179 | 0,637 | 3,91 |
| 50 | 988.05 | 0,547 | 0,553 | 4.180 | 0,644 | 3,55 |
| 55 | 985,71 | 0,504 | 0,511 | 4. 181 181 | 0,649 | 3,25 |
| 60 | 983,21 | 0,466 | 0,474 | 4.183 | 0,654 | 2,98 |
| 65 | 980,57 | 0,433 | 0,442 | 4,185 | 0,659 | 2,75 |
| 70 | 977,78 | 0,404 | 0,413 | 4,188 | 0,663 | 2,55 |
| 75 | 974,86 | 0,378 | 0,387 | 4.192 | 0,667 | 2,37 |
| 80 | 971.80 | 0,354 | 0,365 | 4.196 | 0,670 | 2,22 |
| 85 | 968,62 | 0,333 | 0,344 | 4.200 | 0,673 | 2,08 |
| 90 | 965,32 | 0,314 | 0,326 | 4.205 | 0,675 | 1,96 |
| 95 | 961,90 | 0,297 | 0,309 | 4. 211 211 | 0,677 | 1,85 |
| 100 | 958,43 | 0,282 | 0,294 | 4.217 | 0,679 | 1,75 |
Предыдущая статьяОбъедините ячейки даты и времени в ExcelСледующая статьяСвойства воздуха при атмосферном давлении
Frontiers | Удельная теплоемкость замкнутой воды в чрезвычайно узких графеновых наноканалах
Введение
Удельная теплоемкость — важное теплофизическое свойство, измеряющее способность вещества накапливать энергию, определяемое как количество тепла, необходимое для повышения температуры на 1 К субстрата на единицу массы.Благодаря высокой удельной теплоемкости вода широко используется в качестве среды в процессах теплообмена и охлаждения устройств (Steeneveld et al., 2014; Izadi et al., 2020). Поскольку размеры многих устройств, таких как лаборатории на кристаллах, NEMS и электронные чипы, уменьшены до наноразмеров, быстрое рассеивание тепла становится проблемой, ограничивающей разработку наноустройств (Lee et al. , 2013). Теплофизические свойства нанозамкнутой воды (Sun et al., 2020), особенно удельная теплоемкость, определяют, может ли она функционировать в наномасштабах.
, 2013). Теплофизические свойства нанозамкнутой воды (Sun et al., 2020), особенно удельная теплоемкость, определяют, может ли она функционировать в наномасштабах.
Большое внимание исследователей привлекла удельная теплоемкость нанозамкнутой воды и других жидкостей. Томбари и др. (2005a), Томбари и др. (2005b) с помощью калориметрии исследовали удельную теплоемкость воды, заключенной в стеклянных нанопорах со средним диаметром 4 нм. Они обнаружили, что изобарическая удельная теплоемкость отклоняется от объемного значения, и объяснили это снижением плотности из-за наноограничения. Тот же метод был использован для изучения удельной теплоемкости бензола, заключенного в мезопорах MCM-41 (Nagoe et al., 2015). Помимо калориметрии, метод неупругого рассеяния нейтронов также был разработан для оценки удельной теплоемкости жидкостей, заключенных в нанопоры (Gautam et al., 2018). Тем не менее, прямые экспериментальные измерения удельной теплоемкости нанозамкнутой воды все еще ограничены из-за проблемы точного контроля и измерения небольшого количества воды.
В качестве эффективного и мощного альтернативного инструмента моделирование молекулярной динамики (МД) продемонстрировало отличные результаты при изучении теплофизических свойств воды в наномасштабах, таких как вязкость (Neek-Amal et al., 2016; Zhou et al., 2021), теплопроводность (Zhao et al., 2020a; Zhao et al., 2020b), коэффициент диффузии (Zhao et al., 2020c) и диэлектрическая проницаемость (Hamid et al., 2021). И становится здравым смыслом то, что молекулярное поведение воды в условиях наноудержания отличается от поведения в объеме (Sofos et al., 2013; Sofos and Karakasidis, 2021) из-за большого отношения поверхности к объему и усиленного влияния поверхностных свойств, включая поверхностные. смачиваемость и морфология поверхности (Shadloo-Jahromi et al., 2020; Шадлу-Джахроми и др., 2021). Таким образом, теплофизические свойства в основном зависят от размера наноканалов или пор (Sofos et al., 2013; Zhao et al., 2020a; Zhao et al., 2020b; Zhao et al., 2020c; Hamid et al., 2021; Sofos and Karakasidis, 2021; Zhou et al. , 2021). Исследования удельной теплоемкости воды и других жидкостей с использованием метода МД (Gautam et al., 2018; Alkhwaji et al., 2021) дополнительно продемонстрировали потенциал метода МД при исследовании воды на наноуровне.Недавно Лу и соавт. (Jin et al., 2021) с помощью метода МД исследовали зависящую от размера удельную теплоемкость воды, заключенной в медных наноканалах размером более 5 нм, и обнаружили, что удельная теплоемкость воды увеличивалась с увеличением размера канала до постоянное плато. Однако предыдущие исследования других теплофизических свойств показали, что более резкие изменения теплофизических свойств, представленные в замкнутой воде, содержащейся в чрезвычайно узких наноканалах размером менее 5 нм (Neek-Amal et al., 2016; Чжао и др., 2020b; Сан и др., 2021а; Sun et al., 2021b), который представляет собой бланк данных удельной теплоемкости, оставленный предыдущими работами (Jin et al., 2021).
, 2021). Исследования удельной теплоемкости воды и других жидкостей с использованием метода МД (Gautam et al., 2018; Alkhwaji et al., 2021) дополнительно продемонстрировали потенциал метода МД при исследовании воды на наноуровне.Недавно Лу и соавт. (Jin et al., 2021) с помощью метода МД исследовали зависящую от размера удельную теплоемкость воды, заключенной в медных наноканалах размером более 5 нм, и обнаружили, что удельная теплоемкость воды увеличивалась с увеличением размера канала до постоянное плато. Однако предыдущие исследования других теплофизических свойств показали, что более резкие изменения теплофизических свойств, представленные в замкнутой воде, содержащейся в чрезвычайно узких наноканалах размером менее 5 нм (Neek-Amal et al., 2016; Чжао и др., 2020b; Сан и др., 2021а; Sun et al., 2021b), который представляет собой бланк данных удельной теплоемкости, оставленный предыдущими работами (Jin et al., 2021).
В этой работе мы исследуем удельную теплоемкость воды, заключенной в чрезвычайно узких графеновых наноканалах высотой менее 5 нм, с использованием метода МД. Сообщается о размерно-зависимом эффекте и эффекте соизмеримости удельной теплоемкости. Основные механизмы раскрываются на основе особенностей конфигурации, включая распределение плотности и водородную связь, а также особенностей вибрации, включая функцию автокорреляции скорости (VACF) и колебательную плотность состояний (VDOS).Эта работа может не только предоставить данные о теплоемкости наноудержанной воды, но и обогатить механизм влияния наноудержания на теплофизические свойства воды. Полученные результаты, наконец, принесут пользу для различных энергетических приложений.
Сообщается о размерно-зависимом эффекте и эффекте соизмеримости удельной теплоемкости. Основные механизмы раскрываются на основе особенностей конфигурации, включая распределение плотности и водородную связь, а также особенностей вибрации, включая функцию автокорреляции скорости (VACF) и колебательную плотность состояний (VDOS).Эта работа может не только предоставить данные о теплоемкости наноудержанной воды, но и обогатить механизм влияния наноудержания на теплофизические свойства воды. Полученные результаты, наконец, принесут пользу для различных энергетических приложений.
Методы моделирования
Модель моделирования и настройка динамики
Система моделирования МД показана на рисунке 1. Пленки воды заключены в двумерные наноканалы, образованные двумя отдельными графеновыми листами размером L x × л у = 39.335 Å × 38,327 Å и с разделением L z в диапазоне от 6,332 до 50,656 Å. Размер блоков моделирования такой же, как у листов графена в направлениях x и y , но немного больше, чем расстояние между листами графена, чтобы устранить граничные эффекты в направлении z . Молекулы воды моделируются с помощью широко используемой трехточечной модели SPC/E, где параметр энергии ε O-O равен 0.0067 эВ, а размерный параметр σ O-O равен 3,166 Å (Berendsen et al., 1987). Взаимодействия между графеном и молекулами воды моделируются потенциалом Леннарда-Джонса (LJ) 12-6 с радиусом отсечки 10 Å, а электростатические силы рассчитываются с помощью алгоритма PPPM с точностью 10 −4 . Параметр энергии между молекулами графена и воды выбран как ε CO = 0,6 ε OO , в соответствии с гидрофобностью графена, а параметр размера просто выбран как σ CO = σ OO , аналогично расчетному значению 3.263 Å в литературе (Bavi and Ghadak, 2021).
Размер блоков моделирования такой же, как у листов графена в направлениях x и y , но немного больше, чем расстояние между листами графена, чтобы устранить граничные эффекты в направлении z . Молекулы воды моделируются с помощью широко используемой трехточечной модели SPC/E, где параметр энергии ε O-O равен 0.0067 эВ, а размерный параметр σ O-O равен 3,166 Å (Berendsen et al., 1987). Взаимодействия между графеном и молекулами воды моделируются потенциалом Леннарда-Джонса (LJ) 12-6 с радиусом отсечки 10 Å, а электростатические силы рассчитываются с помощью алгоритма PPPM с точностью 10 −4 . Параметр энергии между молекулами графена и воды выбран как ε CO = 0,6 ε OO , в соответствии с гидрофобностью графена, а параметр размера просто выбран как σ CO = σ OO , аналогично расчетному значению 3.263 Å в литературе (Bavi and Ghadak, 2021). Плотность воды составляет 1 г/см 3 , и соответствующее количество молекул воды зависит от высоты наноканалов (определяется как H = L z – σ = от 1 до 15 σ , где σ является сокращением от σ OO ). Периодические граничные условия используются во всех направлениях. Графеновые стенки замораживаются во время моделирования. Шаг по времени составляет 1 фс.Перед сбором данных мы проводим моделирование 1,1 нс для достижения равновесия в ансамбле NVT, контролируемом термостатом Нозе-Гувера. Затем с интервалом 100 фс замеряются температура T и внутренняя энергия U воды в течение 5-нс моделирования.
Плотность воды составляет 1 г/см 3 , и соответствующее количество молекул воды зависит от высоты наноканалов (определяется как H = L z – σ = от 1 до 15 σ , где σ является сокращением от σ OO ). Периодические граничные условия используются во всех направлениях. Графеновые стенки замораживаются во время моделирования. Шаг по времени составляет 1 фс.Перед сбором данных мы проводим моделирование 1,1 нс для достижения равновесия в ансамбле NVT, контролируемом термостатом Нозе-Гувера. Затем с интервалом 100 фс замеряются температура T и внутренняя энергия U воды в течение 5-нс моделирования.
РИСУНОК 1 . Схема системы моделирования. Цветовые коды: атом кислорода — синий, атом водорода — белый, атом углерода — зеленый.
Расчет удельной теплоемкости
Необходимо отметить, что удельная теплоемкость здесь конкретно относится к изохорной удельной теплоемкости ( c v = ( ∂u / ∂T ) v , где u — удельная внутренняя энергия, определяемая как внутренняя энергия единицы массы, U / m ) принадлежащая постоянному объему воды. Однако, поскольку разница между изохорной удельной теплоемкостью и изобарической удельной теплоемкостью при 300 К достаточно мала, чтобы ею можно было вообще пренебречь, и составляет всего 1,2% в объемной воде (Haynes, 2014; Sekerka, 2015), в дальнейшем различия не делаются. между изохорной удельной теплоемкостью и изобарической удельной теплоемкостью, если это существенно не влияет на вывод.
Однако, поскольку разница между изохорной удельной теплоемкостью и изобарической удельной теплоемкостью при 300 К достаточно мала, чтобы ею можно было вообще пренебречь, и составляет всего 1,2% в объемной воде (Haynes, 2014; Sekerka, 2015), в дальнейшем различия не делаются. между изохорной удельной теплоемкостью и изобарической удельной теплоемкостью, если это существенно не влияет на вывод.
Существует три основных различных метода расчета удельной теплоемкости (Pathria and Beale, 2011; Alkhwaji et al., 2021; Джин и др., 2021). Первые два метода просты и предполагают, что удельная теплоемкость не зависит от температуры в небольшом диапазоне (Alkhwaji et al., 2021; Jin et al., 2021). Первый метод основан на следующем уравнении (Alkhwaji et al., 2021):
cv=〈U2〉−〈U1〉〈T2〉−〈T1〉⋅1m,(1)
, где <···> представляет собой среднее значение переменной. T 1 = 295 К и T 2 = 305 К в этом случае моделируются соответственно. Второй метод соответствует удельной теплоемкости со следующими соотношениями (Jin et al. , 2021):
, 2021):
U(t)=kU⋅t+U0,T(t)=kT⋅t+T0,cv=kUkT·m, (2)
где k U и k T – скорости изменения внутренней энергии U и температуры T во времени t соответственно. В этом случае равновесная температура устанавливается равной 295 К, а затем температура повышается до 305 К со скоростью 2 К/нс. В основе третьего метода лежит статистическая механика, основанная на соотношении между c v и среднеквадратичным отклонением U следующим образом (Pathria and Beale, 2011; Alkhwaji et al., 2021):
cv=〈U2〉−〈U〉2kBT2⋅m, (3)
, где k B – постоянная Больцмана. В этом случае температура составляет 300 К. Кроме того, предыдущие исследования моделирования (Jorgensen and Tirado-Rives, 2005; Vega et al., 2010) показали, что удельная теплоемкость, рассчитанная с помощью классического моделирования, была немного больше, чем экспериментальный результат, 4,13 Дж/(г·К) (Haynes, 2014). Вега и др. (2010) объяснили это отклонение отсутствием ядерных квантовых эффектов в классическом МД-моделировании.Таким образом, к исходной удельной теплоемкости следует добавить квантовый вклад -0,520 Дж/(г·К) при 300 К (Alkhwaji et al., 2021).
Вега и др. (2010) объяснили это отклонение отсутствием ядерных квантовых эффектов в классическом МД-моделировании.Таким образом, к исходной удельной теплоемкости следует добавить квантовый вклад -0,520 Дж/(г·К) при 300 К (Alkhwaji et al., 2021).
Сначала мы рассчитываем удельную теплоемкость воды в свободном объеме, чтобы протестировать имитационную модель и методы. Проверки независимости, включая размер ящика, количество молекул воды, время релаксации, точность сходимости алгоритма PPPM, интервал выборки и время моделирования, были тщательно выполнены для обеспечения достоверности моделирования. (см. раздел 1 дополнительных материалов).Скорректированное значение c v объемной воды при 300 К, рассчитанное тремя методами (сообщено как 4,026 ± 0,023 Дж/(г·К), 4,037 ± 0,002 Дж/(г·К) и 4,099 ± 0,038 Дж/(г·К) , соответственно) подобны друг другу, демонстрируя эквивалентность трех методов, и приближаются к экспериментальному значению, демонстрируя, что классическая модель воды SPC/E может хорошо описывать теплоемкость воды с квантовой поправкой. Поскольку удельная теплоемкость по третьему методу лучше всего согласуется с экспериментальным значением (см. рис. 2А), имеет преимущества в скорости и надежности и не зависит от постоянной гипотезы; третий метод выбран для расчета c v замкнутой воды далее.На данный момент продемонстрированы как обоснованность, так и надежность имитационной модели и метода расчета.
Поскольку удельная теплоемкость по третьему методу лучше всего согласуется с экспериментальным значением (см. рис. 2А), имеет преимущества в скорости и надежности и не зависит от постоянной гипотезы; третий метод выбран для расчета c v замкнутой воды далее.На данный момент продемонстрированы как обоснованность, так и надежность имитационной модели и метода расчета.
РИСУНОК 2 . Удельная теплоемкость и удельная внутренняя энергия при 300 К. (A) Удельная теплоемкость в зависимости от размера канала. Черная пунктирная линия показывает флуктуации, синяя пунктирная линия представляет собой линейную подгонку, а точка поворота, в которой они пересекаются, соответствует H = 5,5 σ. Вставка: сравнение литературы (Jin et al., 2021). (B) Удельная внутренняя энергия в зависимости от размера канала.Штриховые линии представляют соответствующее объемное значение.
Результаты и обсуждение
Удельная теплоемкость нанонапорной воды
На рис. , нормированная удельная теплоемкость c , нормированная , отношение c к воды, заключенной в графеновых наноканалах, к объемному значению, нанесено на график в зависимости от высоты канала на вставке к рисунку 2, а значения c нормализовано воды, заключенной в медных наноканалах (отношение к подобранному асимптотическому значению) в диапазоне от 50 Å до 800 Å (Jin et al., 2021) также нанесены на вставку для сравнения. Установлено, что c v напорной воды ниже, чем у свободной объемной воды, и отклонение обычно увеличивается по мере уменьшения H . В канале выше 5,5 σ изменение c v монотонно. Но ниже этой критической точки c v колеблются одновременно с H . Это явление происходит из-за основного физического механизма.Ник-Амаль и др. (2016) обнаружили аналогичные колебания вязкости замкнутой воды в чрезвычайно узких графеновых наноканалах и назвали это эффектом соизмеримости, возникающим в результате слоистой структуры из-за наноограничения.
, нормированная удельная теплоемкость c , нормированная , отношение c к воды, заключенной в графеновых наноканалах, к объемному значению, нанесено на график в зависимости от высоты канала на вставке к рисунку 2, а значения c нормализовано воды, заключенной в медных наноканалах (отношение к подобранному асимптотическому значению) в диапазоне от 50 Å до 800 Å (Jin et al., 2021) также нанесены на вставку для сравнения. Установлено, что c v напорной воды ниже, чем у свободной объемной воды, и отклонение обычно увеличивается по мере уменьшения H . В канале выше 5,5 σ изменение c v монотонно. Но ниже этой критической точки c v колеблются одновременно с H . Это явление происходит из-за основного физического механизма.Ник-Амаль и др. (2016) обнаружили аналогичные колебания вязкости замкнутой воды в чрезвычайно узких графеновых наноканалах и назвали это эффектом соизмеримости, возникающим в результате слоистой структуры из-за наноограничения. Они показали, что локальному минимуму вязкости соответствует локальное максимальное расстояние слоев воды, и наоборот. Такая же зависимость применима и к теплоемкости. Насколько нам известно, здесь впервые сообщается об эффектах соизмеримости в c v нанозамкнутой воды.Для удельной внутренней энергии ее изменение, в основном определяемое потенциальной энергией, показывает противоположную тенденцию по сравнению с c v (см. рис. 2Б). Различные вариации c v и удельной внутренней энергии показывают, что c v измеряют чувствительность внутренней энергии к температуре, но не значение внутренней энергии (Tombari et al., 2005b), хотя они есть взаимосвязь, которая будет рассмотрена в VACF и VDOS .
Они показали, что локальному минимуму вязкости соответствует локальное максимальное расстояние слоев воды, и наоборот. Такая же зависимость применима и к теплоемкости. Насколько нам известно, здесь впервые сообщается об эффектах соизмеримости в c v нанозамкнутой воды.Для удельной внутренней энергии ее изменение, в основном определяемое потенциальной энергией, показывает противоположную тенденцию по сравнению с c v (см. рис. 2Б). Различные вариации c v и удельной внутренней энергии показывают, что c v измеряют чувствительность внутренней энергии к температуре, но не значение внутренней энергии (Tombari et al., 2005b), хотя они есть взаимосвязь, которая будет рассмотрена в VACF и VDOS .
Чтобы объяснить отклонение c v в нанозамкнутой воде, мы должны обратиться к конфигурациям и колебаниям нанозамкнутой воды, которые определяют c v . Поскольку эти два аспекта не являются независимыми, а тесно связаны (Tombari et al., 2005a), сначала будут обсуждаться конфигурационные характеристики, включая распределение плотности и водородные связи, а затем колебательные характеристики, включая VACF и VDOS.
Поскольку эти два аспекта не являются независимыми, а тесно связаны (Tombari et al., 2005a), сначала будут обсуждаться конфигурационные характеристики, включая распределение плотности и водородные связи, а затем колебательные характеристики, включая VACF и VDOS.
Распределение плотности и водородная связь
Конфигурация воды, заключенной в графеновых наноканалах, отличается от конфигурации воды в объеме из-за эффекта удержания стенками канала (Sun et al., 2020; Чжоу и др., 2021 г.; Чжао и др., 2020a; Чжао и др., 2020b; Чжао и др., 2020c). В частности, сила отталкивания удерживает молекулы воды в наноканале, тогда как потенциальная яма или адсорбционное взаимодействие меняют структуру замкнутой воды (Zhao et al., 2020b). По сравнению с однородной объемной водой напорная вода неоднородна. Распределение плотности воды (Калашами и др., 2018) приурочено к типичным каналам размером H = 2 σ , 5.5 σ , 10.5 σ , 15 σ , представляющие собой по высоте ниже критической точки, вблизи критической точки и выше критической точки соответственно, наглядно показывает отличие конфигурации напорной воды от объемная вода (см. Рисунок 3A, другие случаи показаны на дополнительном рисунке S7). В широких наноканалах плотность, прилегающая к стенке, значительно выше объемной, образуя по три значимых пика плотности с каждой стороны, причем интенсивность соответствующих пиков плотности практически одинакова в разных наноканалах, тогда как плотность в средней области стремится к объемному значению, а распределение плотности плоское.Мы определяем замкнутую воду с таким распределением плотности как 3P-B-3P. При уменьшении высоты канала до H = 5,5 σ объемная область перестает существовать, и третьи (тоже самые слабые) пики перекрываются друг с другом; таким образом, остается только пять пиков, но интенсивность пиков плотности увеличивается по сравнению с таковой в широких наноканалах. По мере того как высота канала продолжает уменьшаться до H = 2 σ , остаются только ближайшие к стенке пики, а интенсивность пиков плотности чрезвычайно возрастает.Кроме того, хотя средний пик слабый, число пиков плотности атомов водорода на единицу больше, чем атомов кислорода, что указывает на резкое изменение структуры.
Рисунок 3A, другие случаи показаны на дополнительном рисунке S7). В широких наноканалах плотность, прилегающая к стенке, значительно выше объемной, образуя по три значимых пика плотности с каждой стороны, причем интенсивность соответствующих пиков плотности практически одинакова в разных наноканалах, тогда как плотность в средней области стремится к объемному значению, а распределение плотности плоское.Мы определяем замкнутую воду с таким распределением плотности как 3P-B-3P. При уменьшении высоты канала до H = 5,5 σ объемная область перестает существовать, и третьи (тоже самые слабые) пики перекрываются друг с другом; таким образом, остается только пять пиков, но интенсивность пиков плотности увеличивается по сравнению с таковой в широких наноканалах. По мере того как высота канала продолжает уменьшаться до H = 2 σ , остаются только ближайшие к стенке пики, а интенсивность пиков плотности чрезвычайно возрастает.Кроме того, хотя средний пик слабый, число пиков плотности атомов водорода на единицу больше, чем атомов кислорода, что указывает на резкое изменение структуры. Мы определяем напорную воду с такими типами распределения плотности как x P-0- x P, где x ≤ 3. Различия в структуре и свойствах напорной воды 3P-B-3P в разных наноканалах в основном связаны от доли основного объема, но различия между x P-0- x P замкнутой воды вызваны сложными факторами, включая количество пиков и эффекты соизмеримости (подробности на дополнительном рисунке S7).Пока можно разумно предположить, что уменьшение удельной теплоемкости замкнутой воды и появление критической точки определенно связаны с изменением структуры, на которое указывает распределение плотности. Чтобы наглядно показать изменение конфигурации воды в наноканалах, мы дополнительно делаем снимки для каждого случая, представляя молекулы воды атомами кислорода (см. рис. 3А). В отличие от объемной воды, в напорной воде слоистая структура, соответствующая пикам в распределении плотности, возникает вблизи стенки.Анизотропная кристаллоподобная характеристика может оказывать большое влияние на c v замкнутой воды (Левченко и др.
Мы определяем напорную воду с такими типами распределения плотности как x P-0- x P, где x ≤ 3. Различия в структуре и свойствах напорной воды 3P-B-3P в разных наноканалах в основном связаны от доли основного объема, но различия между x P-0- x P замкнутой воды вызваны сложными факторами, включая количество пиков и эффекты соизмеримости (подробности на дополнительном рисунке S7).Пока можно разумно предположить, что уменьшение удельной теплоемкости замкнутой воды и появление критической точки определенно связаны с изменением структуры, на которое указывает распределение плотности. Чтобы наглядно показать изменение конфигурации воды в наноканалах, мы дополнительно делаем снимки для каждого случая, представляя молекулы воды атомами кислорода (см. рис. 3А). В отличие от объемной воды, в напорной воде слоистая структура, соответствующая пикам в распределении плотности, возникает вблизи стенки.Анизотропная кристаллоподобная характеристика может оказывать большое влияние на c v замкнутой воды (Левченко и др. , 2007; Ши и др., 2012).
, 2007; Ши и др., 2012).
РИСУНОК 3 . Распределение плотности и среднее координационное число водородной связи воды. (A) Распределение плотности воды перпендикулярно стенке зависит от высоты канала; пунктирные горизонтальные линии относятся к общему значению; пики, соответствующие слоям воды, обозначены цифрами; снимки представляют собой конфигурации молекул воды, представленные атомами кислорода, где слои воды появляются с двух сторон у стены. (Б) Среднее координационное число водородных связей воды зависит от высоты канала; снимок — вид сверху на первый слой воды.
Одним из возможных эффектов изменения структуры на удельную теплоемкость, возможно, наиболее важным, является ослабление связи водородными связями между молекулами воды. Водородная связь по существу представляет собой вид сильного электрического взаимодействия, и ряд особых свойств воды в основном обусловлен водородными связями, в том числе более высокая удельная теплоемкость, чем у других обычных веществ. Чтобы продемонстрировать это, мы вычислили удельную теплоемкость виртуальной воды без заряда, которая составляет 1,305 ± 0,006 Дж/(г·К), что намного ниже, чем у реальной воды, но согласуется с теоретическим значением для идеальной трехатомной молекулы, 1,15–1,62 Дж. /(г К). Взаимодействия между молекулами воды с водородными связями можно количественно определить по среднему координационному числу водородных связей на молекулу воды n hсвязи . Как правило, упорядоченная слоистая структура воды, примыкающая к графеновой стенке, не способствует образованию водородных связей и может снижать значение n hbond .Для образования водородных связей две соседние молекулы воды должны находиться в соответствующей ориентации и на соответствующем расстоянии, поэтому должно быть достаточно места для регулировки положения молекул воды. Однако пространство в пристеночной области ограничено. С одной стороны, молекулы воды потеряли половину пространства и возможностей для образования водородных связей из-за стерического барьера стенки; с другой стороны, высокая плотность воды из-за поглощения стеной еще больше уменьшает доступное пространство.
Чтобы продемонстрировать это, мы вычислили удельную теплоемкость виртуальной воды без заряда, которая составляет 1,305 ± 0,006 Дж/(г·К), что намного ниже, чем у реальной воды, но согласуется с теоретическим значением для идеальной трехатомной молекулы, 1,15–1,62 Дж. /(г К). Взаимодействия между молекулами воды с водородными связями можно количественно определить по среднему координационному числу водородных связей на молекулу воды n hсвязи . Как правило, упорядоченная слоистая структура воды, примыкающая к графеновой стенке, не способствует образованию водородных связей и может снижать значение n hbond .Для образования водородных связей две соседние молекулы воды должны находиться в соответствующей ориентации и на соответствующем расстоянии, поэтому должно быть достаточно места для регулировки положения молекул воды. Однако пространство в пристеночной области ограничено. С одной стороны, молекулы воды потеряли половину пространства и возможностей для образования водородных связей из-за стерического барьера стенки; с другой стороны, высокая плотность воды из-за поглощения стеной еще больше уменьшает доступное пространство. Следовательно, молекулы воды не могут в достаточной степени соединяться водородными связями с другими молекулами воды у стенки (Vila Verde et al., 2012), а имеют тенденцию образовывать ромбические и пятиугольные кольца (см. вставку к рисунку 3B). Предыдущие экспериментальные работы показали, что удельная теплоемкость воды на поверхности действительно ниже объемного значения (Левченко и др., 2007; Ши и др., 2012). В узких каналах пристеночная область занимает большую часть и влияние графеновой стенки существенно.Но в широких каналах влияние пристеночной области относительно малочувствительно, и поэтому теплофизические свойства, включая удельную теплоемкость и n hсвязь , стремятся к объемному значению. Чтобы продемонстрировать это, мы рассчитали водородные связи между молекулами воды, заключенными в разных наноканалах, используя геометрическое определение, такое же, как и в предыдущей работе (Sun et al., 2021b; Kumar et al., 2007). Как и ожидалось, n hbond демонстрирует тенденцию к увеличению в зависимости от высоты канала (см.
Следовательно, молекулы воды не могут в достаточной степени соединяться водородными связями с другими молекулами воды у стенки (Vila Verde et al., 2012), а имеют тенденцию образовывать ромбические и пятиугольные кольца (см. вставку к рисунку 3B). Предыдущие экспериментальные работы показали, что удельная теплоемкость воды на поверхности действительно ниже объемного значения (Левченко и др., 2007; Ши и др., 2012). В узких каналах пристеночная область занимает большую часть и влияние графеновой стенки существенно.Но в широких каналах влияние пристеночной области относительно малочувствительно, и поэтому теплофизические свойства, включая удельную теплоемкость и n hсвязь , стремятся к объемному значению. Чтобы продемонстрировать это, мы рассчитали водородные связи между молекулами воды, заключенными в разных наноканалах, используя геометрическое определение, такое же, как и в предыдущей работе (Sun et al., 2021b; Kumar et al., 2007). Как и ожидалось, n hbond демонстрирует тенденцию к увеличению в зависимости от высоты канала (см. рис. 3B).С увеличением размера канала оно постепенно приближается к объемному значению 3,31 (согласуется со значением для модели воды SPC/E в литературе (Kumar et al., 2007)), а именно к изменению n hbond качественно согласуется с изменением удельной теплоемкости и обратно изменению удельной внутренней энергии. Далее мы оцениваем корреляцию между n hсвязи и удельной теплоемкостью и корреляцию между n hсвязи и удельной внутренней энергией соответственно.Коэффициент корреляции Пирсона произведение-момент между n hсвязи и удельной теплоемкостью составляет -0,94, а между n hсвязи и удельной внутренней энергией сообщается как 0,88 после удаления особой точки при H = 1.4 σ (обсуждается в разделе 4 дополнительных материалов). Таким образом, мы количественно показываем, что водородная связь действительно оказывает огромное влияние на удельную теплоемкость воды и внутреннюю энергию.
рис. 3B).С увеличением размера канала оно постепенно приближается к объемному значению 3,31 (согласуется со значением для модели воды SPC/E в литературе (Kumar et al., 2007)), а именно к изменению n hbond качественно согласуется с изменением удельной теплоемкости и обратно изменению удельной внутренней энергии. Далее мы оцениваем корреляцию между n hсвязи и удельной теплоемкостью и корреляцию между n hсвязи и удельной внутренней энергией соответственно.Коэффициент корреляции Пирсона произведение-момент между n hсвязи и удельной теплоемкостью составляет -0,94, а между n hсвязи и удельной внутренней энергией сообщается как 0,88 после удаления особой точки при H = 1.4 σ (обсуждается в разделе 4 дополнительных материалов). Таким образом, мы количественно показываем, что водородная связь действительно оказывает огромное влияние на удельную теплоемкость воды и внутреннюю энергию. Таким образом, с конфигурационного аспекта мы заключаем, что графеновые стенки изменяют структуру воды, заключенной в наноканалах, и препятствуют образованию водородных связей, тем самым снижая удельную теплоемкость воды. Кроме того, мы обсуждаем влияние изменения структуры на удельную теплоемкость с точки зрения функции радиального распределения (RDF) в разделе 3 дополнительных материалов, что еще раз подтверждает вывод, сделанный в этом разделе.
Таким образом, с конфигурационного аспекта мы заключаем, что графеновые стенки изменяют структуру воды, заключенной в наноканалах, и препятствуют образованию водородных связей, тем самым снижая удельную теплоемкость воды. Кроме того, мы обсуждаем влияние изменения структуры на удельную теплоемкость с точки зрения функции радиального распределения (RDF) в разделе 3 дополнительных материалов, что еще раз подтверждает вывод, сделанный в этом разделе.
VACF и VDOS
После обсуждения «статических» конфигурационных характеристик, включая распределение плотности и водородную связь, мы затем проанализируем удельную теплоемкость по «динамическим» характеристикам вибрации замкнутой воды, включая VACF и VDOS, которые более непосредственно связано с теплоемкостью.Сначала мы вычисляем VACF молекул воды, представленных атомом кислорода (см. рис. 4A), определяемый следующим образом: (t0)〉, (4)
, где v i — скорость атома с индексом i , t 0 — начало отсчета времени, а t — корреляция времени.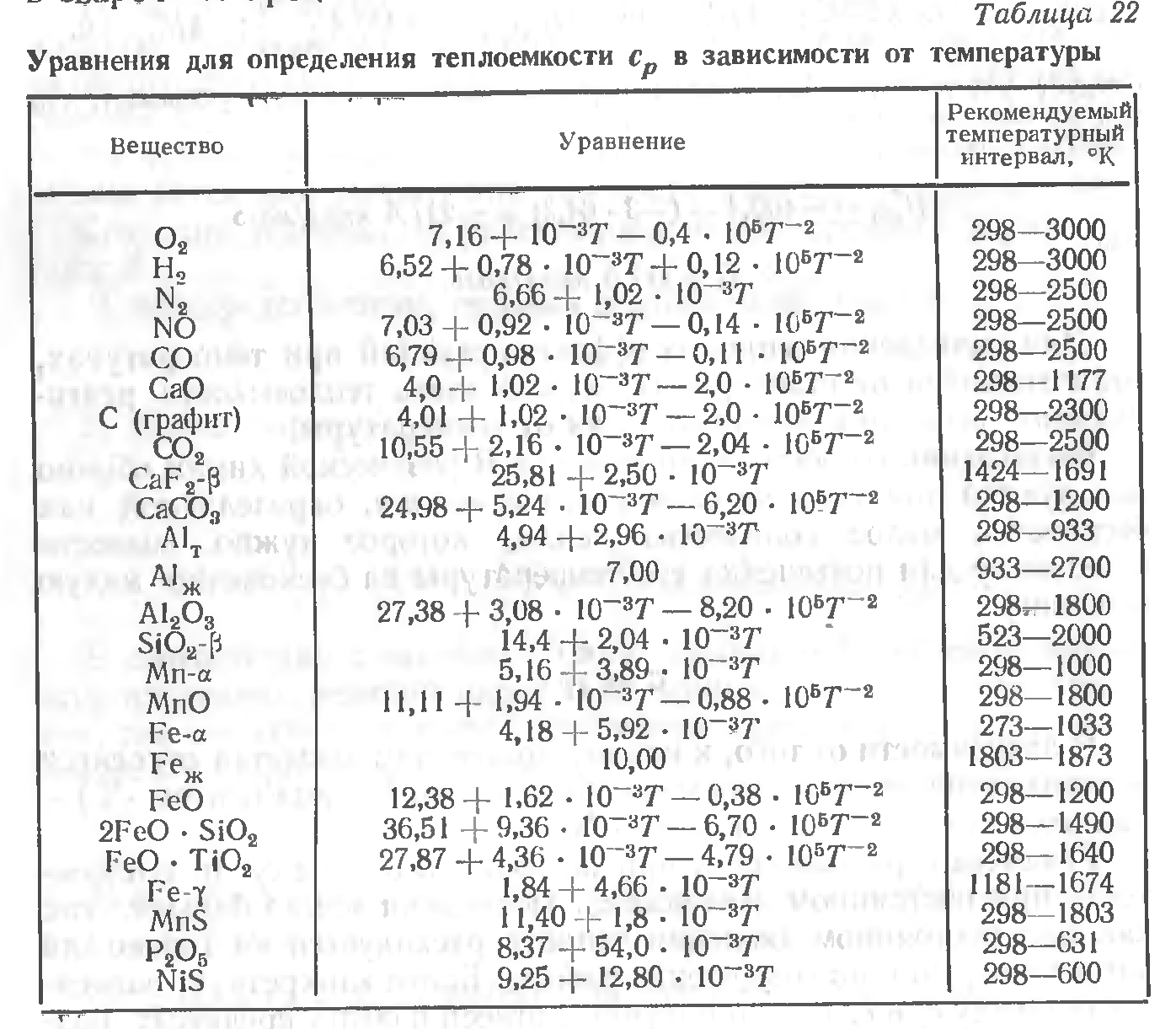 VACF здесь показывает, что режимы движения различны в продольном ( x — и y -) направлении и перпендикулярном ( z -) направлении.Таким образом, мы сравниваем ВАКФ в разных наноканалах в продольном и перпендикулярном направлениях соответственно. Мы находим, что ВАКФ в продольном направлении быстрее всего сходится в канале с H = 2 σ , но медленнее в объеме, а в перпендикулярном направлении наоборот. Анизотропные режимы движения в разных направлениях и в каналах разной высоты свидетельствуют о несоответствии колебательных характеристик объему.
VACF здесь показывает, что режимы движения различны в продольном ( x — и y -) направлении и перпендикулярном ( z -) направлении.Таким образом, мы сравниваем ВАКФ в разных наноканалах в продольном и перпендикулярном направлениях соответственно. Мы находим, что ВАКФ в продольном направлении быстрее всего сходится в канале с H = 2 σ , но медленнее в объеме, а в перпендикулярном направлении наоборот. Анизотропные режимы движения в разных направлениях и в каналах разной высоты свидетельствуют о несоответствии колебательных характеристик объему.
РИСУНОК 4 . VACF и VDOS молекул воды, представленных атомами кислорода.
Затем мы вычисляем VDOS воды, где молекула воды представлена атомом кислорода, в различных каналах (см. рис. 4B), используя следующую зависимость:
VDOS(ω)=∫VACF(t)exp(−2πiωt)dt ,(5)
где ω — угловая частота колебаний атомов. Высокочастотное движение соответствует более высокому энергетическому состоянию.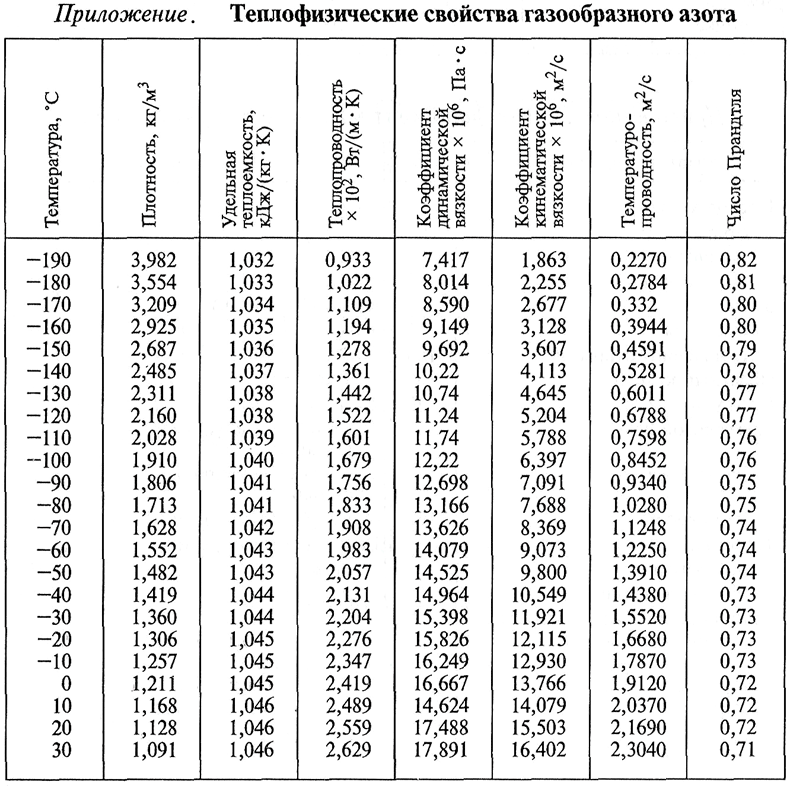 Таким образом, абсцисса на рис. 4В обычно выражается как х в единицах энергии, где х — приведенная постоянная Планка.
Таким образом, абсцисса на рис. 4В обычно выражается как х в единицах энергии, где х — приведенная постоянная Планка.
VDOS представляет возможность распределения режимов вибрации.В общем, острый характерный пик в VDOS соответствует гармонической моде колебаний, а другие — ангармоническим модам колебаний. Тем не менее оба они вносят вклад в удельную теплоемкость. Поскольку SPC/E представляет собой жесткую модель воды с фиксированной связью и углом, единственный пик в VDOS, соответствующий 5,93 мэВ, представляет собой поступательное движение молекул воды. Установлено, что VDOS пика выше объемного значения и уменьшается с размером канала в продольном направлении, но, наоборот, в перпендикулярном направлении.Наиболее существенное различие проявляется в наноканале с H = 2 σ , где пик в перпендикулярном направлении необычайно выше, чем в продольном направлении, и в других случаях, демонстрируя особенность вибрации твердого тела.
Тем не менее, независимо от того, в продольном или перпендикулярном направлении, VDOS низкоэнергетических мод снижается, а VDOS высокоэнергетических мод увеличивается в замкнутой воде, что согласуется с увеличением внутренней энергии, или, точнее говоря, потенциальная энергия. Особая низкоэнергетическая мода, соответствующая ω , стремящаяся к нулю, пропорциональна коэффициенту диффузии. Как и предсказывает пересечение VDOS, коэффициент диффузии в продольном направлении выше, чем в перпендикулярном направлении. То есть коэффициент диффузии анизотропен. Можно также сделать вывод, что коэффициенты диффузии замкнутой воды ниже объемного значения во всех направлениях и уменьшаются по мере уменьшения размера канала, что согласуется с результатами, опубликованными в литературе (Zhao et al., 2020в; Куи и др., 2021). Показано, что движение молекул воды, заключенных в наноканале, ограничено, в основном, за счет адсорбции стенкой.
Особая низкоэнергетическая мода, соответствующая ω , стремящаяся к нулю, пропорциональна коэффициенту диффузии. Как и предсказывает пересечение VDOS, коэффициент диффузии в продольном направлении выше, чем в перпендикулярном направлении. То есть коэффициент диффузии анизотропен. Можно также сделать вывод, что коэффициенты диффузии замкнутой воды ниже объемного значения во всех направлениях и уменьшаются по мере уменьшения размера канала, что согласуется с результатами, опубликованными в литературе (Zhao et al., 2020в; Куи и др., 2021). Показано, что движение молекул воды, заключенных в наноканале, ограничено, в основном, за счет адсорбции стенкой.
Вклад мод колебаний в различных энергетических состояниях в c v , определенный как c v | ω , можно приблизительно оценить с помощью следующего выражения (Gautam et al., 2018): 6)
Таким образом, мы знаем, что вклад более низкой энергетической моды больше, если VDOS одинаковы. Тогда можно просто сделать вывод, что c v нанозамкнутой воды будет уменьшаться по мере уменьшения VDOS низкоэнергетических мод и увеличения VDOS высокоэнергетических мод. Таким образом, с вибрационного аспекта мы заключаем, что уменьшение c v нанозамкнутой воды является результатом снижения низкоэнергетических колебательных мод, вызванных дополнительным взаимодействием жидкости и твердого тела и измененной структурой.
Тогда можно просто сделать вывод, что c v нанозамкнутой воды будет уменьшаться по мере уменьшения VDOS низкоэнергетических мод и увеличения VDOS высокоэнергетических мод. Таким образом, с вибрационного аспекта мы заключаем, что уменьшение c v нанозамкнутой воды является результатом снижения низкоэнергетических колебательных мод, вызванных дополнительным взаимодействием жидкости и твердого тела и измененной структурой.
Заключение
В этой работе мы проводим МД-моделирование для исследования удельной теплоемкости воды, заключенной в чрезвычайно узких графеновых наноканалах, с точки зрения конфигурации и вибрации.Установлено, что удельная теплоемкость замкнутой воды ниже объемной и уменьшается с уменьшением высоты канала. В частности, эффект соизмеримости проявляется при уменьшении высоты канала до 5,5 σ , примерно 1,7 нм. Из распределения плотности обнаружено, что слоистая структура появляется рядом со стенками графена и отличает структуру замкнутой воды от объемной воды. При высоте канала менее 5,5 σ слои начинают смешиваться друг с другом, что приводит к эффекту соизмеримости.Такая структура не подходит для образования и поддержания водородных связей. Поскольку доля слоистой структуры, приходящаяся на долю каналов, увеличивается с уменьшением высоты каналов, координационное число водородных связей уменьшается. Уменьшение числа водородных связей приводит к уменьшению удельной теплоемкости. Кроме того, изменение конфигурации приводит к изменению режимов вибрации. При этом VDOS низкоэнергетических мод колебаний уменьшается, а VDOS высокоэнергетических мод колебаний увеличивается.Поскольку моды колебаний с более низкой энергией вносят больший вклад в удельную теплоемкость, чем моды колебаний с более высокой энергией, удельная теплоемкость воды уменьшается в наноканале. Эта работа демонстрирует ингибирование чрезвычайно узкими графеновыми наноканалами удельной теплоемкости заключенной в них воды и раскрывает лежащие в их основе физические механизмы.
При высоте канала менее 5,5 σ слои начинают смешиваться друг с другом, что приводит к эффекту соизмеримости.Такая структура не подходит для образования и поддержания водородных связей. Поскольку доля слоистой структуры, приходящаяся на долю каналов, увеличивается с уменьшением высоты каналов, координационное число водородных связей уменьшается. Уменьшение числа водородных связей приводит к уменьшению удельной теплоемкости. Кроме того, изменение конфигурации приводит к изменению режимов вибрации. При этом VDOS низкоэнергетических мод колебаний уменьшается, а VDOS высокоэнергетических мод колебаний увеличивается.Поскольку моды колебаний с более низкой энергией вносят больший вклад в удельную теплоемкость, чем моды колебаний с более высокой энергией, удельная теплоемкость воды уменьшается в наноканале. Эта работа демонстрирует ингибирование чрезвычайно узкими графеновыми наноканалами удельной теплоемкости заключенной в них воды и раскрывает лежащие в их основе физические механизмы. Полученные результаты закладывают основу для последующих научных исследований и дают основные данные об удельной теплоемкости воды, заключенной в наноканалы, для приложений в энергетике.
Полученные результаты закладывают основу для последующих научных исследований и дают основные данные об удельной теплоемкости воды, заключенной в наноканалы, для приложений в энергетике.
Заявление о доступности данных
Первоначальные материалы, представленные в исследовании, включены в статью/дополнительный материал; дальнейшие запросы можно направлять соответствующему автору.
Вклад авторов
RZ, XM, HL и CS задумали и разработали моделирование. RZ выполнил моделирование, проанализировал данные и написал первый черновик рукописи. CS и BB пересмотрели рукопись. Все авторы внесли свой вклад в доработку рукописи, прочитали и одобрили представленную версию.
Финансирование
Исследование финансировалось Национальным фондом естественных наук Китая для общего проекта №. 51876169.
Конфликт интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.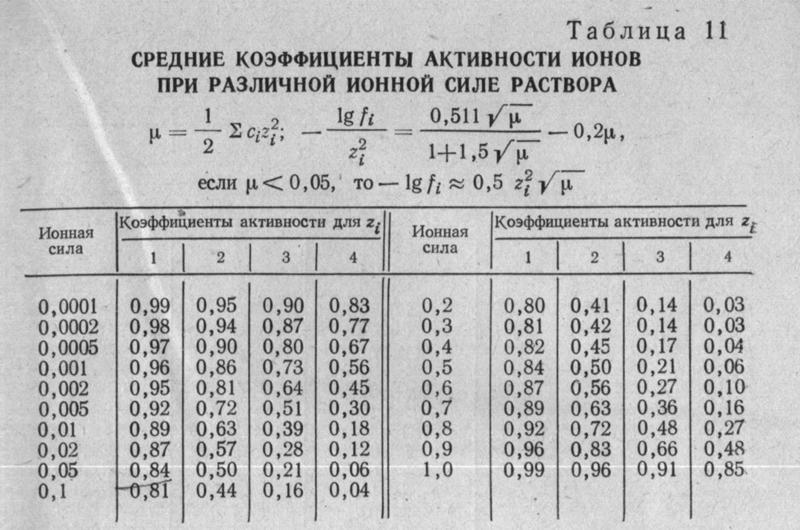
Примечание издателя
Все утверждения, изложенные в этой статье, принадлежат исключительно авторам и не обязательно представляют претензии их дочерних организаций или издателя, редакторов и рецензентов.Любой продукт, который может быть оценен в этой статье, или претензии, которые могут быть сделаны его производителем, не гарантируются и не поддерживаются издателем.
Дополнительный материал
Дополнительный материал к этой статье можно найти в Интернете по адресу: https://www.frontiersin.org/articles/10.3389/fenrg.2021.736713/full#supplementary-material
Ссылки
A. Alkhwaji. , Эльбахлул, С., Абдулла, М.З., и Бакар, KFBA (2021). Выбранные тепловые свойства воды из молекулярной динамики для инженерных целей. Дж. Мол. Жидкости 324, 114703. doi:10.1016/j.molliq.2020.114703
CrossRef Полный текст | Google Scholar
Бави О. и Гадак Ф. (2021). Возможность создания аэрофобных поверхностей с помощью нановыступов: исследование трения атомного масштаба на границах раздела воздух-твердое тело. Физ. хим. хим. физ. 23, 4711–4717. doi:10.1039/d0cp06404a
Физ. хим. хим. физ. 23, 4711–4717. doi:10.1039/d0cp06404a
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Берендсен Х. Дж. К., Григера Дж. Р. и Страатсма Т.П. (1987). Недостающий член в эффективных парных потенциалах. J. Phys. хим. 91, 6269–6271. doi:10.1021/j100308a038
CrossRef Полный текст | Google Scholar
Cui, S.H., Fu, JF, Guo, M.L., Zhao, Z.X., Sun, C.Z., and Wang, YJ (2021). Диффузия высокотемпературного и высоконапорного газа Ch5 в наноканалах SiO2. Фронт Энерг. Res 9, 667640. doi:10.3389/fenrg.2021.667640
CrossRef Full Text | Google Scholar
Гаутам С., Колесников А.И., Ротер Г., Дай С., Цяо З.-А. и Коул Д. (2018). Влияние ограничения и давления на вибрационное поведение наноограниченного пропана. J. Phys. хим. А. 122, 6736–6745. doi:10.1021/acs.jpca.8b05028
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Хамид И., Джалали Х., Питерс Ф. М. и Ник-Амаль М. (2021). Аномальная плоская диэлектрическая проницаемость и сегнетоэлектричество замкнутой воды: от субнанометровых каналов до объема. J. Chem. физ. 154, 114503. doi:10.1063/5.0038359
М. и Ник-Амаль М. (2021). Аномальная плоская диэлектрическая проницаемость и сегнетоэлектричество замкнутой воды: от субнанометровых каналов до объема. J. Chem. физ. 154, 114503. doi:10.1063/5.0038359
CrossRef Full Text | Google Scholar
Haynes, WM (2014). CRC Справочник по химии и физике . Флорида: пресса CRC.
Google Scholar
Изади А., Сиаваши М., Расам Х. и Сюн К. (2020). МГД-усиленная теплопередача с помощью наножидкостей в пористом металле для охлаждения ЦП. Заяв. Терм. англ. 168, 114843. doi:10.1016/j.applthermaleng.2019.114843
CrossRef Полный текст | Google Scholar
Джин, Л., Noraldeen, SFM, Zhou, L., and Du, X. (2021). Влияние границы раздела твердое тело/жидкость на зависящую от размера удельную теплоемкость наноразмерных пленок воды: результаты молекулярного моделирования. Равновесия в жидкой фазе 537, 113001. doi:10.1016/j.fluid.2021.113001
CrossRef Полный текст | Google Scholar
Йоргенсен В. Л. и Тирадо-Ривз Дж. (2005). Функции потенциальной энергии для моделирования воды, органических и биомолекулярных систем на атомном уровне. Проц. Натл.акад. науч. 102, 6665–6670. doi:10.1073/pnas.0408037102
Л. и Тирадо-Ривз Дж. (2005). Функции потенциальной энергии для моделирования воды, органических и биомолекулярных систем на атомном уровне. Проц. Натл.акад. науч. 102, 6665–6670. doi:10.1073/pnas.0408037102
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Калашами Х.Г., Ник-Амаль М. и Питерс Ф.М. (2018). Динамика проскальзывания замкнутой воды в капиллярах из оксида графена. Физ. Преподобный Матер. 2, 74004. doi:10.1103/physrevmaterials.2.074004
CrossRef Полный текст | Google Scholar
Lee, W., Kim, K., Jeong, W., Zotti, L.A., Pauly, F., Cuevas, J.C., et al. (2013). Тепловыделение в соединениях атомного масштаба. Природа 498, 209–212. doi:10.1038/nature12183
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Левченко А. А., Колесников А. И., Росс Н. Л., Боэрио-Гоутс Дж., Вудфилд Б. Ф., Ли Г. и др. (2007). Динамика воды, удерживаемой на поверхности TiO2(анатаз)†. J. Phys. хим. А. 111, 12584–12588. doi:10.1021/jp076033j
Phys. хим. А. 111, 12584–12588. doi:10.1021/jp076033j
CrossRef Полный текст | Google Scholar
Нагоэ, А., Огуни, М., и Фухимори, Х. (2015). Низкотемпературная теплоемкость замкнутого жидкого бензола, предполагающая поведение обычных объемных жидкостей. J. Phys. Конденс. Matter 27, 455103. doi:10.1088/0953-8984/27/45/455103
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Ник-Амаль М., Петерс Ф. М., Григорьева И. В., Гейм А. К. (2016). Эффекты соизмеримости в вязкости нанозамкнутой воды. ACS Nano 10, 3685–3692. doi:10.1021/acsnano.6b00187
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Патрия, Р., и Бил, П. Д. (2011). Статистическая механика .Флорида: CRC press, 744.
Google Scholar
Sekerka, RF (2015). Теплофизика: термодинамика и статистическая механика для ученых и инженеров . Нидерланды: Эльзевир.
Google Scholar
Шадлу-Джахроми А.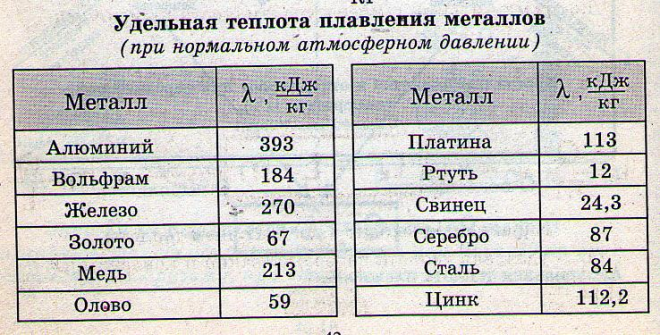 , Харати-Купаи М. и Бави О. (2020). Расчет коэффициента трения в наноканалах с различной гидрофобностью стенок и супергидрофобными структурами: молекулярно-динамическое моделирование. Междунар. коммун. Тепломассообмен 117, 104763.doi:10.1016/j.icheatmasstransfer.2020.104763
, Харати-Купаи М. и Бави О. (2020). Расчет коэффициента трения в наноканалах с различной гидрофобностью стенок и супергидрофобными структурами: молекулярно-динамическое моделирование. Междунар. коммун. Тепломассообмен 117, 104763.doi:10.1016/j.icheatmasstransfer.2020.104763
CrossRef Полный текст | Google Scholar
Шадлу-Джахроми, А., Харати-Купаи, М., и Бави, О. (2021). Молекулярно-динамическое моделирование течения жидкости через наноканалы, состоящие из различных супергидрофобных структур. Междунар. коммун. Тепломассообмен 124. doi:10.1016/j.icheatmasstransfer.2021.105278
CrossRef Полный текст | Google Scholar
Ши К., Боэрио-Гоутс Дж., Вудфилд К., Риттинг М., Пульсифер К., Spencer, E.C., et al. (2012). Исследования теплоемкости поверхностных вод, ограниченных наночастицами касситерита (SnO2). J. Phys. хим. C 116, 3910–3917. doi:10.1021/jp2088862
CrossRef Полный текст | Google Scholar
Софос Ф., Каракасидис Т.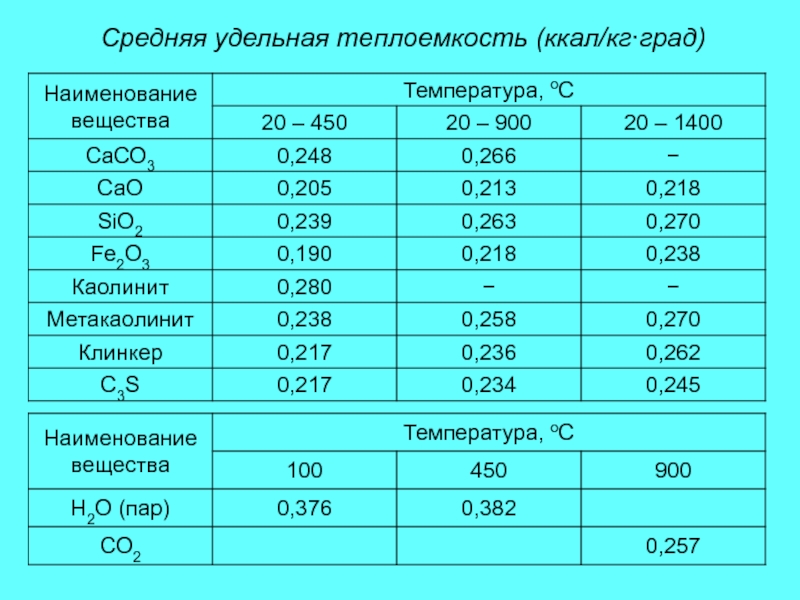 Э. и Лиакопулос А. (2013). Поток жидкости в наномасштабе: как свойства жидкости отличаются от объема. Nanosci Nanotechnol Lett. 5, 457–460. doi:10.1166/nnl.2013.1555
Э. и Лиакопулос А. (2013). Поток жидкости в наномасштабе: как свойства жидкости отличаются от объема. Nanosci Nanotechnol Lett. 5, 457–460. doi:10.1166/nnl.2013.1555
CrossRef Полный текст | Google Scholar
Стиневельд, Г.J., Koopmans, S., Heusinkveld, BG, и Theeuwes, NE (2014). Обновление роли открытых водных поверхностей в смягчении максимального эффекта городского теплового острова. Пейзаж Градостроительный план. 121, 92–96. doi:10.1016/j.landurbplan.2013.09.001
CrossRef Полный текст | Google Scholar
Сунь К., Чжоу Р., Чжао З. и Бай Б. (2021). Расширение классической теории континуума для описания потока воды через двумерные нанопоры. Ленгмюр 37, 6158–6167. дои: 10.1021/acs.langmuir.1c00298
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Сунь К., Чжоу Р., Чжао З. и Бай Б. (2021). Выявление зависящей от гидроксила вязкости воды в наноканалах оксида графена с помощью моделирования молекулярной динамики. Хим. физ. лат. 778, 138808. doi:10.1016/j.cplett.2021.138808
Хим. физ. лат. 778, 138808. doi:10.1016/j.cplett.2021.138808
CrossRef Полный текст | Google Scholar
Томбари Э., Сальветти Г., Феррари К. и Джохари Г. П. (2005). Термодинамические функции воды и льда ограничены порами радиусом 2 нм. J. Chem. физ. 122, 104712. doi:10.1063/1.1862244
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Вега, К., Конде, М. М., Макбрайд, К., Абаскал, Дж. Л. Ф., Ноя, Э. Г., Рамирес, Р., и др. (2010). Теплоемкость воды: признак ядерных квантовых эффектов. J. Chem. физ. 132, 046101. doi:10.1063/1.3298879
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Вила Верде А., Болуис П. Г. и Кампен Р. К. (2012).Статика и динамика свободных и связанных водородом групп ОН на границе раздела воздух/вода. J. Phys. хим. Б 116, 9467–9481. doi:10.1021/jp304151e
CrossRef Полный текст | Google Scholar
Чжао З. Х., Сунь Ч. З. и Чжоу Р.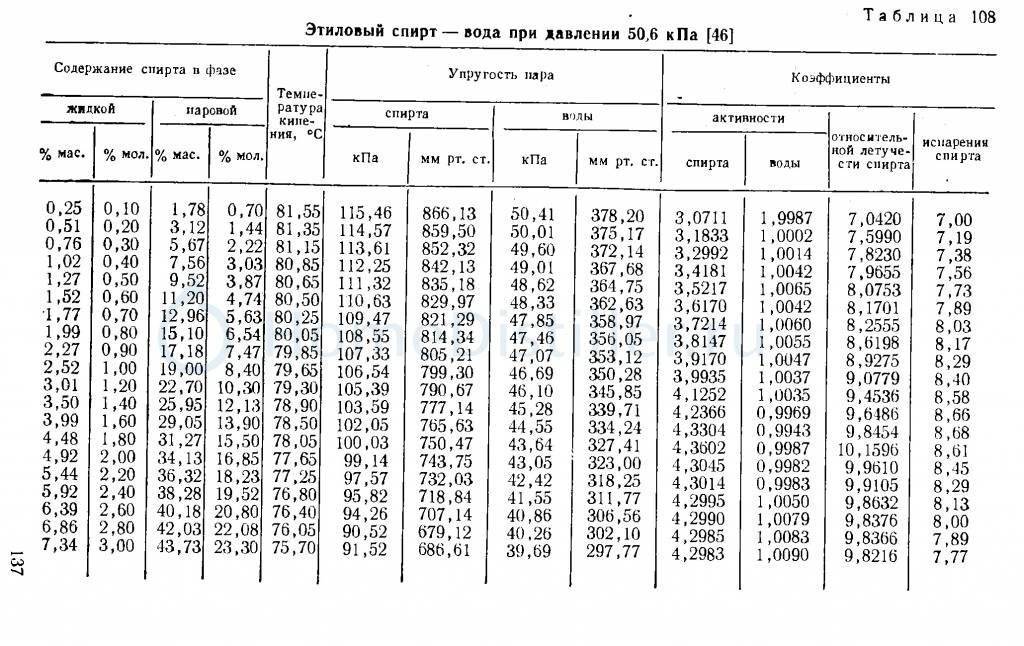 Ф. (2020). Теплопроводность замкнутой воды в графеновых наноканалах. Междунар. J. Heat Mass. Tran 152, 119502. doi:10.1016/j.ijheatmasstransfer.2020.119502
Ф. (2020). Теплопроводность замкнутой воды в графеновых наноканалах. Междунар. J. Heat Mass. Tran 152, 119502. doi:10.1016/j.ijheatmasstransfer.2020.119502
CrossRef Полный текст | Google Scholar
Чжао, З. X., Чжоу, Р.Ф., и Сунь, Ч.З. (2020). Иерархический тепловой перенос в нанозамкнутой воде. J. Chem. физ. 153, 234701. doi:10.1063/5.0030738
CrossRef Full Text | Google Scholar
Чжао, З. Х., Чжоу, Р. Ф., и Сунь, Ч. З. (2020). Молекулярно-динамическое исследование диффузии воды в графеновых наноканалах. Междунар. Дж. Термофиз. 41. doi:10.1007/s10765-020-02660-5
CrossRef Full Text | Google Scholar
Чжоу Р. Ф., Сун С. З. и Бай Б.Ф. (2021). Трение о стенки должно быть отделено от вязкости жидкости для прогнозирования наноразмерного потока. J. Chem. физ. 154, 074709. doi:10.1063/5.0039228
CrossRef Full Text | Google Scholar
Плотность воды | Геологическая служба США
• Школа наук о воде ДОМАШНЯЯ СТРАНИЦА • Темы свойств воды •
Плотность воды
Если вы еще учитесь в школе, вы, вероятно, слышали это утверждение на уроках естествознания: » Плотность — это масса вещества на единицу объема».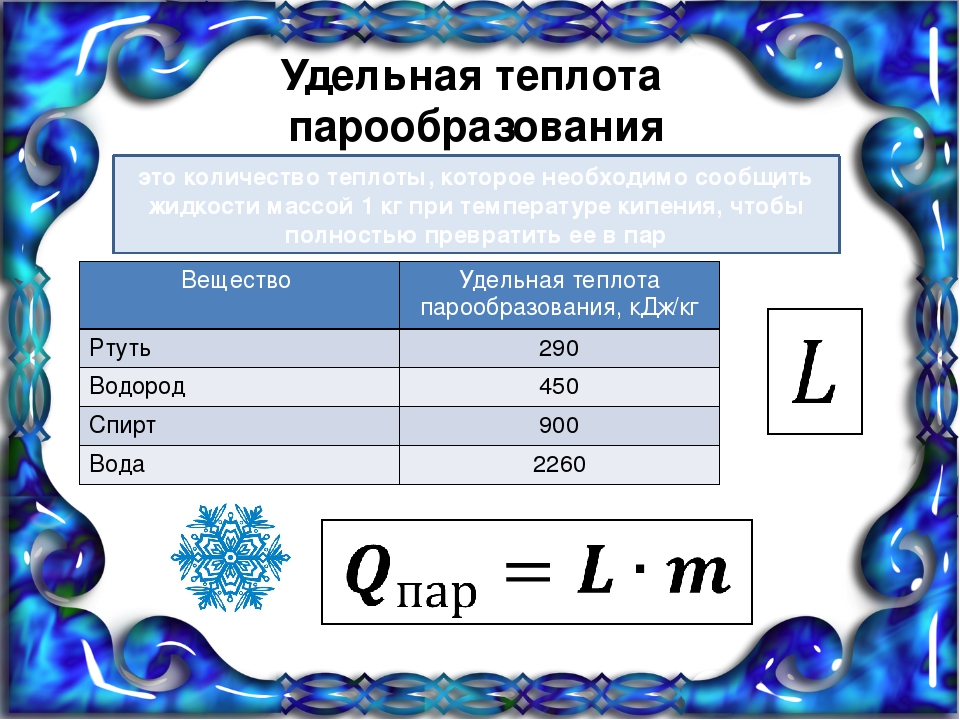 На Земле вы можете предположить, что масса равна весу, если это упрощает задачу.
На Земле вы можете предположить, что масса равна весу, если это упрощает задачу.
Если вы еще не в школе, то вы, вероятно, забыли, что вообще когда-либо слышали это. Определение плотности имеет гораздо больше смысла с небольшим объяснением. Пока объект состоит из молекул и, следовательно, имеет размер или массу, он имеет плотность. Плотность — это просто вес выбранного количества (объема) материала. Общепринятой единицей измерения плотности воды является грамм на миллилитр (1 г/мл) или 1 грамм на кубический сантиметр (1 г/см 3 ).
На самом деле, точная плотность воды на самом деле не 1 г/мл, а немного меньше (очень, очень немного меньше), 0,9998395 г/мл при 4,0° по Цельсию (39,2° по Фаренгейту). Однако чаще всего вы будете видеть округленное значение 1 г/мл.
Плотность воды зависит от температуры
Расти со старшим братом было трудно, особенно когда к нему приходили его друзья, потому что их любимым занятием было думать о том, как насолить мне. Однако однажды я смог использовать плотность воды, чтобы, по крайней мере, подшутить над ними.В один из жарких летних дней они забрались на огромный холм рядом с нашим домом, чтобы выкопать яму, чтобы спрятать свою коллекцию бутылочных крышек. Им захотелось пить, и они заставили меня вернуться домой и принести им галлон воды. Этот галлон водопроводной воды при температуре 70 ° F весил 8,329 фунта, что было много для 70-фунтового ребенка, чтобы подняться на огромный холм.
Однако однажды я смог использовать плотность воды, чтобы, по крайней мере, подшутить над ними.В один из жарких летних дней они забрались на огромный холм рядом с нашим домом, чтобы выкопать яму, чтобы спрятать свою коллекцию бутылочных крышек. Им захотелось пить, и они заставили меня вернуться домой и принести им галлон воды. Этот галлон водопроводной воды при температуре 70 ° F весил 8,329 фунта, что было много для 70-фунтового ребенка, чтобы подняться на огромный холм.
Итак, когда они потребовали еще галлон воды, я заглянул в «Интернет» того дня — энциклопедию — и узнал, что галлон воды с температурой кипения весит всего 7.996 фунтов! Я взбежал на холм, неся свой галлон воды, который весил на 0,333 фунта меньше; и побежали вниз еще быстрее, их сердитые голоса затихли позади меня.
| Температура (°F/°C) | Плотность (грамм/см 3 | Вес (фунт/фут 3 |
|---|---|---|
| 32°F/0°C | 0,99987 | 62.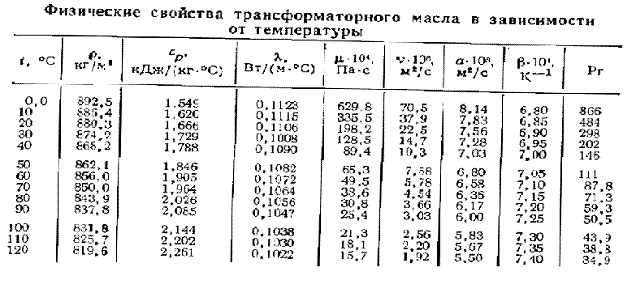 416 416 |
| 39,2°F/4,0°C | 1.00000 | 62.424 |
| 40°F/4,4°C | 0,99999 | 62.423 |
| 50°F/10°C | 0,99975 | 62.408 |
| 60°F/15,6°C | 0,99907 | 62,366 |
| 70°F/21°C | 0,99802 | 62.300 |
| 80°F/26,7°C | 0,99669 | 62.217 |
| 90°F/32,2°C | 0,99510 | 62,118 |
| 100°F/37.8°С | 0,99318 | 61,998 |
| 120°F/48,9°C | 0,98870 | 61.719 |
| 140°F/60°C | 0,98338 | 61,386 |
| 160°F/71,1°C | 0,97729 | 61.006 |
| 180°F/82,2°C | 0,97056 | 60.586 |
| 200°F/93,3°C | 0,96333 | 60.135 |
| 212°F/100°C | 0. 95865 95865 | 59.843 |
Источник: Министерство внутренних дел США, Бюро мелиорации, 1977 г., Руководство по подземным водам , из
Энциклопедия водных ресурсов, третье издание, гидрологические данные и интернет-ресурсы, под редакцией Педро Фиерро-младшего
и Эвана К. Найлер, 2007
Лед менее плотный, чем вода
Если вы посмотрите на это изображение, то увидите, что часть айсберга находится ниже уровня воды. Это не удивительно, но на самом деле почти весь объем айсберга находится ниже ватерлинии, а не над ней.Это связано с тем, что плотность льда меньше плотности жидкой воды. При замерзании плотность льда уменьшается примерно на 9 процентов.
Большая часть айсберга находится ниже поверхности воды.
Лучший способ представить себе, как вода может иметь разную плотность, — это посмотреть на замерзшую воду. Лед на самом деле имеет совсем другую структуру, чем жидкая вода, в которой молекулы выстраиваются в правильную решетку, а не более беспорядочно, как в жидкой форме. Бывает, что решетчатое устройство позволяет молекулам воды быть более разбросанными, чем в жидкости, и, таким образом, лед менее плотен, чем вода.Опять же, к счастью для нас, так как мы не услышали бы восхитительного звона кубиков льда о стенку стакана, если бы лед в нашем чае со льдом опустился на дно. Плотность льда составляет около 90 процентов от плотности воды, но она может варьироваться, поскольку лед также может содержать воздух. Это означает, что около 10 процентов ледяного куба (или айсберга) будет находиться над ватерлинией.
Бывает, что решетчатое устройство позволяет молекулам воды быть более разбросанными, чем в жидкости, и, таким образом, лед менее плотен, чем вода.Опять же, к счастью для нас, так как мы не услышали бы восхитительного звона кубиков льда о стенку стакана, если бы лед в нашем чае со льдом опустился на дно. Плотность льда составляет около 90 процентов от плотности воды, но она может варьироваться, поскольку лед также может содержать воздух. Это означает, что около 10 процентов ледяного куба (или айсберга) будет находиться над ватерлинией.
Это свойство воды имеет решающее значение для всего живого на Земле. Поскольку вода при температуре около 39 ° F (4 ° C) более плотная, чем вода при 32 ° F (0 ° C), в озерах и других водоемах более плотная вода опускается ниже менее плотной воды.Если бы вода была наиболее плотной в точке замерзания, то зимой очень холодная вода на поверхности озер опускалась бы, озеро могло бы замерзнуть снизу вверх. А поскольку вода является таким хорошим изолятором (из-за ее теплоемкости , ), некоторые замерзшие озера могут не полностью оттаять летом.
Реальное объяснение плотности воды на самом деле более сложное, поскольку плотность воды также зависит от количества растворенного в ней вещества. Вода в природе содержит минералы, газы, соли и даже пестициды и бактерии, некоторые из которых растворены.Чем больше вещества растворяется в галлоне воды, тем больше этот галлон будет весить и быть более плотным — океанская вода плотнее чистой воды.
Тяжелые кубики льда опускаются на дно стакана с водой, а обычные плавают.
Авторы и права: Майк Уокер
Мы говорили, что лед плавает на воде, но как насчет «тяжелого льда»?
Мы уже говорили, что лед плавает на воде, потому что он менее плотный, но лед особого вида может быть более плотным, чем обычная вода. «Тяжелый лед» — 10.На 6 процентов плотнее обычной воды, потому что лед состоит из «тяжелой воды». Тяжелая вода, D 2 O вместо H 2 O, представляет собой воду, в которой оба атома водорода заменены дейтерием, изотопом водорода, содержащим один протон и один нейтрон. Тяжелая вода действительно тяжелее обычной воды (которая естественным образом содержит небольшое количество молекул тяжелой воды), и лед из тяжелой воды тонет в обычной воде.
Тяжелая вода действительно тяжелее обычной воды (которая естественным образом содержит небольшое количество молекул тяжелой воды), и лед из тяжелой воды тонет в обычной воде.
Измерение плотности
Ареометр используется для измерения плотности жидкости.
Прибор для измерения плотности жидкости называется ареометром. Это одно из самых простых научно-измерительных устройств, и вы даже можете сделать его сами из пластиковой соломинки (см. ссылки ниже). Однако чаще он сделан из стекла и очень похож на термометр. Он состоит из цилиндрического стержня и утяжеленной груши на дне, чтобы держать его в вертикальном положении. Ареометр осторожно опускают в измеряемую жидкость до тех пор, пока ареометр не начнет свободно плавать. На устройстве есть выгравированные или отмеченные линии, чтобы пользователь мог видеть, насколько высоко или низко плавает ареометр.В менее плотных жидкостях ареометр будет плавать ниже, а в более плотных — выше. Поскольку вода является «стандартом», по которому измеряются другие жидкости, отметка для воды, вероятно, обозначена как «1. 000»; следовательно, удельный вес воды при температуре около 4°C равен 1.000.
000»; следовательно, удельный вес воды при температуре около 4°C равен 1.000.
Ареометры имеют множество применений, не последним из которых является измерение солености воды на уроках естествознания в школах. Они также используются в молочной промышленности для оценки содержания жира в молоке, поскольку молоко с более высоким содержанием жира будет менее плотным, чем молоко с меньшим содержанием жира.Ареометры часто используются людьми, которые делают пиво и вино дома, поскольку они показывают, сколько сахара находится в жидкости, и позволяют пивовару узнать, как далеко зашел процесс брожения.
Сделайте свой собственный ареометр:
Вы думаете, что много знаете о свойствах воды?
Пройдите наш интерактивный тест на определение истинности/неверности свойств воды и проверьте свои знания о воде.
5.1 Свойства воды. Введение в океанографию
Наиболее очевидной особенностью океанов является то, что они содержат воду. Вода настолько вездесуща, что может показаться не очень интересным веществом, но она обладает многими уникальными свойствами, влияющими на глобальные океанографические и климатологические процессы. Многие из этих процессов обусловлены образованием водородных связей между молекулами воды.
Вода настолько вездесуща, что может показаться не очень интересным веществом, но она обладает многими уникальными свойствами, влияющими на глобальные океанографические и климатологические процессы. Многие из этих процессов обусловлены образованием водородных связей между молекулами воды.
Рисунок 5.1.1 Водородные связи (штриховые линии) между молекулами воды. Атомы кислорода показаны красным, атомы водорода — белым (общественное достояние, через Wikimedia Commons).
Молекула воды состоит из двух атомов водорода и одного атома кислорода.Электроны, ответственные за связи между атомами, распределены по всей молекуле неравномерно, так что водородные концы молекул воды имеют небольшой положительный заряд, а кислородный конец имеет небольшой отрицательный заряд, что делает воду полярной молекулой . Отрицательная кислородная сторона молекулы образует притяжение к положительному водородному концу соседней молекулы. Эта довольно слабая сила притяжения называется водородной связью (рис. 5.1.1). Если бы не водородные связи, вода испарялась бы при температуре -68 o C, а это означало, что жидкая вода (и, следовательно, жизнь) не могла бы существовать на Земле.Эти водородные связи ответственны за некоторые уникальные свойства воды:
5.1.1). Если бы не водородные связи, вода испарялась бы при температуре -68 o C, а это означало, что жидкая вода (и, следовательно, жизнь) не могла бы существовать на Земле.Эти водородные связи ответственны за некоторые уникальные свойства воды:
1. Вода – это единственное вещество, существующее в природе в твердом, жидком и газообразном состояниях при обычных для Земли диапазонах температур и давлений. Это связано с относительно высокими температурами замерзания и испарения воды (см. ниже).
2. Вода имеет высокую теплоемкость , которая представляет собой количество тепла, которое необходимо добавить, чтобы повысить ее температуру. Удельной теплоемкостью называют количество теплоты, необходимое для повышения температуры 1 г вещества на 1 o °С.Вода имеет самую высокую удельную теплоемкость из всех жидкостей, кроме аммиака (табл. 5.1.1).
Таблица 5.1.1 Удельная теплота сгорания ряда обычных веществ
| Удельная теплоемкость (калории/г/C o ) | |
|---|---|
| Аммиак | 1,13 |
| Вода | 1,00 |
| Ацетон | 0,51 |
| Зерновой спирт | 0,23 |
| Алюминий | 0. 22 22 |
| Медь | 0,09 |
| Серебро | 0,06 |
Таким образом, вода является одной из самых трудных для нагревания или охлаждения жидкостей; он может поглощать большое количество тепла без повышения его температуры. Помните, что температура отражает среднюю кинетическую энергию молекул внутри вещества; чем энергичнее движение, тем выше температура. В воде молекулы удерживаются вместе водородными связями, и эти связи необходимо преодолеть, чтобы позволить молекулам свободно двигаться.Когда к воде добавляется тепло, энергия должна сначала пойти на разрыв водородных связей, прежде чем температура начнет повышаться. Следовательно, большая часть добавочного тепла поглощается за счет разрыва Н-связей, а не за счет повышения температуры, что придает воде высокую теплоемкость.
Водородные связи также придают воде высокую скрытую теплоту; теплота, необходимая для фазового перехода из твердого состояния в жидкое или из жидкого в газообразное. Скрытая теплота плавления — это теплота, необходимая для перехода из твердого состояния в жидкое; 80 кал/г в случае таяния льда в воду.Лед является твердым телом, потому что водородные связи удерживают молекулы воды в твердой кристаллической решетке (см. ниже). При нагревании льда температура поднимается до 0 o С. В этот момент любое дополнительное тепло идет на плавление льда за счет разрыва водородных связей, а не на повышение температуры. Так что пока есть лед, температура воды не повысится. Вот почему ваш напиток останется холодным, пока в нем есть лед; любое поглощенное тепло идет на таяние льда, а не на подогрев напитка.
Когда весь лед растает, дополнительное тепло повысит температуру воды на 1 o C на каждую добавленную калорию тепла, пока она не достигнет 100 o C. В этот момент любое дополнительное тепло идет на преодоление водородные связи и превращение жидкой воды в водяной пар, а не повышение температуры воды. Теплота, необходимая для испарения жидкой воды в водяной пар, представляет собой скрытую теплоту парообразования , которая имеет значение 540 кал/г (рис. 5.1.2).
Рисунок 5.1.2 Скрытая теплота, необходимая для фазовых переходов в воде. Скрытая теплота плавления — это теплота, необходимая для таяния льда (80 кал/г), а скрытая теплота парообразования — это теплота, необходимая для превращения жидкой воды в водяной пар (540 кал/г) (PW).
Высокая теплоемкость воды помогает регулировать глобальный климат, поскольку океаны медленно поглощают и выделяют тепло, предотвращая резкие колебания температуры (см. раздел 8.1). Это также означает, что водные организмы не так подвержены таким быстрым изменениям температуры, как наземные организмы.У глубоководного организма за всю жизнь температура не может измениться более чем на 0,5 o C, а у наземных видов за один день изменения температуры могут составить более 20 o C!
3. Вода растворяет больше веществ, чем любая другая жидкость; это «универсальный растворитель» , поэтому в океане растворено так много веществ. Вода особенно хорошо растворяет ионные соли; молекулы, состоящие из противоположно заряженных ионов, таких как NaCl (Na + и Cl – ).В воде заряженные ионы притягивают полярные молекулы воды. Ионы окружаются слоем молекул воды, ослабляя связь между ионами до 80 раз. При ослаблении связей между ионами вещество растворяется (рис. 5.1.3).
Рисунок 5.1.3 Притяжение между полярными молекулами воды и заряженными ионами (например, в NaCl) больше, чем притяжение между заряженными ионами, вызывая диссоциацию ионов и растворение соли (PW).
4. Твердая фаза менее плотна, чем жидкая фаза .Другими словами, лед плавает. Большинство веществ более плотные в твердом состоянии, чем в жидком, поскольку их молекулы более плотно упакованы в твердом состоянии. Исключение составляет вода: плотность пресной воды 1,0 г/см 3 , а плотность льда 0,92 г/см 3 , и опять-таки это связано с действием водородных связей.
При понижении температуры воды молекулы замедляются, в конечном итоге замедляясь настолько, что могут образовываться водородные связи и удерживать молекулы воды в кристаллической решетке.Молекулы в решетке расположены дальше друг от друга, чем молекулы в жидкой воде, что делает лед менее плотным, чем жидкая вода (рис. 5.1.4). Это знакомо каждому, кто когда-либо оставлял полную бутылку с водой в морозильной камере только для того, чтобы она лопнула, когда вода замерзнет и расширится.
Рисунок 5.1.4 Структура кристаллической решетки льда, показывающая молекулы воды, удерживаемые вместе водородными связями (автор Adam001d (собственная работа) [CC BY-SA 3.0], через Wikimedia Commons).
Но зависимость между температурой и плотностью воды не является простой линейной.Когда вода охлаждается, ее плотность, как и ожидалось, увеличивается, так как молекулы воды замедляются и сближаются. Однако пресная вода достигает максимальной плотности при температуре 4 o C, и по мере охлаждения выше этой точки ее плотность снижается, поскольку начинают формироваться водородные связи и увеличивается межмолекулярное расстояние (рис. 5.1.5, вставка). Плотность продолжает снижаться до тех пор, пока температура не достигнет 0 o C и не образуются кристаллы льда, резко снижающие плотность (рис. 5.1.5).
Рисунок 5.1.5 По мере снижения температуры плотность воды увеличивается, пока не достигнет максимальной плотности при 4 o C (врезка). Затем плотность немного снижается до 0 o C, где она резко снижается по мере образования кристаллов льда (Клаус-Дитер Келлер, [CC BY-SA 3.0], через Wikimedia Commons).
То, что лед менее плотный, чем вода, имеет ряд важных последствий. Лед, плавающий на поверхности океана, помогает регулировать температуру океана и, следовательно, глобальный климат, влияя на количество солнечного света, который отражается, а не поглощается (см.1). В меньших масштабах поверхностный лед может предотвратить замерзание озер и прудов зимой. По мере того как пресная поверхностная вода охлаждается, она становится более плотной и опускается на дно. Затем новая поверхностная вода охлаждается и опускается, и процесс повторяется в так называемом опрокидывании , при этом более плотная вода опускается, а менее плотная вода движется на поверхность только для того, чтобы охладиться и опуститься. Таким образом, весь водоем охлаждается несколько равномерно. Этот процесс продолжается до тех пор, пока поверхностные воды не остынут ниже 4 o С.Ниже 4 o C вода становится менее плотной по мере охлаждения, поэтому она больше не тонет. Вместо этого он остается на поверхности, становясь все холоднее и менее плотным, пока не замерзнет при температуре 0 o C. Как только пресная вода замерзает, лед всплывает и изолирует остальную воду под ним, уменьшая дальнейшее охлаждение. Самая плотная придонная вода по-прежнему имеет температуру 4 o C, поэтому она не замерзает, позволяя дну озера или пруда оставаться незамерзающим (что является хорошей новостью для живущих там животных), независимо от того, насколько холодно на улице.
Растворенные в морской воде соли препятствуют образованию кристаллической решетки и, следовательно, затрудняют образование льда. Таким образом, морская вода имеет точку замерзания около -2 o C (в зависимости от солености) и замерзает до достижения температуры максимальной плотности. Таким образом, морская вода будет продолжать тонуть по мере того, как становится холоднее, пока, наконец, не замерзнет.
5. Вода имеет очень высокое поверхностное натяжение , самое высокое из всех жидкостей, кроме ртути (таблица 5.1.2). Молекулы воды притягиваются друг к другу водородными связями.Молекулы, не находящиеся на поверхности воды, окружены другими молекулами воды во всех направлениях, поэтому силы притяжения равномерно распределяются во всех направлениях. Но для молекул на поверхности над ними мало соседних молекул, только внизу, поэтому все силы притяжения направлены внутрь, от поверхности (рис. 5.1.6). Эта внутренняя сила заставляет капли воды принимать сферическую форму, а вода собирается на поверхности, поскольку сферическая форма обеспечивает минимально возможную площадь поверхности.Эти силы притяжения также заставляют поверхность воды действовать как эластичная «кожа», которая позволяет таким вещам, как насекомые, сидеть на поверхности воды и не тонуть.
Рисунок 5.1.6 Чистая сила притяжения между молекулами на поверхности направлена внутрь, что приводит к поверхностному натяжению. Для молекул в центре сила одинакова во всех направлениях (PW).
Таблица 5.1.2 Поверхностное натяжение различных жидкостей
| Жидкость | Поверхностное натяжение (миллиньютон/метр) | Температура o С |
|---|---|---|
| Меркурий | 487.00 | 15 |
| Вода | 71,97 | 25 |
| Глицерин | 63,00 | 20 |
| Ацетон | 23,70 | 20 |
| Этанол | 22,27 | 20 |
.

 Объемная теплоемкость воды
Объемная теплоемкость воды 00
00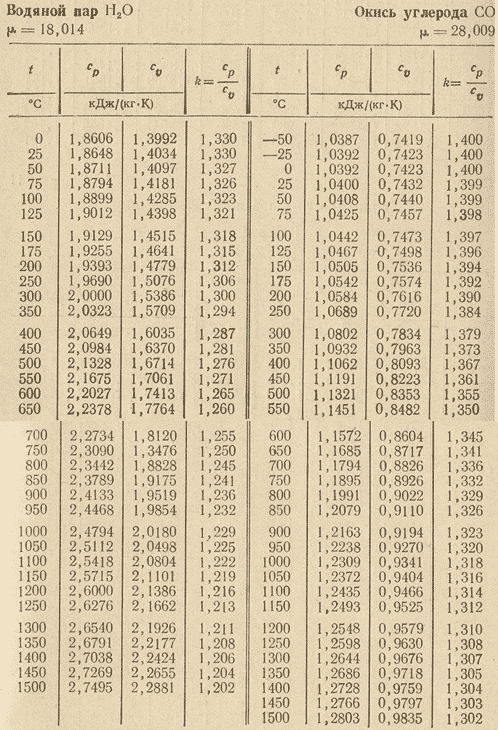 90
90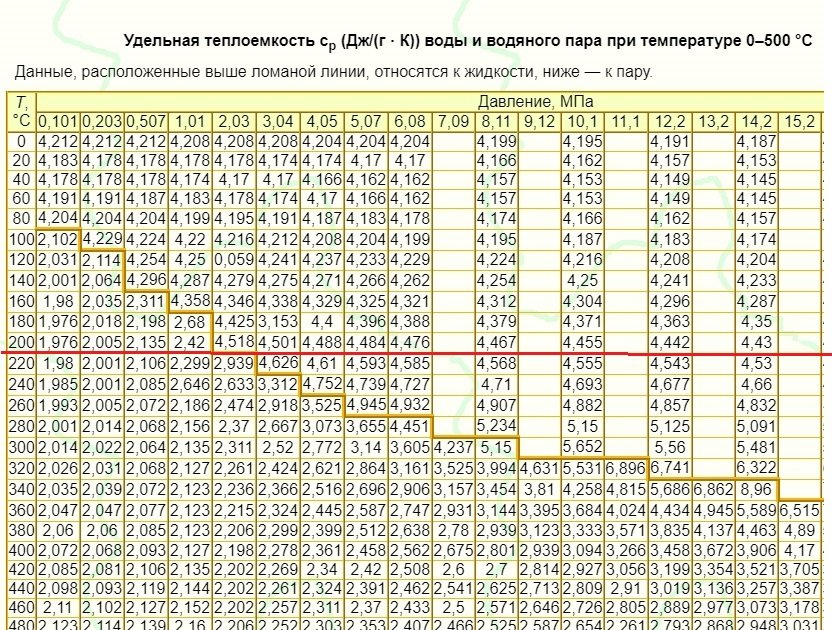 002
002 00
00 41
41 999
999 000891
000891 71
71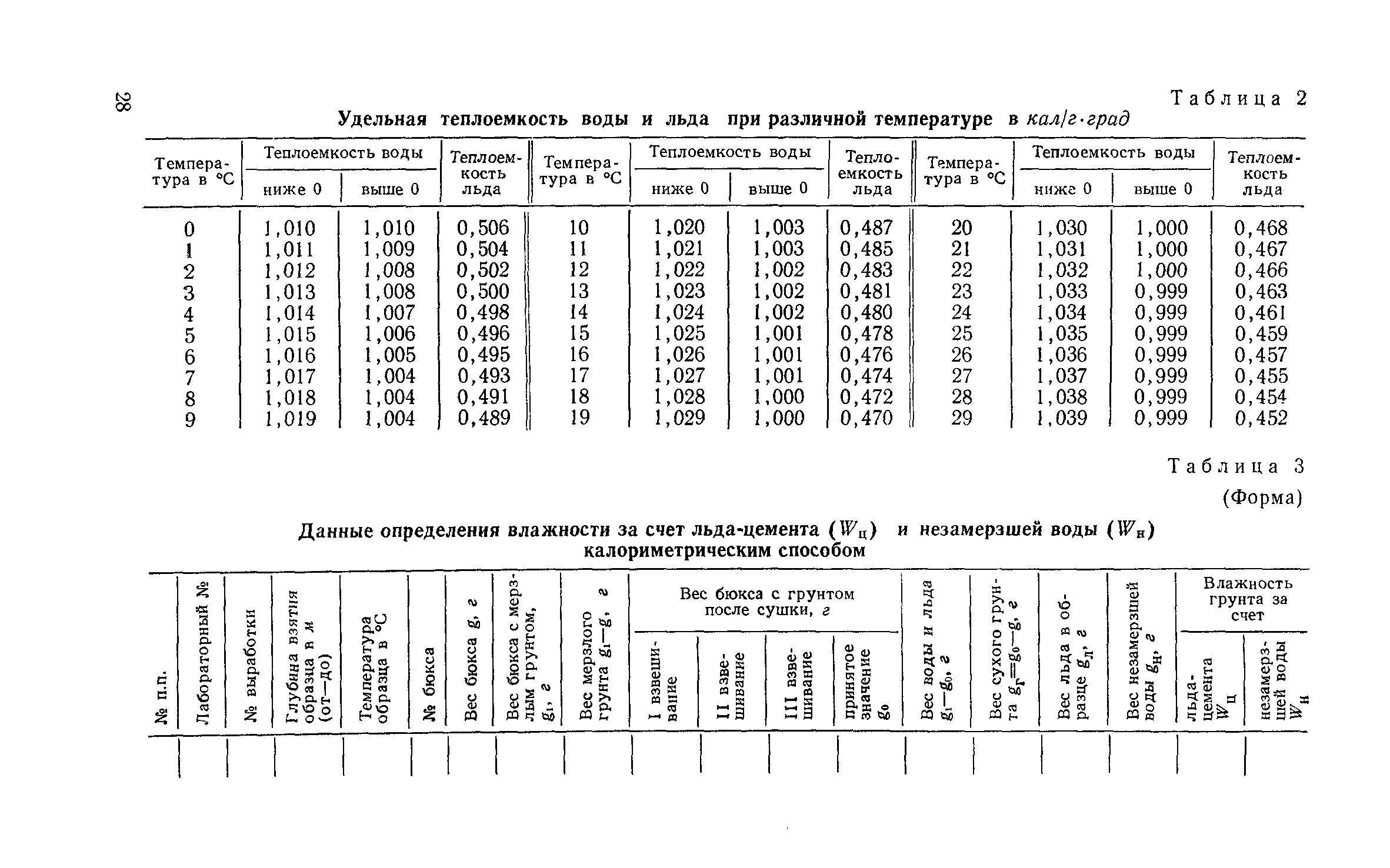 03
03 00
00 25
25 01
01 998
998 000529
000529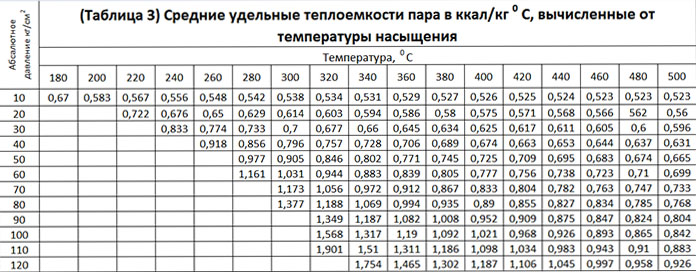 00
00 60
60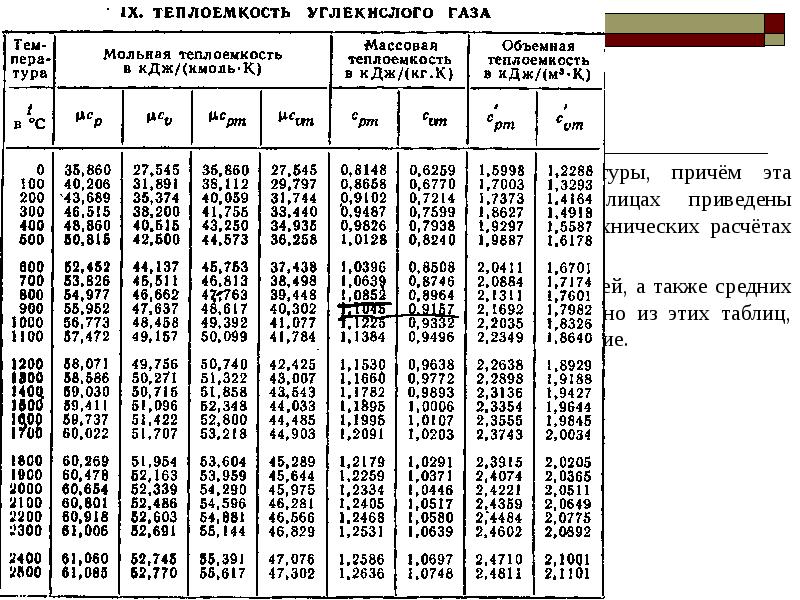 99
99 001
001 000388
000388 00
00 97
97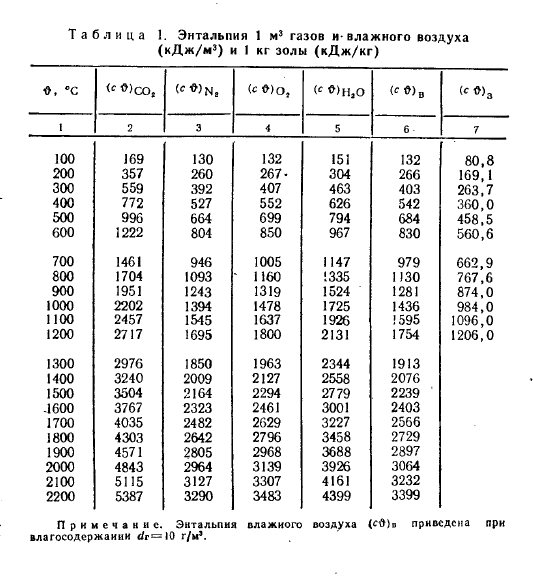 02
02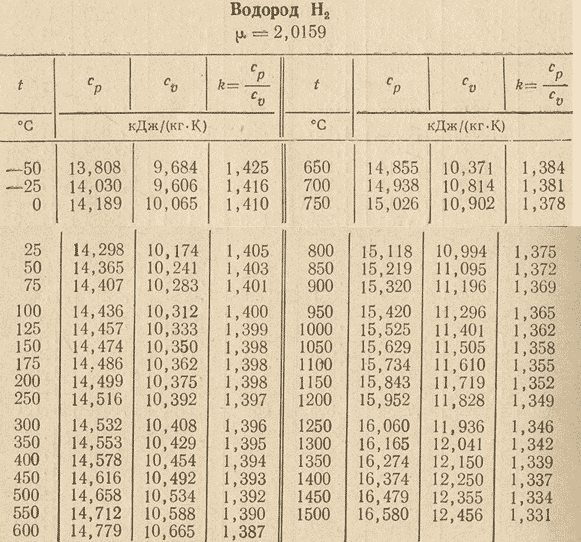 004
004 000304
000304 49
49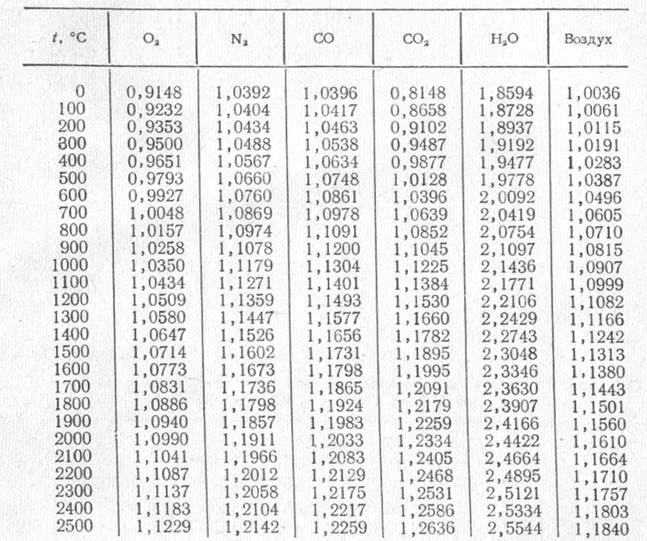
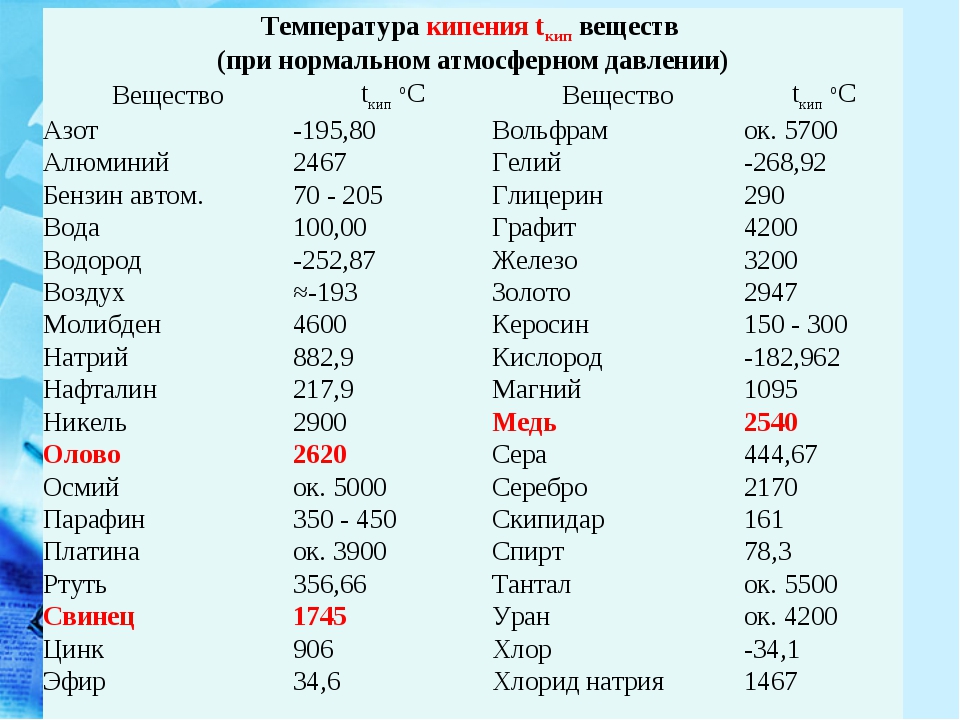
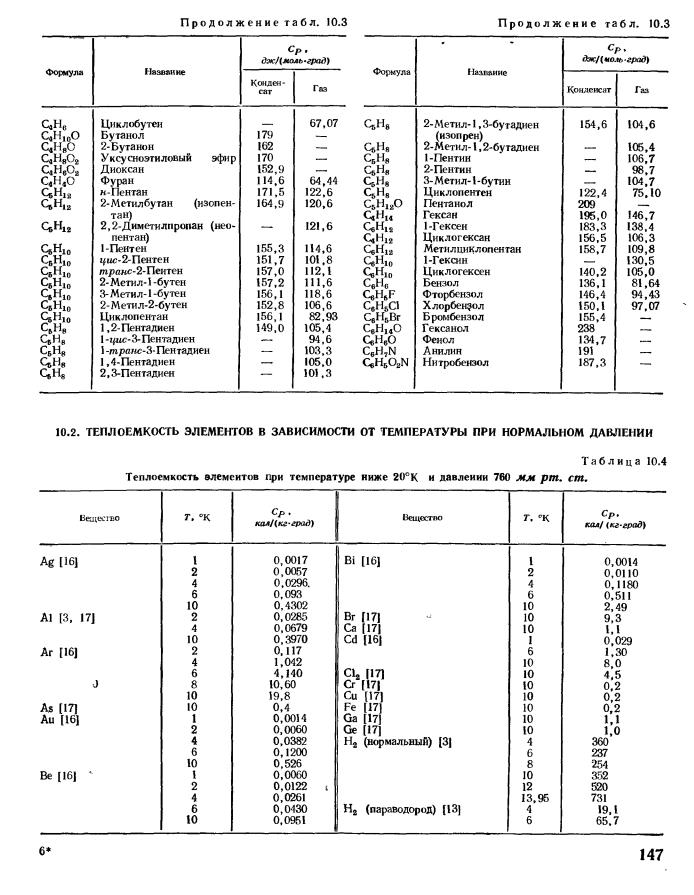 650
650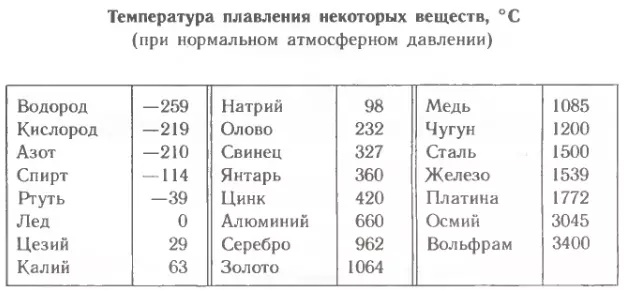 0941
0941 1861
1861 41
41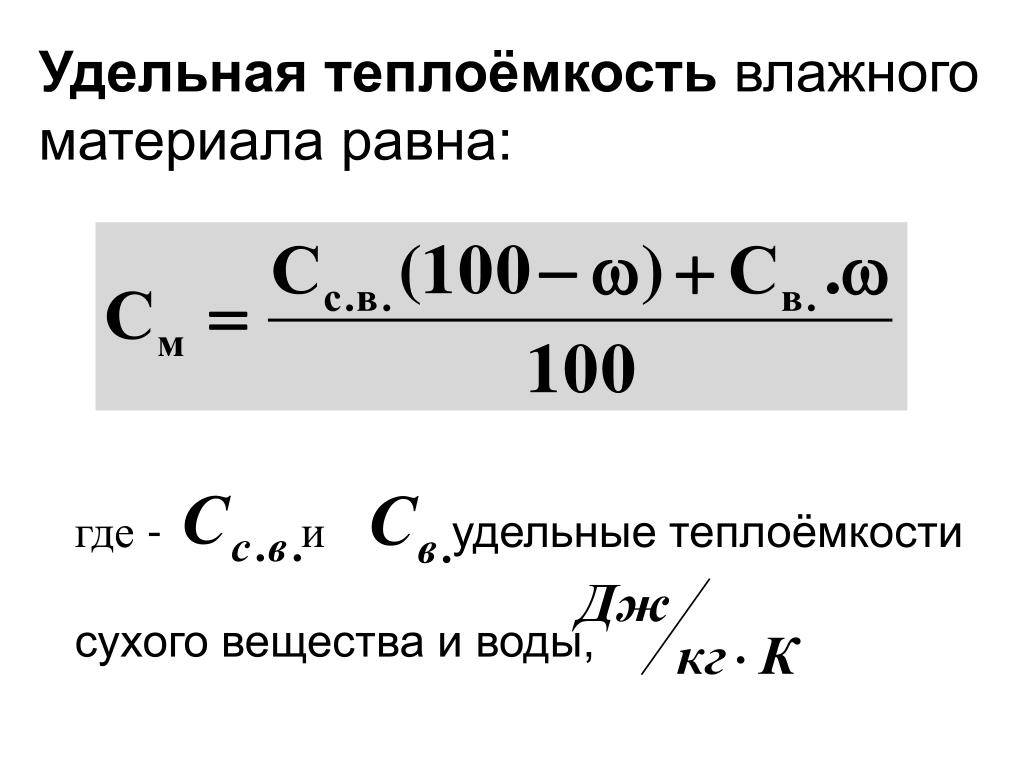 34
34 Вы хотите максимально сохранить тепловую энергию лампы, заключенной в области вашего эксперимента.
Вы хотите максимально сохранить тепловую энергию лампы, заключенной в области вашего эксперимента.